题目
7.在含有固体AgCl的饱和溶液中,加入下列哪种物质,会使AgCl的溶解度降低-|||-A.NaCl __ B.AgNO3 C.NaNO3 D.KBr E.氨水
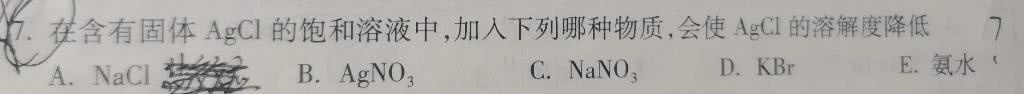
题目解答
答案

解析
本题考查溶度积原理和勒沙特列原理的应用,关键在于分析加入不同物质对AgCl溶解平衡的影响。
核心思路:
- 同离子效应:若加入与AgCl同离子的物质(如NaCl、AgNO₃),会增加对应离子浓度,使平衡左移,溶解度降低。
- 盐效应:加入无关离子的强电解质(如NaNO₃),可能略微增加溶解度,但题目中不考虑此微小变化。
- 沉淀转化:若加入Br⁻,会生成更难溶的AgBr,消耗Ag⁺,使平衡右移,溶解度升高。
- 配位效应:氨水与Ag⁺形成配合物,降低Ag⁺浓度,平衡右移,溶解度升高。
选项分析
A. NaCl
NaCl完全解离为Na⁺和Cl⁻,增加Cl⁻浓度,触发同离子效应,平衡左移,AgCl溶解度降低。
B. AgNO₃
AgNO₃解离为Ag⁺和NO₃⁻,增加Ag⁺浓度,同理通过同离子效应使平衡左移,溶解度降低。
C. NaNO₃
NaNO₃解离为Na⁺和NO₃⁻,与AgCl溶解平衡无关,不改变Ag⁺或Cl⁻浓度,溶解度不变。
D. KBr
KBr解离为K⁺和Br⁻,Br⁻与Ag⁺生成更难溶的AgBr沉淀,消耗Ag⁺,使平衡右移,AgCl溶解度升高。
E. 氨水
氨水与Ag⁺反应生成配合物[Ag(NH₃)₂]⁺,降低Ag⁺浓度,平衡右移,溶解度升高。