101 mg胰岛素溶于 10.0mL 水,该溶液在25.0℃时的渗透压是 4.34kPa,计算胰岛素的摩尔质量和该溶液的蒸气压下降Δp(已知25.0℃水的饱和蒸气压为3.17kPa)。则,0.01+ S / cθ≈0.01,S / cθ= Ksp/0.01=8.5×10-15mol?L-12.将等体积的0.004 mol·L-1AgNO3溶液和0.004 mol·L-1的K2CrO4溶液混合,有无砖红色的Ag2CrO4沉淀析出?已知 (Ag2CrO4)=1.1×10-12。有砖红色沉淀析出。3.1L溶液中含有4molNH4Cl和0.2molNH3,试计算:(1)溶液的[OH-]和pH;(2)在此条件下若有Fe(OH)2沉淀析出,溶液中Fe2+的最低浓度为多少?已知 (Fe(OH)2)=4.9×10-17。解:(1)(2) 4.在0.1mol·L-1ZnCl2溶液中通入H2S气体至饱和,如果加入盐酸以控制溶液的pH,试计算开始析出ZnS沉淀和Zn2+沉淀完全时溶液的pH。已知 (ZnS)=2.5×10-22, (H2S)=1.3×10-7, (H2S)=7.1×10-15。.
101 mg胰岛素溶于 10.0mL 水,该溶液在25.0℃时的渗透压是 4.34kPa,计算胰岛素的摩尔质量和该溶液的蒸气压下降Δp(已知25.0℃水的饱和蒸气压为3.17kPa)。
则,0.01+ S / cθ≈0.01,S / cθ= Ksp/0.01=8.5×10-15mol?L-1
2.将等体积的0.004 mol·L-1AgNO3溶液和0.004 mol·L-1的K2CrO4溶液混合,有无砖红色的Ag2CrO4沉淀析出?已知 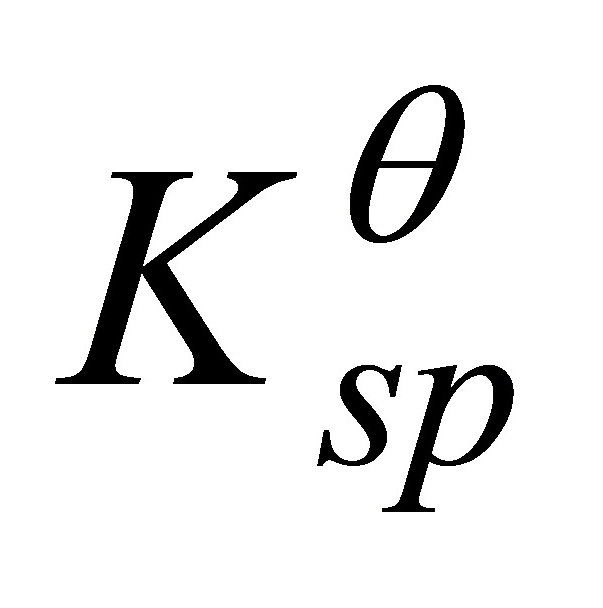 (Ag2CrO4)=1.1×10-12。
(Ag2CrO4)=1.1×10-12。
有砖红色沉淀析出。
3.1L溶液中含有4molNH4Cl和0.2molNH3,试计算:(1)溶液的[OH-]和pH;(2)在此条件下若有Fe(OH)2沉淀析出,溶液中Fe2+的最低浓度为多少?已知 (Fe(OH)2)=4.9×10-17。
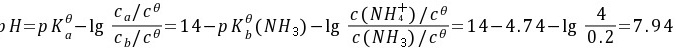 解:(1)
解:(1)
(2) 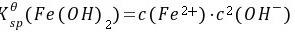
4.在0.1mol·L-1ZnCl2溶液中通入H2S气体至饱和,如果加入盐酸以控制溶液的pH,试计算开始析出ZnS沉淀和Zn2+沉淀完全时溶液的pH。已知
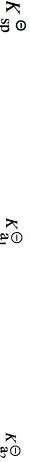 (ZnS)=2.5×10-22, (H2S)=1.3×10-7, (H2S)=7.1×10-15。
(ZnS)=2.5×10-22, (H2S)=1.3×10-7, (H2S)=7.1×10-15。
题目解答
答案
解: ZnS开始沉淀时S2-的浓度为
pH=0.72
Zn2+完全沉淀时S2-的浓度为
pH=0.72
5. 某溶液中含有Ca2+和Ba2+,浓度均为0.10mol·L-1,向溶液中滴加Na2SO4溶液,开始出现沉淀时浓度应为多大?当CaSO4开始沉淀时,溶液中剩下的Ba2+浓度为多大?能否用此方法分离Ca2+和Ba2+?已知 (BaSO4)=1.1×101、, (CaSO4)=4.9×105、。
解:BaSO4开始沉淀时,溶液中c(SO42-)为:
CaSO4开始沉淀时,溶液中c(SO42-)为:
先沉淀的是BaSO4,此时c(SO42-)为1.08×109、 mol·L1、
当CaSO4开始沉淀时,溶液中的c(Ba2+)为:
故可用此法分离Ca2+和Ba2+。
.