题目
在含有10g氢气的气球内需要加入多少摩尔氩气,才能使气球停留在空气中(气球-|||-的质量等于相同体积的空气的质量)?假定混合气体是理想气体,气球本身的质量可忽略不-|||-计。已知空气的平均摩尔质量为 cdot mo(L)^-1

题目解答
答案
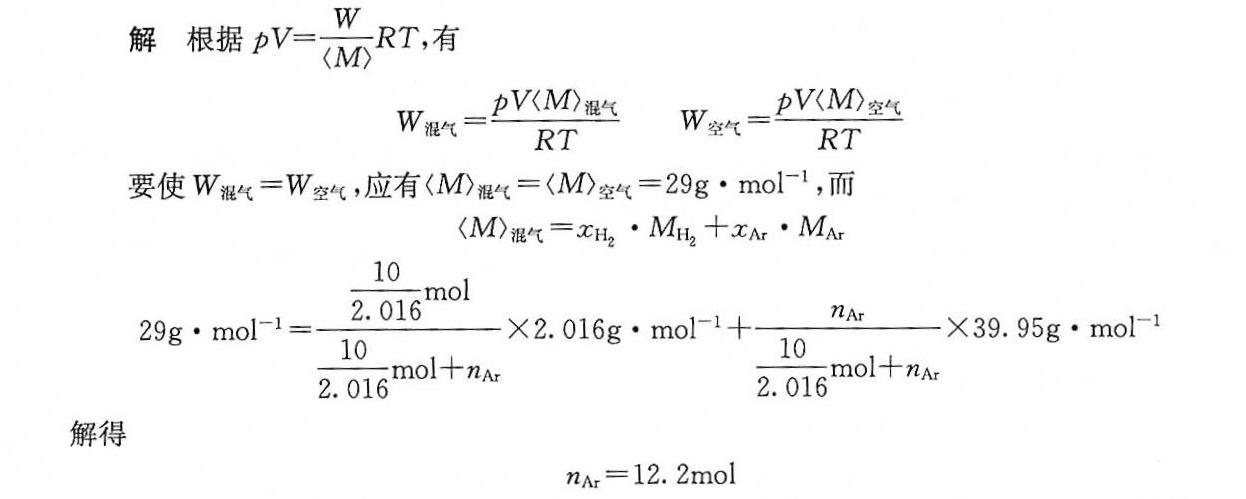
解析
步骤 1:确定氢气的摩尔数
氢气的摩尔质量为 $2g\cdot {mol}^{-1}$,因此10g氢气的摩尔数为:
$$
n_{H_2} = \frac{10g}{2g\cdot {mol}^{-1}} = 5mol
$$
步骤 2:设定氩气的摩尔数
设需要加入的氩气的摩尔数为 $n_{Ar}$。
步骤 3:计算混合气体的平均摩尔质量
混合气体的平均摩尔质量为:
$$
\langle M \rangle_{mix} = \frac{n_{H_2} \cdot M_{H_2} + n_{Ar} \cdot M_{Ar}}{n_{H_2} + n_{Ar}}
$$
其中,$M_{H_2} = 2g\cdot {mol}^{-1}$,$M_{Ar} = 40g\cdot {mol}^{-1}$。
步骤 4:使混合气体的平均摩尔质量等于空气的平均摩尔质量
为了使气球停留在空气中,混合气体的平均摩尔质量应等于空气的平均摩尔质量,即:
$$
\langle M \rangle_{mix} = 29g\cdot {mol}^{-1}
$$
步骤 5:解方程求解氩气的摩尔数
将步骤3中的表达式代入步骤4中的等式,得到:
$$
\frac{5mol \cdot 2g\cdot {mol}^{-1} + n_{Ar} \cdot 40g\cdot {mol}^{-1}}{5mol + n_{Ar}} = 29g\cdot {mol}^{-1}
$$
解这个方程,得到:
$$
10g + 40n_{Ar} = 29(5 + n_{Ar})
$$
$$
10g + 40n_{Ar} = 145g + 29n_{Ar}
$$
$$
11n_{Ar} = 135g
$$
$$
n_{Ar} = \frac{135g}{11g\cdot {mol}^{-1}} = 12.27mol
$$
氢气的摩尔质量为 $2g\cdot {mol}^{-1}$,因此10g氢气的摩尔数为:
$$
n_{H_2} = \frac{10g}{2g\cdot {mol}^{-1}} = 5mol
$$
步骤 2:设定氩气的摩尔数
设需要加入的氩气的摩尔数为 $n_{Ar}$。
步骤 3:计算混合气体的平均摩尔质量
混合气体的平均摩尔质量为:
$$
\langle M \rangle_{mix} = \frac{n_{H_2} \cdot M_{H_2} + n_{Ar} \cdot M_{Ar}}{n_{H_2} + n_{Ar}}
$$
其中,$M_{H_2} = 2g\cdot {mol}^{-1}$,$M_{Ar} = 40g\cdot {mol}^{-1}$。
步骤 4:使混合气体的平均摩尔质量等于空气的平均摩尔质量
为了使气球停留在空气中,混合气体的平均摩尔质量应等于空气的平均摩尔质量,即:
$$
\langle M \rangle_{mix} = 29g\cdot {mol}^{-1}
$$
步骤 5:解方程求解氩气的摩尔数
将步骤3中的表达式代入步骤4中的等式,得到:
$$
\frac{5mol \cdot 2g\cdot {mol}^{-1} + n_{Ar} \cdot 40g\cdot {mol}^{-1}}{5mol + n_{Ar}} = 29g\cdot {mol}^{-1}
$$
解这个方程,得到:
$$
10g + 40n_{Ar} = 29(5 + n_{Ar})
$$
$$
10g + 40n_{Ar} = 145g + 29n_{Ar}
$$
$$
11n_{Ar} = 135g
$$
$$
n_{Ar} = \frac{135g}{11g\cdot {mol}^{-1}} = 12.27mol
$$