题目
化学是一门以实验为基础的科学。根据如图回答问题。m n-|||-A B C D E F G(1)仪器a的名称是 ____ 。(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学反应方程式为 ____ ,若用F装置收集氧气,当观察到 ____ 的现象时再开始收集。(3)甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,应选用的发生装置是 ____ (填标号,下同),若用G装置收集时,则气体要从 ____ 端通入。(4)若用如图套管实验装置验证碳酸钠和碳酸氢钠的稳定性,其反应的化学方程式为 ____ 、 ____ ,试管B中装入的固体最好是 ____ (填化学式)。m n-|||-A B C D E F G(5)碳酸氢钠溶液与过量澄清石灰水反应的离子方程式为 ____ 。
化学是一门以实验为基础的科学。根据如图回答问题。
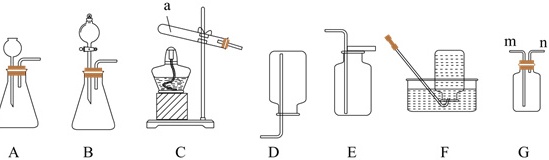
(1)仪器a的名称是 ____ 。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学反应方程式为 ____ ,若用F装置收集氧气,当观察到 ____ 的现象时再开始收集。
(3)甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,应选用的发生装置是 ____ (填标号,下同),若用G装置收集时,则气体要从 ____ 端通入。
(4)若用如图套管实验装置验证碳酸钠和碳酸氢钠的稳定性,其反应的化学方程式为 ____ 、 ____ ,试管B中装入的固体最好是 ____ (填化学式)。
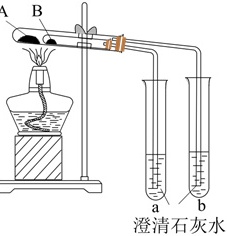
(5)碳酸氢钠溶液与过量澄清石灰水反应的离子方程式为 ____ 。

(1)仪器a的名称是 ____ 。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学反应方程式为 ____ ,若用F装置收集氧气,当观察到 ____ 的现象时再开始收集。
(3)甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,应选用的发生装置是 ____ (填标号,下同),若用G装置收集时,则气体要从 ____ 端通入。
(4)若用如图套管实验装置验证碳酸钠和碳酸氢钠的稳定性,其反应的化学方程式为 ____ 、 ____ ,试管B中装入的固体最好是 ____ (填化学式)。

(5)碳酸氢钠溶液与过量澄清石灰水反应的离子方程式为 ____ 。
题目解答
答案
(1)根据仪器的构造可知a为试管,
故答案为:试管;
(2)过氧化氢在二氧化锰作催化剂条件下分解生成氧气和水,反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O,用排水法收集氧气时,要等到导管口气泡稳定后即空气被排尽后收集,
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O;气泡均匀连续冒出;
(3)实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,为固体混合物加热制取气体,应选用向下倾斜试管加热,即采用C装置;若用排空气法收集甲烷,因其密度比空气小应采用向下排空气法,若用G装置收集则应短管进气长管出气,则气体要从n端通入,
故答案为:C;n;
(4)碳酸钠和碳酸氢钠加热时只有碳酸氢钠不稳定会发生分解生成碳酸钠、二氧化碳,反应为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,生成的二氧化碳气体进入澄清石灰水中反应生成碳酸钙沉淀,反应为:CO2+Ca(OH)2=CaCO3↓+H2O;碳酸热稳定性比碳酸氢钠强,应将其置于外管高温出,碳酸氢钠置于内管,如果仍能看到试管a无浑浊,试管b出现浑浊则能说明碳酸钠比碳酸氢钠稳定,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;NaHCO3;
(5)碳酸氢钠溶液与过量澄清石灰水反应生成碳酸钙沉淀和NaOH,反应的离子方程式为${HCO}_{3}^{-}$+OH-+Ca2+=CaCO3↓+H2O,
故答案为:${HCO}_{3}^{-}$+OH-+Ca2+=CaCO3↓+H2O。
故答案为:试管;
(2)过氧化氢在二氧化锰作催化剂条件下分解生成氧气和水,反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O,用排水法收集氧气时,要等到导管口气泡稳定后即空气被排尽后收集,
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O;气泡均匀连续冒出;
(3)实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,为固体混合物加热制取气体,应选用向下倾斜试管加热,即采用C装置;若用排空气法收集甲烷,因其密度比空气小应采用向下排空气法,若用G装置收集则应短管进气长管出气,则气体要从n端通入,
故答案为:C;n;
(4)碳酸钠和碳酸氢钠加热时只有碳酸氢钠不稳定会发生分解生成碳酸钠、二氧化碳,反应为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,生成的二氧化碳气体进入澄清石灰水中反应生成碳酸钙沉淀,反应为:CO2+Ca(OH)2=CaCO3↓+H2O;碳酸热稳定性比碳酸氢钠强,应将其置于外管高温出,碳酸氢钠置于内管,如果仍能看到试管a无浑浊,试管b出现浑浊则能说明碳酸钠比碳酸氢钠稳定,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;NaHCO3;
(5)碳酸氢钠溶液与过量澄清石灰水反应生成碳酸钙沉淀和NaOH,反应的离子方程式为${HCO}_{3}^{-}$+OH-+Ca2+=CaCO3↓+H2O,
故答案为:${HCO}_{3}^{-}$+OH-+Ca2+=CaCO3↓+H2O。
解析
- 仪器识别:根据常见实验仪器的结构特征判断名称。
- 反应方程式与收集时机:掌握过氧化氢制氧气的化学反应式,理解排水法收集氧气的正确时机。
- 发生装置与收集方式:根据反应条件(固体加热)选择发生装置,根据气体密度与溶解性选择排空气法的进气方向。
- 物质稳定性验证:通过分解产物判断物质稳定性,明确实验设计中固体位置与现象对应关系。
- 离子方程式书写:注意反应物的过量关系,正确表达产物的沉淀和离子形式。
第(1)题
仪器结构分析
仪器a为直形玻璃管,两端开口,底部封闭,符合试管的特征。
第(2)题
反应方程式
过氧化氢在二氧化锰催化下分解:
$2\text{H}_2\text{O}_2 \xrightarrow{\text{MnO}_2} 2\text{H}_2\text{O} + \text{O}_2↑$
收集时机
排水法收集氧气时,需待气泡均匀连续冒出,避免混入空气。
第(3)题
发生装置选择
反应需加热固体混合物,故选固体加热型装置C。
排空气法进气
甲烷密度比空气小,向下排空气法需从n端通入(短管进气)。
第(4)题
反应方程式
- 碳酸氢钠分解:
$2\text{NaHCO}_3 \xrightarrow{\Delta} \text{Na}_2\text{CO}_3 + \text{H}_2\text{O} + \text{CO}_2↑$ - 二氧化碳与石灰水反应:
$\text{CO}_2 + \text{Ca(OH)}_2 \rightarrow \text{CaCO}_3↓ + \text{H}_2\text{O}$
固体位置设计
为验证稳定性,NaHCO₃应置于外管(高温侧),Na₂CO₃置于内管。
第(5)题
离子方程式
过量石灰水与碳酸氢钠反应生成CaCO₃沉淀和NaOH:
$\text{HCO}_3^- + \text{OH}^- + \text{Ca}^{2+} \rightarrow \text{CaCO}_3↓ + \text{H}_2\text{O}$