(10分)(2015春•山东校级期中)氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 激光-|||-TiO2 2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:(1)分解海水时,二氧化钛作 催化剂 .生成的氢气用于燃料电池时, 化学 能转变为 电 能.分解海水的反应属于 吸热 反应(填“放热”或“吸热”).(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应如下:A极:2H2+2O2﹣﹣4e﹣═2H2O B极:O2+4e﹣═2O2﹣则A极是电池的 负 极;电子从该极 流出 (填“流入”或“流出”).(3)(a)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片上发生的电极反应 Zn﹣2e﹣=Zn2+; 银片上发生的电极反应 2H++2e﹣=H2↑(b)若以上电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:①产生氢气的体积(标准状况) 4.48 L;②消耗的锌的质量 13 g.(已知NA=6.02×1023 mol﹣1,)考点:原电池和电解池的工作原理.版权所有专题:电化学专题.分析:(1)利用太阳能分解海水是将太阳能转化为化学能;氢氧燃料电池属于原电池,是将化学能转化为电能,断裂化学键需要吸收能量,形成化学键放出能量;(2)原电池中,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流出;(3)(a)锌片、银片、稀硫酸构成原电池,活泼金属锌作负极,负极上失电子发生氧化反应,银作正极,正极上得电子发生还原反应,据此写出电极反应式;(b)根据得失电子守恒计算生成氢气的体积.解答:解:(1)科学家利用太阳能使海水分解,所以是太阳能转变为化学能,该反应中二氧化钛作催化剂;生成的氢气用于燃料电池时是把化学能转变为电能,水分解时,断裂的化学键是H﹣O键;电解水是吸热反应,故答案为:催化剂、化学、电、吸热;(2)A极是失去电子发生氧化反应的电极,所以A极是负极,正极上得电子发生还原反应,所以电子从负极流出,故答案为:负;流出;(3)(a)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn﹣2e﹣=Zn2+;银作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e﹣=H2↑,故答案为:Zn﹣2e﹣=Zn2+;2H++2e﹣=H2↑;(b)该原电池中,负极上锌失电子变成锌离子进入溶液,导致质量减少,正极上金属不参加反应,所以该装置中减少的质量是锌的质量,根据转移电子相等知,生成氢气的物质的量和锌的物质的量相等,所以生成气体的体积=×22.4L/mol=4.48L,所以参加反应锌的质量为g=13g,故答案为:4.48L,13g.点评:本题考查原电池反应的原理,负极发生氧化反应,正极发生还原反应,在得失电子守恒的情况下根据电极反应进行计算,难度不大.
(10分)(2015春•山东校级期中)氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 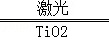 2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
(1)分解海水时,二氧化钛作 催化剂 .生成的氢气用于燃料电池时, 化学 能转变为 电 能.分解海水的反应属于 吸热 反应(填“放热”或“吸热”).
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应如下:A极:2H2+2O2﹣﹣4e﹣═2H2O B极:O2+4e﹣═2O2﹣则A极是电池的 负 极;电子从该极 流出 (填“流入”或“流出”).
(3)(a)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片上发生的电极反应 Zn﹣2e﹣=Zn2+; 银片上发生的电极反应 2H++2e﹣=H2↑
(b)若以上电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:①产生氢气的体积(标准状况) 4.48 L;②消耗的锌的质量 13 g.(已知NA=6.02×1023 mol﹣1,)
考点:
原电池和电解池的工作原理.版权所有
专题:
电化学专题.
分析:
(1)利用太阳能分解海水是将太阳能转化为化学能;氢氧燃料电池属于原电池,是将化学能转化为电能,断裂化学键需要吸收能量,形成化学键放出能量;
(2)原电池中,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流出;
(3)(a)锌片、银片、稀硫酸构成原电池,活泼金属锌作负极,负极上失电子发生氧化反应,银作正极,正极上得电子发生还原反应,据此写出电极反应式;
(b)根据得失电子守恒计算生成氢气的体积.
解答:
解:(1)科学家利用太阳能使海水分解,所以是太阳能转变为化学能,该反应中二氧化钛作催化剂;生成的氢气用于燃料电池时是把化学能转变为电能,水分解时,断裂的化学键是H﹣O键;电解水是吸热反应,
故答案为:催化剂、化学、电、吸热;
(2)A极是失去电子发生氧化反应的电极,所以A极是负极,正极上得电子发生还原反应,所以电子从负极流出,故答案为:负;流出;
(3)(a)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn﹣2e﹣=Zn2+;银作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e﹣=H2↑,
故答案为:Zn﹣2e﹣=Zn2+;2H++2e﹣=H2↑;
(b)该原电池中,负极上锌失电子变成锌离子进入溶液,导致质量减少,正极上金属不参加反应,所以该装置中减少的质量是锌的质量,根据转移电子相等知,生成氢气的物质的量和锌的物质的量相等,所以生成气体的体积=×22.4L/mol=4.48L,所以参加反应锌的质量为
g=13g,故答案为:4.48L,13g.
点评:
本题考查原电池反应的原理,负极发生氧化反应,正极发生还原反应,在得失电子守恒的情况下根据电极反应进行计算,难度不大.
题目解答
答案
解答:
解:(1)科学家利用太阳能使海水分解,所以是太阳能转变为化学能,该反应中二氧化钛作催化剂;生成的氢气用于燃料电池时是把化学能转变为电能,水分解时,断裂的化学键是H﹣O键;电解水是吸热反应,
故答案为:催化剂、化学、电、吸热;
(2)A极是失去电子发生氧化反应的电极,所以A极是负极,正极上得电子发生还原反应,所以电子从负极流出,故答案为:负;流出;
(3)(a)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn﹣2e﹣=Zn2+;银作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e﹣=H2↑,
故答案为:Zn﹣2e﹣=Zn2+;2H++2e﹣=H2↑;
(b)该原电池中,负极上锌失电子变成锌离子进入溶液,导致质量减少,正极上金属不参加反应,所以该装置中减少的质量是锌的质量,根据转移电子相等知,生成氢气的物质的量和锌的物质的量相等,所以生成气体的体积=×22.4L/mol=4.48L,所以参加反应锌的质量为
g=13g,故答案为:4.48L,13g.