题目
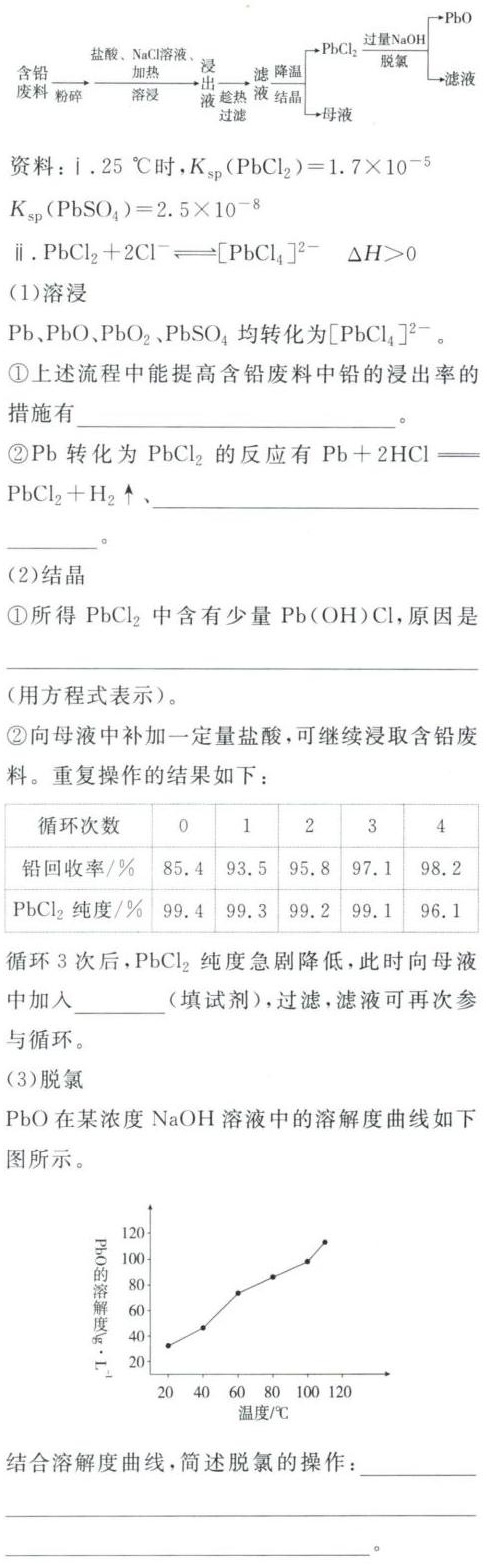
(2023·北京市朝阳区高三期末质量检测)以废-|||-旧铅酸蓄电池中的含铅废料(Pb、PbO、PbO 2、-|||-PbSO4等)为原料制备PbO,实现铅的再生利-|||-用。流程示意图如下:(2023·北京市朝阳区高三期末质量检测)以废-|||-旧铅酸蓄电池中的含铅废料(Pb、PbO、PbO 2、-|||-PbSO4等)为原料制备PbO,实现铅的再生利-|||-用。流程示意图如下:(2023·北京市朝阳区高三期末质量检测)以废-|||-旧铅酸蓄电池中的含铅废料(Pb、PbO、PbO 2、-|||-PbSO4等)为原料制备PbO,实现铅的再生利-|||-用。流程示意图如下:


题目解答
答案

解析
步骤 1:提高含铅废料中铅的浸出率的措施
含铅废料中铅的浸出率可以通过粉碎、加热、加入NaCl增大 $c({Cl}^{-})$ 来提高。
步骤 2:Pb转化为PbCl2的反应
Pb转化为PbCl2的反应除了 Pb+2HCl= $Pb{Cl}_{2}+{H}_{2}\uparrow $ 外,还有 Pb+PbO2+4HCl=2PbCl2+2H2O。
步骤 3:所得PbCl2中含有少量Pb(OH)Cl的原因
所得PbCl2中含有少量Pb(OH)Cl,原因是 ${[ Pb{Cl}_{4}] }^{2-}+{H}_{2}O\rightleftharpoons Pb(OH)Cl+{H}^{+}+3{Cl}^{-}$。
步骤 4:循环3次后,PbCl2纯度急剧降低,向母液中加入的试剂
循环3次后,PbCl2纯度急剧降低,此时向母液中加入CaCl2 (或BaCl2),过滤,滤液可再次参与循环。
步骤 5:脱氯的操作
脱氯的操作为向PbCl2中加入一定量NaOH溶液,加热至固体完全溶解后,冷却结晶,过滤得到PbO固体。
步骤 6:计算废料中铅的质量分数
将ag含铅废料与足量盐酸、NaCl溶液充分反应,得到100 mL溶液。取10mL溶液加水稀释,再加几滴二甲酚橙作指示剂,用0.01 mol· ${L}^{-1}$ 的乙二胺四乙酸二钠盐(用Na2H2 Y表示)进行滴定,滴定终点时消耗Na2H2Y溶液VmL。计算废料中铅的质量分数为 $\dfrac {2.07V}{a}\% $。
含铅废料中铅的浸出率可以通过粉碎、加热、加入NaCl增大 $c({Cl}^{-})$ 来提高。
步骤 2:Pb转化为PbCl2的反应
Pb转化为PbCl2的反应除了 Pb+2HCl= $Pb{Cl}_{2}+{H}_{2}\uparrow $ 外,还有 Pb+PbO2+4HCl=2PbCl2+2H2O。
步骤 3:所得PbCl2中含有少量Pb(OH)Cl的原因
所得PbCl2中含有少量Pb(OH)Cl,原因是 ${[ Pb{Cl}_{4}] }^{2-}+{H}_{2}O\rightleftharpoons Pb(OH)Cl+{H}^{+}+3{Cl}^{-}$。
步骤 4:循环3次后,PbCl2纯度急剧降低,向母液中加入的试剂
循环3次后,PbCl2纯度急剧降低,此时向母液中加入CaCl2 (或BaCl2),过滤,滤液可再次参与循环。
步骤 5:脱氯的操作
脱氯的操作为向PbCl2中加入一定量NaOH溶液,加热至固体完全溶解后,冷却结晶,过滤得到PbO固体。
步骤 6:计算废料中铅的质量分数
将ag含铅废料与足量盐酸、NaCl溶液充分反应,得到100 mL溶液。取10mL溶液加水稀释,再加几滴二甲酚橙作指示剂,用0.01 mol· ${L}^{-1}$ 的乙二胺四乙酸二钠盐(用Na2H2 Y表示)进行滴定,滴定终点时消耗Na2H2Y溶液VmL。计算废料中铅的质量分数为 $\dfrac {2.07V}{a}\% $。