题目
气相反应 (g)+(Cl)_(2)(g)arrow CO(Cl)_(2)(g) 是一个二级反应,当CO(g )和Cl2(g)-|||-的初始压力均为10 kPa时,在25℃时反应的半衰期为1h,在35 ℃时反应的半衰期为-|||-0.5h。①计算25℃和35 ℃时反应的速率常数。②计算该反应的阿累尼乌斯活化能Ea和-|||-指前因子k0。

题目解答
答案
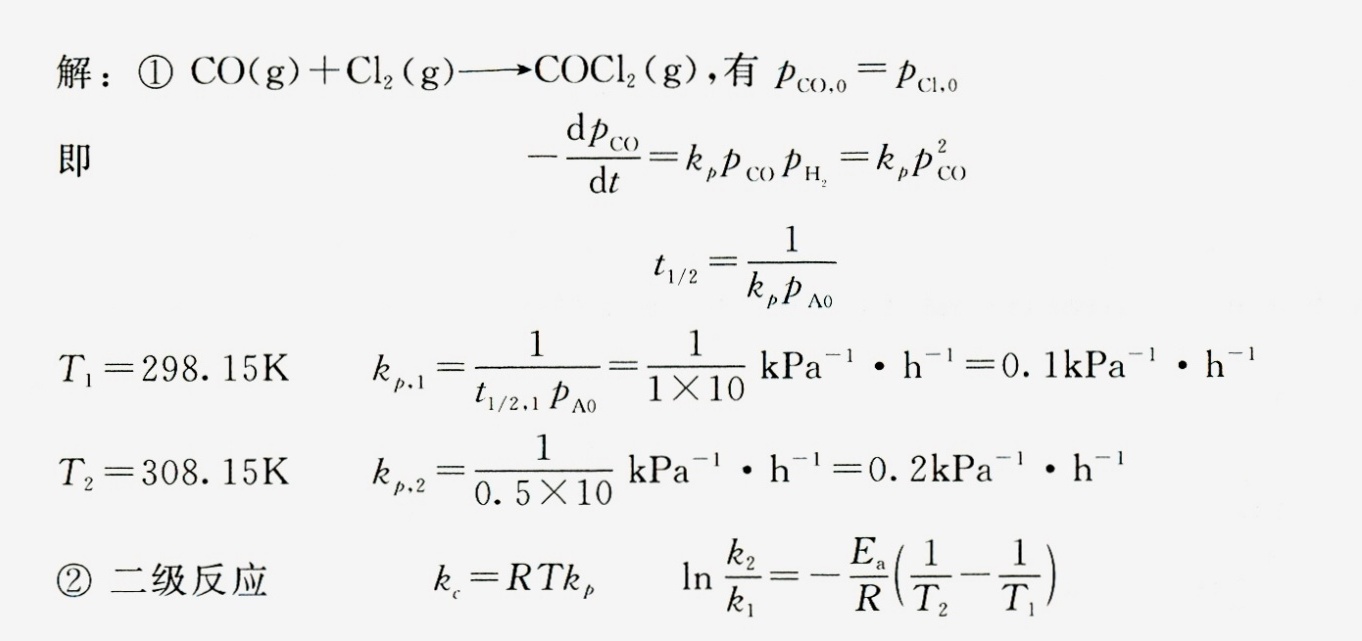
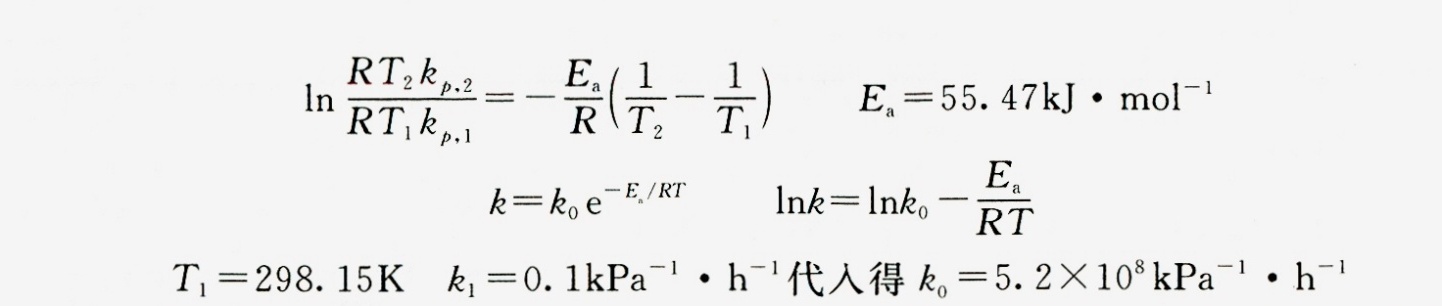
解析
步骤 1:确定反应的半衰期公式
对于二级反应,半衰期公式为 ${t}_{1/2}=\dfrac {1}{{k}_{P}{P}_{AO}}$,其中 ${k}_{P}$ 是速率常数,${P}_{AO}$ 是初始压力。
步骤 2:计算25℃时的速率常数
在25℃时,${t}_{1/2}=1h$,${P}_{AO}=10kPa$,代入公式 ${k}_{P}=\dfrac {1}{{t}_{1/2}{P}_{AO}}$,得到 ${k}_{P}=0.1kPa^{-1}\cdot h^{-1}$。
步骤 3:计算35℃时的速率常数
在35℃时,${t}_{1/2}=0.5h$,${P}_{AO}=10kPa$,代入公式 ${k}_{P}=\dfrac {1}{{t}_{1/2}{P}_{AO}}$,得到 ${k}_{P}=0.2kPa^{-1}\cdot h^{-1}$。
步骤 4:计算阿累尼乌斯活化能Ea
利用阿累尼乌斯方程 $\ln \dfrac {{k}_{2}}{{k}_{1}}=-\dfrac {{E}_{a}}{R}(\dfrac {1}{{T}_{2}}-\dfrac {1}{{T}_{1}})$,其中 ${k}_{1}$ 和 ${k}_{2}$ 分别是两个温度下的速率常数,${T}_{1}$ 和 ${T}_{2}$ 分别是两个温度,R 是气体常数。代入 ${k}_{1}=0.1kPa^{-1}\cdot h^{-1}$,${k}_{2}=0.2kPa^{-1}\cdot h^{-1}$,${T}_{1}=298.15K$,${T}_{2}=308.15K$,得到 ${E}_{a}=55.47kJ\cdot mol^{-1}$。
步骤 5:计算指前因子k0
利用阿累尼乌斯方程 $k={k}_{0}{e}^{-{E}_{a}/RT}$,代入 ${k}_{1}=0.1kPa^{-1}\cdot h^{-1}$,${T}_{1}=298.15K$,${E}_{a}=55.47kJ\cdot mol^{-1}$,得到 ${k}_{0}=5.2\times {10}^{8}kPa^{-1}\cdot h^{-1}$。
对于二级反应,半衰期公式为 ${t}_{1/2}=\dfrac {1}{{k}_{P}{P}_{AO}}$,其中 ${k}_{P}$ 是速率常数,${P}_{AO}$ 是初始压力。
步骤 2:计算25℃时的速率常数
在25℃时,${t}_{1/2}=1h$,${P}_{AO}=10kPa$,代入公式 ${k}_{P}=\dfrac {1}{{t}_{1/2}{P}_{AO}}$,得到 ${k}_{P}=0.1kPa^{-1}\cdot h^{-1}$。
步骤 3:计算35℃时的速率常数
在35℃时,${t}_{1/2}=0.5h$,${P}_{AO}=10kPa$,代入公式 ${k}_{P}=\dfrac {1}{{t}_{1/2}{P}_{AO}}$,得到 ${k}_{P}=0.2kPa^{-1}\cdot h^{-1}$。
步骤 4:计算阿累尼乌斯活化能Ea
利用阿累尼乌斯方程 $\ln \dfrac {{k}_{2}}{{k}_{1}}=-\dfrac {{E}_{a}}{R}(\dfrac {1}{{T}_{2}}-\dfrac {1}{{T}_{1}})$,其中 ${k}_{1}$ 和 ${k}_{2}$ 分别是两个温度下的速率常数,${T}_{1}$ 和 ${T}_{2}$ 分别是两个温度,R 是气体常数。代入 ${k}_{1}=0.1kPa^{-1}\cdot h^{-1}$,${k}_{2}=0.2kPa^{-1}\cdot h^{-1}$,${T}_{1}=298.15K$,${T}_{2}=308.15K$,得到 ${E}_{a}=55.47kJ\cdot mol^{-1}$。
步骤 5:计算指前因子k0
利用阿累尼乌斯方程 $k={k}_{0}{e}^{-{E}_{a}/RT}$,代入 ${k}_{1}=0.1kPa^{-1}\cdot h^{-1}$,${T}_{1}=298.15K$,${E}_{a}=55.47kJ\cdot mol^{-1}$,得到 ${k}_{0}=5.2\times {10}^{8}kPa^{-1}\cdot h^{-1}$。