题目
计算题-|||-由玻璃电极和饱和甘汞电极组成电池,在25℃时测得pH为8.0的标准缓冲溶液的电池-|||-电动势为0.340V,测得未知溶液电动势为0.428V,计算该未知溶液的pH。

题目解答
答案
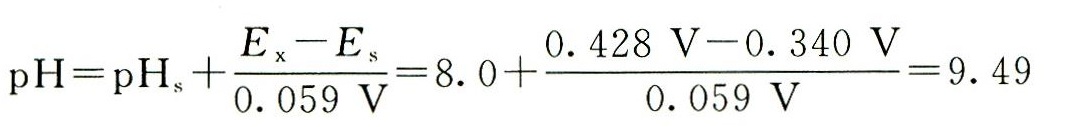
解析
本题考查的是利用玻璃电极和饱和甘汞电极组成的电池电动势来计算溶液的pH。解题思路如下:
- 首先明确在一定温度下,玻璃电极的电位与溶液的pH之间存在线性关系。
- 对于已知pH的标准缓冲溶液和未知溶液,分别测量其电池电动势$E_1$和$E_2$。
- 根据线性关系,未知溶液的pH$pH_2$可以通过已知溶液的pH$pH_1$以及两个电动势的差值来计算。
- 具体的计算公式为$pH_2 = pH_1+\frac{E_2 - E_1}{0.059}$,其中$0.059$是在$25^{\circ}C$时的能斯特常数。
- 下面进行计算:
已知$pH_1 = 8.0$,$E_1 = 0.340V$,$E_2 = 0.428V$。
将这些值代入公式$pH_2 = pH_1+\frac{E_2 - E_1}{0.059}$可得:
$pH_2 = 8.0+\frac{0.428 - 0.340}{0.059}$
先计算分子$0.428 - 0.340 = 0.088$。
再计算$\frac{0.088}{0.059}\approx1.45$。
最后$pH_2 = 8.0 + 1.45 = 9.45$。