题目
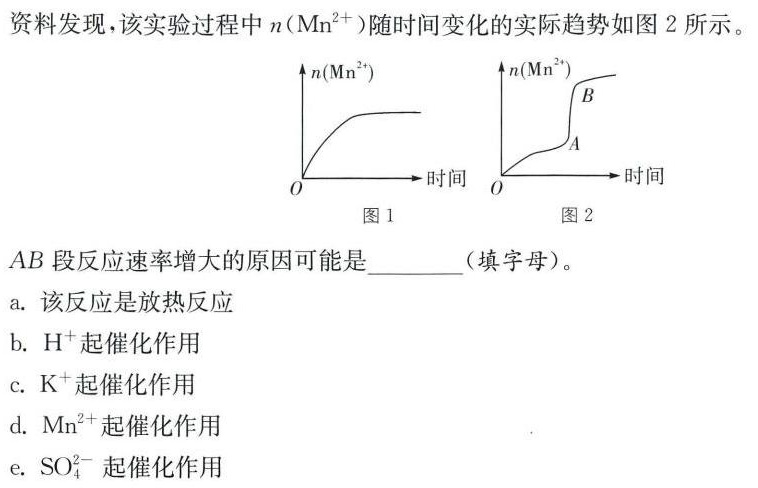
13分)(2023·吉林长春东北师范大学附属中学高一期中)合成氨的反应对人类解决粮食问题贡献巨大。合-|||-成氨反应的化学方程式为 _(2)(g)+3(H)_(2)(g)leftharpoons 2N(H)_(3)(g) 回答下列问题:-|||-(1)已知断开1 mol化学键所吸收的能量如下: -H436KJ -H391KJ equiv N946KJ 则-|||-_(2)(g)+3(H)_(2)(g)leftharpoons 2N(H)_(3)(g) 反应中生成17g NH3 __ (填"吸收"或"放出") __-|||-kJ热量。-|||-(2)恒温下,将6 molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,-|||-当反应进行到5s时,有0.1mol NH3生成。-|||-① 资料发现,该实验过程中 ((Mn)^2+) 随时间变化的实际趋势如图2所示。-|||-n(Mn^(2+)) n(Mn^(2+))-|||-B-|||-A-|||-0 时间 0 时间-|||-图1 图2-|||-AB段反应速率增大的原因可能是 __ (填字母)。-|||-a.该反应是放热反应-|||-b. ^+ 起催化作用-|||-c. ^+ 起催化作用-|||-d. ^2+ 起催化作用-|||-e. (S{O)_(4)}^2- 起催化作用sim 5s 内用H2表示该反应的平均反应速率 ((H)_(2))= __ cdot (L)^-1cdot (min)^-1-|||-②再经一段时间后反应达到平衡,此时混合气体总物质的量为13 mol,则平衡时NH3的物质-|||-的量为 __ mol。-|||-③下列可以说明该反应达到平衡状态的是 __ (填字母)。-|||-A. ((N)_(2)):c(N(H)_(3))=1:2-|||-B. (v)_(正)((H)_(2))=2vi(N(H)_(3))-|||-C.容器内气体的密度不再变化-|||-D.混合气体的平均摩尔质量不再变化-|||-E.单位时间内断开 3molH-H 键的同时,断开 6molN-H 键-|||-(3)KMnO4是实验室中常用的一种试剂。回答下列问题:-|||-在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4)溶液,振荡,溶液紫色褪去,同时产生能使-|||-燃着的木条熄灭的气体,发生反应的离子方程式为 __-|||-__ 若将该反应设计成原电池,则正极反应式为 __ 。-|||-(4)为了探究外界条件对化学反应速率的影响,设计如表方案:-|||-0.1mol/L 0.5 mol/L 0.1 mol/L 水浴温 蒸馏水 褪色时-|||-实验-|||-KMnO4/mL 2C2O4/mL 2SO4/mL 度/℃ /mL 间/min-|||-I 5.0 15.0 5.0 35 0 t1-|||-Ⅱ 5.0 10.0 5.0 35 5.0 t2-|||-Ⅲ 5.0 15.0 3.0 35 v 3-|||-① V= __ o-|||-②利用实验Ⅲ中数据计算,用H2C2 O4的浓度变化表示的反应速率为 ((H)_(2)(C)_(2)(O)_(4))=-|||-__ (用含t3的最简分数表示 cdot (L)^-1cdot (min)^-1-|||-③该小组根据经验绘制了 ((Mn)^2+) 随时间变化的趋势如图1所示,但有同学查阅已有实验13分)(2023·吉林长春东北师范大学附属中学高一期中)合成氨的反应对人类解决粮食问题贡献巨大。合-|||-成氨反应的化学方程式为 _(2)(g)+3(H)_(2)(g)leftharpoons 2N(H)_(3)(g) 回答下列问题:-|||-(1)已知断开1 mol化学键所吸收的能量如下: -H436KJ -H391KJ equiv N946KJ 则-|||-_(2)(g)+3(H)_(2)(g)leftharpoons 2N(H)_(3)(g) 反应中生成17g NH3 __ (填"吸收"或"放出") __-|||-kJ热量。-|||-(2)恒温下,将6 molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,-|||-当反应进行到5s时,有0.1mol NH3生成。-|||-① 资料发现,该实验过程中 ((Mn)^2+) 随时间变化的实际趋势如图2所示。-|||-n(Mn^(2+)) n(Mn^(2+))-|||-B-|||-A-|||-0 时间 0 时间-|||-图1 图2-|||-AB段反应速率增大的原因可能是 __ (填字母)。-|||-a.该反应是放热反应-|||-b. ^+ 起催化作用-|||-c. ^+ 起催化作用-|||-d. ^2+ 起催化作用-|||-e. (S{O)_(4)}^2- 起催化作用sim 5s 内用H2表示该反应的平均反应速率 ((H)_(2))= __ cdot (L)^-1cdot (min)^-1-|||-②再经一段时间后反应达到平衡,此时混合气体总物质的量为13 mol,则平衡时NH3的物质-|||-的量为 __ mol。-|||-③下列可以说明该反应达到平衡状态的是 __ (填字母)。-|||-A. ((N)_(2)):c(N(H)_(3))=1:2-|||-B. (v)_(正)((H)_(2))=2vi(N(H)_(3))-|||-C.容器内气体的密度不再变化-|||-D.混合气体的平均摩尔质量不再变化-|||-E.单位时间内断开 3molH-H 键的同时,断开 6molN-H 键-|||-(3)KMnO4是实验室中常用的一种试剂。回答下列问题:-|||-在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4)溶液,振荡,溶液紫色褪去,同时产生能使-|||-燃着的木条熄灭的气体,发生反应的离子方程式为 __-|||-__ 若将该反应设计成原电池,则正极反应式为 __ 。-|||-(4)为了探究外界条件对化学反应速率的影响,设计如表方案:-|||-0.1mol/L 0.5 mol/L 0.1 mol/L 水浴温 蒸馏水 褪色时-|||-实验-|||-KMnO4/mL 2C2O4/mL 2SO4/mL 度/℃ /mL 间/min-|||-I 5.0 15.0 5.0 35 0 t1-|||-Ⅱ 5.0 10.0 5.0 35 5.0 t2-|||-Ⅲ 5.0 15.0 3.0 35 v 3-|||-① V= __ o-|||-②利用实验Ⅲ中数据计算,用H2C2 O4的浓度变化表示的反应速率为 ((H)_(2)(C)_(2)(O)_(4))=-|||-__ (用含t3的最简分数表示 cdot (L)^-1cdot (min)^-1-|||-③该小组根据经验绘制了 ((Mn)^2+) 随时间变化的趋势如图1所示,但有同学查阅已有实验

题目解答
答案
解析
步骤 1:计算生成17gNH3的物质的量
17gNH3的物质的量为 $\frac{17g}{17g/mol}=1mol$。
步骤 2:根据化学方程式计算放出的热量
根据化学方程式,生成2molNH3放出92kJ热量,所以生成1molNH3放出46kJ热量。
【答案】
放出 46
(2)恒温下,将6 molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,当反应进行到5s时,有0.1 mol NH3生成。
【解析】
步骤 1:计算0~5s内用H2表示的平均反应速率
根据化学方程式,生成0.1molNH3需要消耗0.15molH2,所以 $v({H}_{2})=\frac{0.15mol}{2L\times 5s}=\frac{0.15}{10}mol\cdot {L}^{-1}\cdot {s}^{-1}=\frac{0.15}{10}\times 60mol\cdot {L}^{-1}\cdot {min}^{-1}=0.9mol\cdot {L}^{-1}\cdot {min}^{-1}$。
步骤 2:计算平衡时NH3的物质的量
根据化学方程式,生成2molNH3需要消耗2molN2和6molH2,所以生成10molNH3需要消耗10molN2和30molH2,所以平衡时NH3的物质的量为10mol。
步骤 3:判断平衡状态
A. $c({N}_{2}):c(N{H}_{3})=1:2$,不能说明反应达到平衡状态。
B. $3v-({H}_{2})=2vi(N{H}_{3})$,不能说明反应达到平衡状态。
C. 容器内气体的密度不再变化,不能说明反应达到平衡状态。
D. 混合气体的平均摩尔质量不再变化,说明反应达到平衡状态。
E. 单位时间内断开 3molH-H 键的同时,断开 6molN-H 键,说明反应达到平衡状态。
【答案】
①0.9 ②10 ③DE
(3)在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4 )溶液,振荡,溶液紫色褪去,同时产生能使燃着的木条熄灭的气体,发生反应的离子方程式为 $2{Mn{O}_{4}}^{-}+5{H}_{2}{C}_{2}{O}_{4}+6{H}^{+}=\!=\!= 2{Mn}^{2+}+10C{O}_{2}\uparrow +8{H}_{2}O$,若将该反应设计成原电池,则正极反应式为 ${Mn{O}_{4}}^{-}+5{e}^{-}+8{H}^{+}=\!=\!= {Mn}^{2+}+4{H}_{2}O$。
17gNH3的物质的量为 $\frac{17g}{17g/mol}=1mol$。
步骤 2:根据化学方程式计算放出的热量
根据化学方程式,生成2molNH3放出92kJ热量,所以生成1molNH3放出46kJ热量。
【答案】
放出 46
(2)恒温下,将6 molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,当反应进行到5s时,有0.1 mol NH3生成。
【解析】
步骤 1:计算0~5s内用H2表示的平均反应速率
根据化学方程式,生成0.1molNH3需要消耗0.15molH2,所以 $v({H}_{2})=\frac{0.15mol}{2L\times 5s}=\frac{0.15}{10}mol\cdot {L}^{-1}\cdot {s}^{-1}=\frac{0.15}{10}\times 60mol\cdot {L}^{-1}\cdot {min}^{-1}=0.9mol\cdot {L}^{-1}\cdot {min}^{-1}$。
步骤 2:计算平衡时NH3的物质的量
根据化学方程式,生成2molNH3需要消耗2molN2和6molH2,所以生成10molNH3需要消耗10molN2和30molH2,所以平衡时NH3的物质的量为10mol。
步骤 3:判断平衡状态
A. $c({N}_{2}):c(N{H}_{3})=1:2$,不能说明反应达到平衡状态。
B. $3v-({H}_{2})=2vi(N{H}_{3})$,不能说明反应达到平衡状态。
C. 容器内气体的密度不再变化,不能说明反应达到平衡状态。
D. 混合气体的平均摩尔质量不再变化,说明反应达到平衡状态。
E. 单位时间内断开 3molH-H 键的同时,断开 6molN-H 键,说明反应达到平衡状态。
【答案】
①0.9 ②10 ③DE
(3)在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4 )溶液,振荡,溶液紫色褪去,同时产生能使燃着的木条熄灭的气体,发生反应的离子方程式为 $2{Mn{O}_{4}}^{-}+5{H}_{2}{C}_{2}{O}_{4}+6{H}^{+}=\!=\!= 2{Mn}^{2+}+10C{O}_{2}\uparrow +8{H}_{2}O$,若将该反应设计成原电池,则正极反应式为 ${Mn{O}_{4}}^{-}+5{e}^{-}+8{H}^{+}=\!=\!= {Mn}^{2+}+4{H}_{2}O$。