题目
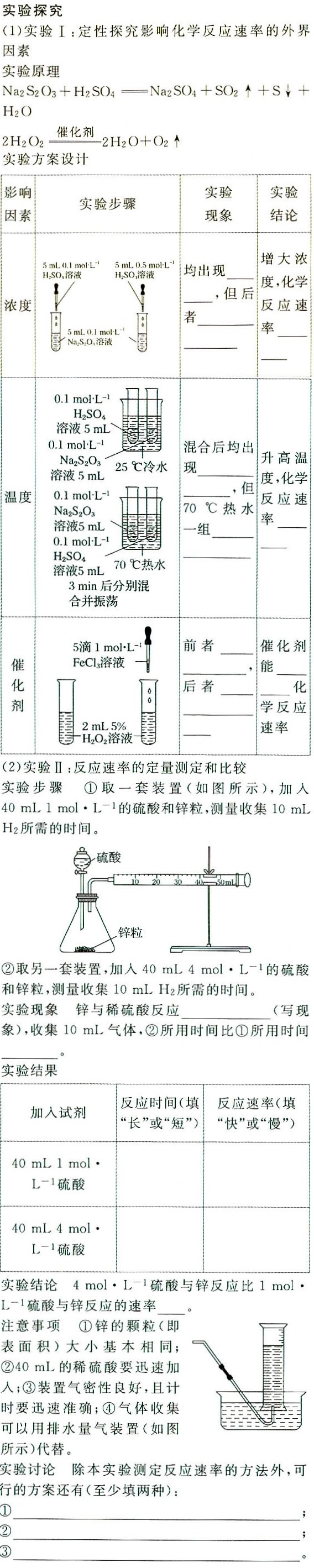
(1)实验I:定性探究影响化学反应速率的外界-|||-因素-|||-实验原理-|||-_(2)(S)_(2)(O)_(3)+(H)_(2)S(O)_(4)=(Na)_(2)S(O)_(4)+S(O)_(2)uparrow +Sdownarrow +-|||-H2O-|||-2H2O2催化剂 =2H2O+O2↑-|||-实验方案设计-|||-影响 实验 实验-|||-因素 实验步骤 现象 结论-|||-5mL0.1mol·L^(-1) 5mL0.5mol·L^(-1) 均出现-|||-增大浓-|||-度,化学-|||-浓度 者 率-|||-,但后 反应速-|||-0.1 L-|||-冒-|||-0.1mol·L^(-1)-|||-H2SO4-|||-溶液5mL-|||-0 cdot (L)^-1 混合后均出 升高温-|||-Na2S2O-|||-Na2S2O3 25℃冷水 现-|||-,但 度,化学-|||-温度 ..1molcdot (L)^-1 70℃热水 反应速-|||-Na2S2O3-|||-溶液5mL 一组 __ 率-|||-..1molcdot (L)^-1-|||-H2SO4-|||-溶液5mL 70℃热水-|||-3min后分别混-|||-合并振荡-|||-5滴 cdot (L)^-1 了 前者 __ 催化剂-|||-催 FeCl3溶液 ,能-|||-荆 后者 化-|||-学反应-|||-2mL5% 速率-|||--H2O2溶液--|||-(2)实验Ⅱ:反应速率的定量测定和比较-|||- 1molcdot (L)^-1 的硫酸和锌粒,测量收集10mL-|||-实验步骤 ①取一套装置(如图所示),加入-|||-H2所需的时间。-|||-硫酸-|||-=-10-|||-锌粒 __-|||-②取另一套装置,加入 4molcdot (L)^-1 的硫酸-|||-和锌粒,测量收集10mLH2所需的时间。-|||-实验现象 锌与稀硫酸反应 __ (写现-|||-象),收集10mL气体,②所用时间比①所用时间-|||-__-|||-实验结果-|||-加入试剂-|||-反应时间(填 反应速率(填-|||-"长"或"短") "快"或"慢")-|||-.cdot -|||-.L^(-1) 硫酸-|||- 4molcdot -|||-.^-1 硫酸-|||-_(-1) 硫酸与锌反应的速率-|||-实验结论 cdot (L)^-1 硫酸与锌反应比 -|||-注意事项 ①锌的颗粒(即-|||-表面积)大小基本相同;-|||-②40m L的稀硫酸要迅速加-|||-入;③装置气密性良好,且计-|||-时要迅速准确;④气体收集-|||-可以用排水量气装置(如图-|||-所示)代替。-|||-实验讨论 除本实验测定反应速率的方法外,可-|||-行的方案还有(至少填两种):-|||-①__ ;-|||-__-|||-2/3 __ -|||-;
题目解答
答案
