题目
1molH2(可视为理想气体)从298K、100kPa在终态压力下经绝热恒外压膨胀至10kPa,求此过程的W、1molH2和1molH2
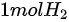 (可视为理想气体)从298K、100kPa在终态压力下经绝热恒外压膨胀至10kPa,求此过程的W、
(可视为理想气体)从298K、100kPa在终态压力下经绝热恒外压膨胀至10kPa,求此过程的W、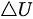 和
和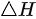
题目解答
答案
对于绝热过程 Q = 0
理想气体绝热过程方程: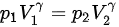
对于双原子理想气体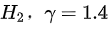
已知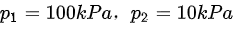
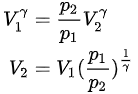
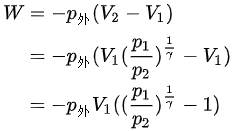
由理想气体状态方程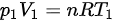 ,可得
,可得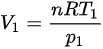 ,代入上式
,代入上式
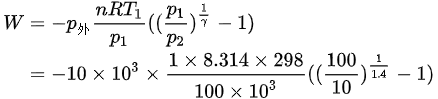
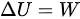
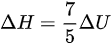 .
.
解析
步骤 1:确定绝热过程的性质
绝热过程意味着没有热量交换,即 Q = 0。对于理想气体,绝热过程遵循方程 ${P}_{1}{V}_{1}^{\gamma}={P}_{2}{V}_{2}^{\gamma}$,其中 $\gamma$ 是比热容比,对于双原子理想气体 ${H}_{2}$,$\gamma = 1.4$。
步骤 2:计算体积变化
已知 ${P}_{1}=100kPa$,${P}_{2}=10kPa$,根据绝热过程方程,可以求出体积变化。首先,利用理想气体状态方程 ${P}_{1}{V}_{1}=nR{T}_{1}$,求出初始体积 ${V}_{1}$。然后,利用绝热过程方程求出终态体积 ${V}_{2}$。
步骤 3:计算功
对于恒外压过程,功的计算公式为 $W=-{P}_{外}({V}_{2}-{V}_{1})$。其中,${P}_{外}$ 是终态压力,即 ${P}_{2}=10kPa$。将 ${V}_{1}$ 和 ${V}_{2}$ 代入公式计算功。
步骤 4:计算内能变化
对于理想气体,内能变化 $\Delta U$ 可以通过 $\Delta U=nC_{V}\Delta T$ 计算,其中 $C_{V}$ 是摩尔定容热容,对于双原子理想气体 ${H}_{2}$,$C_{V}=\dfrac {5}{2}R$。由于绝热过程,$\Delta U=-W$。
步骤 5:计算焓变
焓变 $\Delta H$ 可以通过 $\Delta H=nC_{P}\Delta T$ 计算,其中 $C_{P}$ 是摩尔定压热容,对于双原子理想气体 ${H}_{2}$,$C_{P}=\dfrac {7}{2}R$。由于 $\Delta H=\Delta U+P\Delta V$,可以利用 $\Delta U$ 和体积变化计算 $\Delta H$。
绝热过程意味着没有热量交换,即 Q = 0。对于理想气体,绝热过程遵循方程 ${P}_{1}{V}_{1}^{\gamma}={P}_{2}{V}_{2}^{\gamma}$,其中 $\gamma$ 是比热容比,对于双原子理想气体 ${H}_{2}$,$\gamma = 1.4$。
步骤 2:计算体积变化
已知 ${P}_{1}=100kPa$,${P}_{2}=10kPa$,根据绝热过程方程,可以求出体积变化。首先,利用理想气体状态方程 ${P}_{1}{V}_{1}=nR{T}_{1}$,求出初始体积 ${V}_{1}$。然后,利用绝热过程方程求出终态体积 ${V}_{2}$。
步骤 3:计算功
对于恒外压过程,功的计算公式为 $W=-{P}_{外}({V}_{2}-{V}_{1})$。其中,${P}_{外}$ 是终态压力,即 ${P}_{2}=10kPa$。将 ${V}_{1}$ 和 ${V}_{2}$ 代入公式计算功。
步骤 4:计算内能变化
对于理想气体,内能变化 $\Delta U$ 可以通过 $\Delta U=nC_{V}\Delta T$ 计算,其中 $C_{V}$ 是摩尔定容热容,对于双原子理想气体 ${H}_{2}$,$C_{V}=\dfrac {5}{2}R$。由于绝热过程,$\Delta U=-W$。
步骤 5:计算焓变
焓变 $\Delta H$ 可以通过 $\Delta H=nC_{P}\Delta T$ 计算,其中 $C_{P}$ 是摩尔定压热容,对于双原子理想气体 ${H}_{2}$,$C_{P}=\dfrac {7}{2}R$。由于 $\Delta H=\Delta U+P\Delta V$,可以利用 $\Delta U$ 和体积变化计算 $\Delta H$。