题目
16.21 向各离子浓度均为 .1molcdot (dm)^-3 的 ^2+ ,^2+ ,^2+ ,^+ ,^2+ ,(b)^2+ 混合溶液中通-|||-入H2S气体,可被沉淀的离子有 __
题目解答
答案
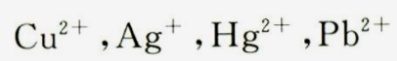
解析
步骤 1:确定H2S的溶解度和电离
H2S在水中部分电离,产生HS-和S2-离子。由于H2S的电离常数较小,因此在水中主要以HS-离子形式存在,而S2-离子浓度较低。
步骤 2:计算S2-离子的浓度
由于H2S的电离常数较小,我们可以假设S2-离子的浓度远小于HS-离子的浓度。因此,S2-离子的浓度可以近似为H2S的电离常数乘以H2S的浓度。根据题目条件,H2S的浓度为0.1mol·dm^-3,因此S2-离子的浓度约为10^-20mol·dm^-3。
步骤 3:计算各离子与S2-离子形成沉淀的溶度积
根据题目条件,各离子的浓度均为0.1mol·dm^-3。因此,各离子与S2-离子形成沉淀的溶度积为各离子的浓度乘以S2-离子的浓度。根据题目条件,各离子的浓度均为0.1mol·dm^-3,因此各离子与S2-离子形成沉淀的溶度积为10^-21mol^2·dm^-6。
步骤 4:比较各离子与S2-离子形成沉淀的溶度积与溶度积常数
根据题目条件,各离子与S2-离子形成沉淀的溶度积为10^-21mol^2·dm^-6。根据溶度积常数表,${Cu}^{2+}$ ,${Ag}^{+}$ ,${Hg}^{2+}$ ,$P{b}^{2+}$ 的溶度积常数均小于10^-21mol^2·dm^-6,因此这些离子可以与S2-离子形成沉淀。而${Mn}^{2+}$ 和${Zn}^{2+}$ 的溶度积常数均大于10^-21mol^2·dm^-6,因此这些离子不能与S2-离子形成沉淀。
H2S在水中部分电离,产生HS-和S2-离子。由于H2S的电离常数较小,因此在水中主要以HS-离子形式存在,而S2-离子浓度较低。
步骤 2:计算S2-离子的浓度
由于H2S的电离常数较小,我们可以假设S2-离子的浓度远小于HS-离子的浓度。因此,S2-离子的浓度可以近似为H2S的电离常数乘以H2S的浓度。根据题目条件,H2S的浓度为0.1mol·dm^-3,因此S2-离子的浓度约为10^-20mol·dm^-3。
步骤 3:计算各离子与S2-离子形成沉淀的溶度积
根据题目条件,各离子的浓度均为0.1mol·dm^-3。因此,各离子与S2-离子形成沉淀的溶度积为各离子的浓度乘以S2-离子的浓度。根据题目条件,各离子的浓度均为0.1mol·dm^-3,因此各离子与S2-离子形成沉淀的溶度积为10^-21mol^2·dm^-6。
步骤 4:比较各离子与S2-离子形成沉淀的溶度积与溶度积常数
根据题目条件,各离子与S2-离子形成沉淀的溶度积为10^-21mol^2·dm^-6。根据溶度积常数表,${Cu}^{2+}$ ,${Ag}^{+}$ ,${Hg}^{2+}$ ,$P{b}^{2+}$ 的溶度积常数均小于10^-21mol^2·dm^-6,因此这些离子可以与S2-离子形成沉淀。而${Mn}^{2+}$ 和${Zn}^{2+}$ 的溶度积常数均大于10^-21mol^2·dm^-6,因此这些离子不能与S2-离子形成沉淀。