利用下表数据,通过计算说明白云石与透辉石的下列转变反应,在298.15 K和标准条件下,自发进行的方向以及下列反应的标准平衡常数K。(10分)CaMg(CO3)2(白云石,s ) + 2SiO2(石英,s ) = CaMg(SiO3)2(透辉石,s) + 2CO2(g)
利用下表数据,通过计算说明白云石与透辉石的下列转变反应,在298.15 K和标准条件下,自发进行的方向以及下列反应的标准平衡常数K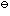 。(10分)
。(10分)
CaMg(CO3)2(白云石,s ) + 2SiO2(石英,s ) = CaMg(SiO3)2(透辉石,s) + 2CO2(g)
题目解答
答案
解: ∆rH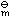 (298.15k)= ∆fH
(298.15k)= ∆fH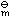 (CaMg(SiO3)2)+ 2∆fH
(CaMg(SiO3)2)+ 2∆fH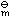 (CO2)-
(CO2)-
∆fH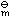 (CaMg(CO3)2)-2∆fH
(CaMg(CO3)2)-2∆fH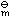 (SiO2)
(SiO2)
=[-3210.76+2×(-393.51)-(-2324.48)- 2×(-910.70)] KJ.mol-1
= 148.1 kJ.mol-1 2分
同理可得:∆rS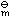 (298.15K) = (143.09+2×213.68-155.19-2×41.46) KJ.mol-1
(298.15K) = (143.09+2×213.68-155.19-2×41.46) KJ.mol-1
=332.34 J.mol-1.K-1 , 2分
∆rG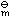 (298.15K) = ∆rH
(298.15K) = ∆rH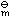 (298.15K) - T∆rS
(298.15K) - T∆rS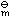 (298.15K) 1分
(298.15K) 1分
=(148.1-298.15×10-3×332.34) KJ.mol-1
=49.01kJ.mol-1>0 1分
所以反应逆向自发 1分
(2) ln K(298.15K) = -∆rG/(RT) 1分=-49.01/8.315×10×298.15=19.77 1分
K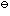 (298.15 K) = 2.59 × 10-9 1分
(298.15 K) = 2.59 × 10-9 1分
解析
根据标准生成焓数据,计算反应的标准焓变(∆rH①)。
步骤 2:计算反应的标准熵变
根据标准熵数据,计算反应的标准熵变(∆rS①)。
步骤 3:计算反应的标准吉布斯自由能变
根据标准焓变和标准熵变,计算反应的标准吉布斯自由能变(∆rG①)。
步骤 4:判断反应的自发性
根据∆rG①的正负判断反应的自发性。
步骤 5:计算标准平衡常数
根据∆rG①计算标准平衡常数K。