15.已知在298K、100 kPa下,丙烷的燃烧焓为 -2220kJcdot (mol)^-1, 水的生成焓 -286.0kJcdot (mol)^-1, CO2的生-|||-成焓 -393.5kJcdot (mol)^-1 试计算丙烷气在等压和等容下的生成焓。

题目解答
答案
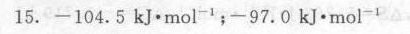
解析
考查要点:本题主要考查燃烧焓与生成焓的关系,以及等压与等容条件下的焓变计算。
解题思路:
- 利用燃烧焓的热化学方程式,结合已知生成焓(CO₂和H₂O),建立方程求解丙烷的等压生成焓。
- 通过理想气体状态方程,计算等容条件下的生成焓,需考虑气体物质的量变化(Δn)。
关键点:
- 燃烧焓的热化学方程式需正确写出反应式,并代入生成焓的差值。
- 等容与等压关系的公式为ΔU = ΔH - Δn·R·T,需准确计算Δn。
步骤1:写出丙烷燃烧的热化学方程式
丙烷燃烧反应为:
$\text{C}_3\text{H}_8(g) + 5\text{O}_2(g) \rightarrow 3\text{CO}_2(g) + 4\text{H}_2\text{O}(l)$
根据燃烧焓的定义,焓变为:
$\Delta H_{\text{combustion}} = \sum \Delta H_f^\circ (\text{生成物}) - \sum \Delta H_f^\circ (\text{反应物})$
代入已知数据(O₂为元素稳定态,ΔHf°=0):
$-2220 = 3(-393.5) + 4(-286.0) - \Delta H_f^\circ (\text{C}_3\text{H}_8)$
步骤2:计算等压生成焓
展开计算:
$-2220 = -1180.5 - 1144.0 - \Delta H_f^\circ (\text{C}_3\text{H}_8)$
$\Delta H_f^\circ (\text{C}_3\text{H}_8) = -2324.5 + 2220 = -104.5 \, \text{kJ·mol}^{-1}$
步骤3:计算等容生成焓
生成丙烷的反应为:
$3\text{C(石墨)} + 4\text{H}_2(g) \rightarrow \text{C}_3\text{H}_8(g)$
气体物质的量变化:
$\Delta n = 1 - 4 = -3$
根据公式 $\Delta U = \Delta H - \Delta n \cdot R \cdot T$:
$\Delta U = -104.5 - (-3) \cdot 8.314 \cdot 298$
$\Delta U = -104.5 + 7.43 = -97.0 \, \text{kJ·mol}^{-1}$