题目
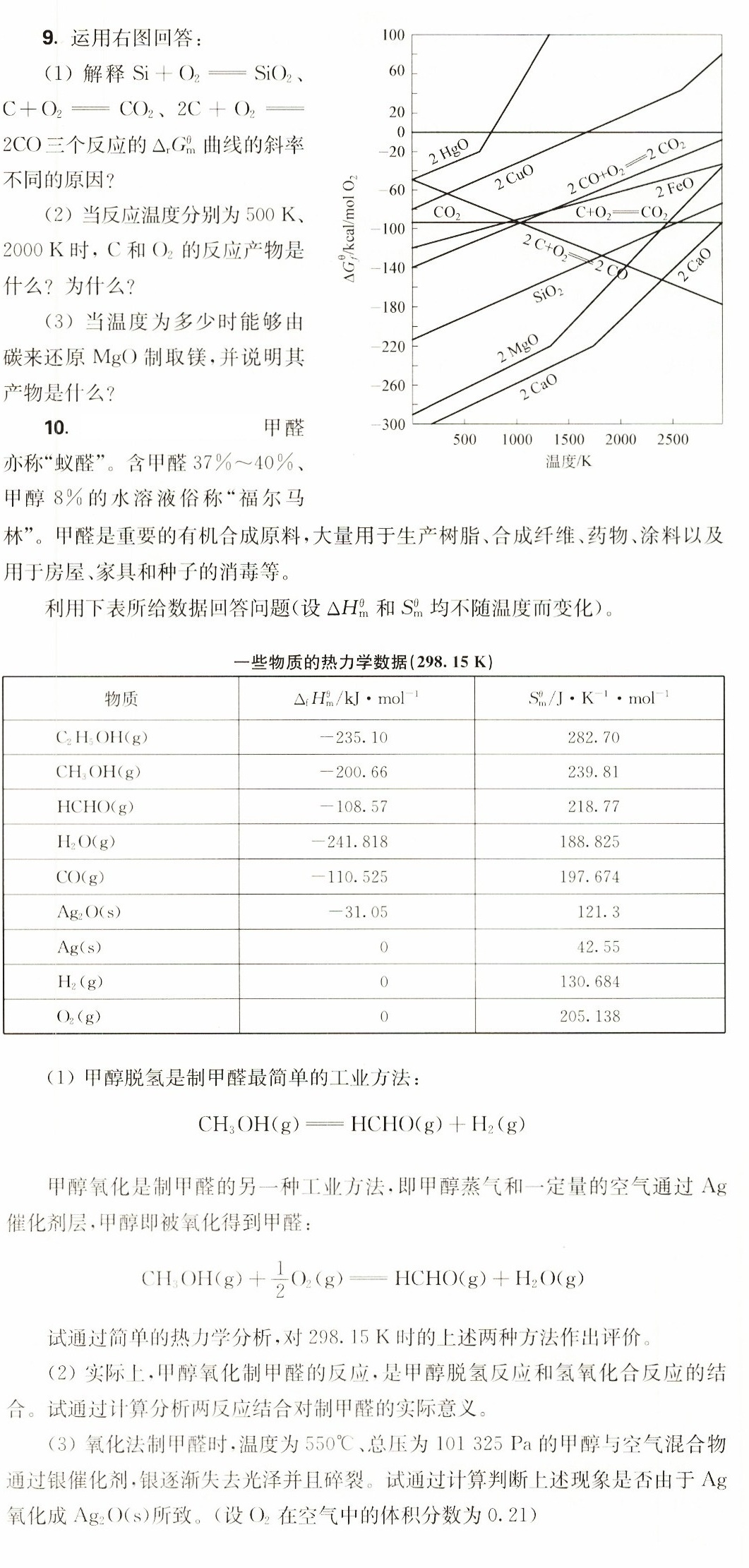
9.运用右图回答:-|||-(1)解释 +(O)_(2)=!=!= Si(O)_(2)-|||-+(O)_(2)=!=!= C(O)_(2)=!=!= Ca((OH))_(2)=!=!= Ca((OH))_(2)=!=!= -|||-2CO三个反应的 Delta (C)_(m)^2 曲线的斜率-|||-不同的原因?-|||-100-|||-60-|||-20-|||-0-|||--20 2HgO-|||-60 2CuO-|||-20000=1000/100-|||-2FeO-|||-CO2 C+O2 CO2-|||-100-|||-2-|||--140-|||-180 SiO2-|||--220 MgO-|||-260 aO-|||--300-|||-500 1000 1500 2000 2500-|||-温度/K-|||-(2)当反应温度分别为500K、-|||-2000K时,C和O2的反应产物是-|||-什么?为什么?-|||-(3)当温度为多少时能够由-|||-碳来还原MgO制取镁,并说明其-|||-产物是什么?-|||-10. 甲醛 -300 500 1000 1500 2000 2500-|||-亦称"蚁醛"。含甲醛 % sim 40% 温度/K-|||-甲醇8%的水溶液俗称"福尔马-|||-林"。甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物、涂料以及-|||-用于房屋、家具和种子的消毒等。-|||-利用下表所给数据回答问题(设 Delta (H)_(1) 和S^(b)与不随温度而变化)。-|||-些物质的热力学数据(298.15K)-|||-物质 Delta (H)_(m)^3=dfrac (1)(2)(N)_(m)((g))^-1 _(10)^11/1cdot (k)^-1cdot (mol)^-1-|||-C2H5OH(g) -235.10 282.70-|||-CH3OH(g) -200.66 239.81-|||-HCHO(g) -108.57 218.77-|||-H2O(g) -241.818 188.825-|||-CO(g) -110.525 197.674-|||-Ag2O(s) -31.05 121.3-|||-Ag(s) 0 42.55-|||-H2(g) 0 130.684-|||-O2(g) 0 205.138-|||-(1)甲醇脱氢是制甲醛最简单的工业方法:-|||-(H)_(3)OH(g)=!=!= HClIO(g)+(H)_(2)(g)-|||-甲醇氧化是制甲醛的另一种工业方法,即甲醇蒸气和一定量的空气通过Ag-|||-催化剂层,甲醇即被氧化得到甲醛:-|||-(H)_(2)OH(g)+dfrac (1)(2)(O)_(2)(g)=!=!= HCHO(g)+(H)_(2)O(g)-|||-试通过简单的热力学分析,对298.15K时的上述两种方法作出评价。-|||-(2)实际上,甲醇氧化制甲醛的反应,是甲醇脱氢反应和氢氧化合反应的结-|||-合。试通过计算分析两反应结合对制甲醛的实际意义。-|||-(3)氧化法制甲醛时温度为550℃、总压为101325 Pa的甲醇与空气混合物-|||-通过银催化剂,银逐渐失去光泽并且碎裂。试通过计算判断上述现象是否由于Ag-|||-氧化成Ag2O(s)所致。(设O2在空气中的体积分数为0.21)
题目解答
答案



