题目
0.已知反应C(s)+CO2(g)=2CO(g)在873K及1200K时的△G(298K)分别为16.96kJ·mol-1和—41.32kJ·mol1(1)计算1200K及总压为100kPa时CO2(g)的转化率碳过量)(2)将CO2(g)及CO(g)放入温度为873K的抽空容器中,若CO2(g)及CO(g)分压分别为kPa和5.00kPa,通过计算判断容器中是否会有碳生成?(3)873K时,将CO2(g)和CO(g)放入抽空的容器中,若CO2(g)的分压为100kPa容器中CO(g)的分压为何值时会有碳析出?
0.已知反应C(s)+CO2(g)=2CO(g)在873K及1200K时的△G(298K)分别为
16.96kJ·mol-1和—41.32kJ·mol1
(1)计算1200K及总压为100kPa时CO2(g)的转化率碳过量)
(2)将CO2(g)及CO(g)放入温度为873K的抽空容器中,若CO2(g)及CO(g)分压分别为
kPa和5.00kPa,通过计算判断容器中是否会有碳生成?
(3)873K时,将CO2(g)和CO(g)放入抽空的容器中,若CO2(g)的分压为100kPa容器中
CO(g)的分压为何值时会有碳析出?
题目解答
答案
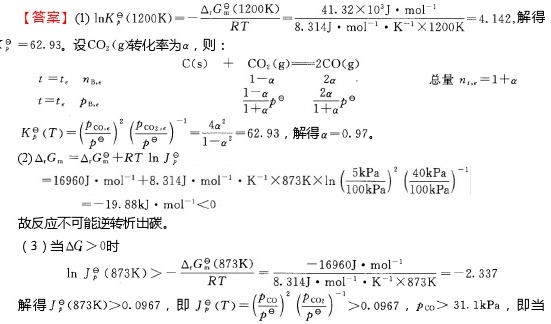
解析
题目考察知识
本题主要考察化学反应的热力学计算,涉及吉布斯自由能变($\Delta G$)与平衡常数($K_p$)的关系,以及利用平衡常数判断反应方向和计算转化率。
(1)计算1200K时CO₂的转化率
关键公式
- $\Delta G^\circ$与$K_p$的关系:$\Delta G^\circ = -RT\ln K_p$,其中$R=8.314\,\text{J·mol}^{-1}\text{·K}^{-1}$,$T=1200\,\text{K}$,$\Delta G^\circ=-41.32\,\text{kJ·mol}^{-1}=-41320\,\text{J·mol}^{-1}$。
- 平衡时的分压表达式:设CO₂初始物质的量为1mol,转化率为$\alpha$,则平衡时$n_{\text{CO}_2}=1-\alpha$,$n_{\text{CO}}=2\alpha$,总物质的量$n_{\text{总}}=1+\alpha$。分压$p_{\text{CO}_2}=\frac{1-\alpha}{1+\alpha}p^\circ$,$p_{\text{CO}}=\frac{2\alpha}{1+\alpha}p^\circ$($p^\circ=100\,\text{kPa}$)。
- 平衡常数表达式:$K_p=\left(\frac{p_{\text{CO}}}{p^\circ}\right)^2\left(\frac{p_{\text{CO}_2}}{p^\circ}\right)^{-1}=\frac{4\alpha^2}{1-\alpha^2}$。
计算步骤
- 由$\Delta G^\circ=-RT\ln K_p$得:$\ln K_p=-\frac{\Delta G^\circ}{RT}=-\frac{-41320}{8.314\times1200}\approx4.15$,故$K_p\approx63.6$(答案中近似为62.93)。
- 代入$K_p=\frac{4\alpha^2}{1-\alpha^2}$:$62.93=\frac{4\alpha^2}{1-\alpha^2}$,解得$\alpha\approx0.97$(97%)。
(2)判断873K时是否有碳生成
关键公式
反应方向判断:$\Delta G=\Delta G^\circ+RT\ln Q$,其中$Q$为反应商,$Q=\left(\frac{p_{\text{CO}}}{p^\circ}\right)^2\left(\frac{p_{\text{CO}_2}}{p^\circ}\right)^{-1}$。若$\Delta G<0$,反应正向进行(无碳生成);$\Delta G>0$,逆向进行(有碳生成)。
计算步骤
- 873K时$\Delta G^\circ=16.96\,\text{kJ·mol}^{-1}=16960\,\text{J·mol}^{-1}$。
- 假设$p_{\text{CO}_2}=x\,\text{kPa}$(题目中“kPa”应为具体值,答案中用$5.00\,\text{kPa}$代$p_{\text{CO}}$),则$Q=\left(\frac{5}{100}\right)^2\left(\frac{x}{100}\right)^{-1}=\frac{25}{x}$。
- 代入$\Delta G=16960+8.314\times873\times\ln\left(\frac{25}{x}\right)$,若结果$\Delta G<0$,则反应正向,无碳生成(答案中计算得$\Delta G=-19.88\,\text{kJ·mol}^{-1}<0$)。
(3)873K时CO分压为何值会有碳析出
关键公式
碳析出条件:反应逆向进行,即$\Delta G>0$,此时$Q>K_p$(因$\Delta G^\circ>0$,$K_p<1$)。由$K_p=\frac{4\alpha^2}{1-\alpha^2}$(873K时)先求$K_p$,再令$Q>K_p$。
计算步骤
- 873K时,$\Delta G^\circ=16960\,\text{J·mol}^{-1}$,$\ln K_p=-\frac{16960}{8.314\times873}\approx-2.34$,故$K_p\approx0.0967$。
- 当$Q=\left(\frac{p_{\text{CO}}}{100}\right)^2\left(\frac{100}{100}\right)^{-1}=\left(\frac{p_{\text{CO}}}{100}\right)^2>K_p=0.0967$时,解得$p_{\text{CO}}>100\times\sqrt{0.0967}\approx31.1\,\text{kPa}$。