题目
8-1 测定 .30times (10)^-4mol/L 的CaCl2溶液的活度,若溶液中存在 0.20mol/L 的NaCl,-|||-计算:-|||-(1)由于NaCl的存在所引起的相对误差是多少?(已知 _({Ca)^2+}, ^+=0.0016)-|||-(2)若要使误差减少至2%,允许NaCl的最高浓度是多少?

题目解答
答案
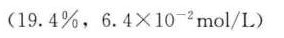
解析
步骤 1:计算CaCl2溶液中Ca2+的活度系数
根据已知的${K}_{{Ca}^{2+}},{Na}^{+}=0.0016$,可以计算出Ca2+的活度系数。活度系数的计算公式为:
$$ \gamma_{Ca^{2+}} = \frac{1}{1 + K_{Ca^{2+},Na^{+}} \cdot c_{Na^{+}}} $$
其中,$c_{Na^{+}}$是Na+的浓度,即0.20mol/L。
步骤 2:计算Ca2+的活度
Ca2+的活度计算公式为:
$$ a_{Ca^{2+}} = \gamma_{Ca^{2+}} \cdot c_{Ca^{2+}} $$
其中,$c_{Ca^{2+}}$是Ca2+的浓度,即$3.30\times {10}^{-4}mol/L$。
步骤 3:计算相对误差
相对误差计算公式为:
$$ \text{相对误差} = \frac{a_{Ca^{2+}} - c_{Ca^{2+}}}{c_{Ca^{2+}}} \times 100\% $$
步骤 4:计算允许NaCl的最高浓度
根据相对误差的计算公式,可以反推出允许NaCl的最高浓度。设允许NaCl的最高浓度为$c_{Na^{+}}'$,则有:
$$ \frac{a_{Ca^{2+}}' - c_{Ca^{2+}}}{c_{Ca^{2+}}} \times 100\% = 2\% $$
其中,$a_{Ca^{2+}}'$是Ca2+的活度,计算公式为:
$$ a_{Ca^{2+}}' = \gamma_{Ca^{2+}}' \cdot c_{Ca^{2+}} $$
其中,$\gamma_{Ca^{2+}}'$是Ca2+的活度系数,计算公式为:
$$ \gamma_{Ca^{2+}}' = \frac{1}{1 + K_{Ca^{2+},Na^{+}} \cdot c_{Na^{+}}'} $$
根据已知的${K}_{{Ca}^{2+}},{Na}^{+}=0.0016$,可以计算出Ca2+的活度系数。活度系数的计算公式为:
$$ \gamma_{Ca^{2+}} = \frac{1}{1 + K_{Ca^{2+},Na^{+}} \cdot c_{Na^{+}}} $$
其中,$c_{Na^{+}}$是Na+的浓度,即0.20mol/L。
步骤 2:计算Ca2+的活度
Ca2+的活度计算公式为:
$$ a_{Ca^{2+}} = \gamma_{Ca^{2+}} \cdot c_{Ca^{2+}} $$
其中,$c_{Ca^{2+}}$是Ca2+的浓度,即$3.30\times {10}^{-4}mol/L$。
步骤 3:计算相对误差
相对误差计算公式为:
$$ \text{相对误差} = \frac{a_{Ca^{2+}} - c_{Ca^{2+}}}{c_{Ca^{2+}}} \times 100\% $$
步骤 4:计算允许NaCl的最高浓度
根据相对误差的计算公式,可以反推出允许NaCl的最高浓度。设允许NaCl的最高浓度为$c_{Na^{+}}'$,则有:
$$ \frac{a_{Ca^{2+}}' - c_{Ca^{2+}}}{c_{Ca^{2+}}} \times 100\% = 2\% $$
其中,$a_{Ca^{2+}}'$是Ca2+的活度,计算公式为:
$$ a_{Ca^{2+}}' = \gamma_{Ca^{2+}}' \cdot c_{Ca^{2+}} $$
其中,$\gamma_{Ca^{2+}}'$是Ca2+的活度系数,计算公式为:
$$ \gamma_{Ca^{2+}}' = \frac{1}{1 + K_{Ca^{2+},Na^{+}} \cdot c_{Na^{+}}'} $$