题目
氢氧化钠溶液用间接法配制的原因是 A 氢氧化钠易吸收空气中的水分B 间接法比直接法更容易配制一定浓度的溶液 C 氢氧化钠会与空气中的 CO2 反应 D 氢氧化钠的相对分子质量太
氢氧化钠溶液用间接法配制的原因是
A 氢氧化钠易吸收空气中的水分
B 间接法比直接法更容易配制一定浓度的溶液
C 氢氧化钠会与空气中的 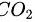 反应
反应
D 氢氧化钠的相对分子质量太
题目解答
答案
ABC
A. 氢氧化钠易吸收空气中的水分
B. 间接法比直接法更容易配制一定浓度的溶液
C. 氢氧化钠会与空气中的CO2反应
A. 氢氧化钠易吸收空气中的水分
B. 间接法比直接法更容易配制一定浓度的溶液
C. 氢氧化钠会与空气中的CO2反应
解析
步骤 1:氢氧化钠的吸湿性
氢氧化钠(NaOH)具有很强的吸湿性,容易吸收空气中的水分,导致其质量增加,从而影响溶液的浓度。如果直接配制氢氧化钠溶液,吸湿性会导致溶液浓度不准确。
步骤 2:氢氧化钠与二氧化碳的反应
氢氧化钠在空气中不稳定,会与二氧化碳(CO2)反应生成碳酸钠(Na2CO3)和水(H2O),导致其变质。反应方程式为:2NaOH + CO2 → Na2CO3 + H2O。这种反应会进一步影响溶液的浓度和稳定性。
步骤 3:间接法配制氢氧化钠溶液
间接法配制氢氧化钠溶液,通常使用基准物质(如邻苯二甲酸氢钾)来标定氢氧化钠溶液的准确浓度。这种方法可以避免氢氧化钠吸湿和与二氧化碳反应带来的影响,确保溶液浓度的准确性和稳定性。
氢氧化钠(NaOH)具有很强的吸湿性,容易吸收空气中的水分,导致其质量增加,从而影响溶液的浓度。如果直接配制氢氧化钠溶液,吸湿性会导致溶液浓度不准确。
步骤 2:氢氧化钠与二氧化碳的反应
氢氧化钠在空气中不稳定,会与二氧化碳(CO2)反应生成碳酸钠(Na2CO3)和水(H2O),导致其变质。反应方程式为:2NaOH + CO2 → Na2CO3 + H2O。这种反应会进一步影响溶液的浓度和稳定性。
步骤 3:间接法配制氢氧化钠溶液
间接法配制氢氧化钠溶液,通常使用基准物质(如邻苯二甲酸氢钾)来标定氢氧化钠溶液的准确浓度。这种方法可以避免氢氧化钠吸湿和与二氧化碳反应带来的影响,确保溶液浓度的准确性和稳定性。