题目
、根据有关热力学数据,近似计算CCl4(l)在101.3 kPa压力下和20 kPa压力下的沸腾温度。已知ΔfH (CCl4,g,298 K) = -102.93 kJ·mol-1,S (CCl4,g,298 K) = 309.74 J·K-1·mol-1,其他数据见书后附录。
、根据有关热力学数据,近似计算CCl4(l)在101.3 kPa压力下和20 kPa压力下的沸腾温度。已知ΔfH (CCl4,g,298 K) = -102.93 kJ·mol-1,S (CCl4,g,298 K) = 309.74 J·K-1·mol-1,其他数据见书后附录。
题目解答
答案
解:查表得:
CCl4(l) CCl4(g)
ΔfH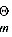 / kJ·mol-1 -135.4 -102.93
/ kJ·mol-1 -135.4 -102.93
S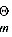 / J·K-1·mol-1, 216.4 309.74
/ J·K-1·mol-1, 216.4 309.74
CCl4(l) = CCl4(g)
ΔrH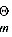 = 32.47 kJ·mol-1
= 32.47 kJ·mol-1
ΔrS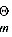 =0.09334 kJ·mol-1
=0.09334 kJ·mol-1
所以,的正常沸点为 T1= ΔrH /ΔrS
/ΔrS = 348 K
= 348 K
根据克拉贝龙-克劳休斯方程
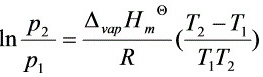
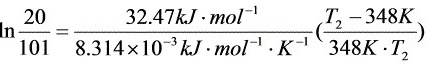
T2=304K
解析
步骤 1:计算反应的焓变和熵变
根据题目提供的数据,计算CCl4(l)转化为CCl4(g)的焓变和熵变。
步骤 2:计算正常沸点
利用焓变和熵变计算CCl4(l)在101.3 kPa下的正常沸点。
步骤 3:利用克拉贝龙-克劳休斯方程计算20 kPa下的沸点
利用克拉贝龙-克劳休斯方程计算CCl4(l)在20 kPa下的沸点。
根据题目提供的数据,计算CCl4(l)转化为CCl4(g)的焓变和熵变。
步骤 2:计算正常沸点
利用焓变和熵变计算CCl4(l)在101.3 kPa下的正常沸点。
步骤 3:利用克拉贝龙-克劳休斯方程计算20 kPa下的沸点
利用克拉贝龙-克劳休斯方程计算CCl4(l)在20 kPa下的沸点。