题目
按分子轨道理论写出 NF ^+ ^- 的基态电子组态,说明它们的不成对电子数和磁-|||-性(提示:按类似O2的能级排)。

题目解答
答案
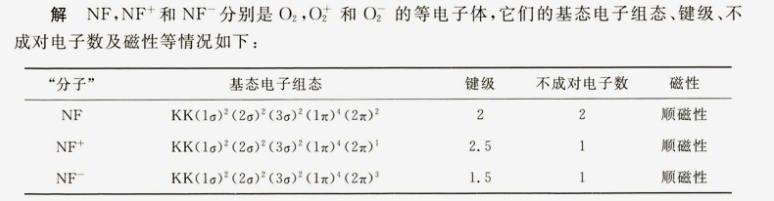
解析
本题考查等电子体分子的基态电子组态、键级、不成对电子数及磁性的判断。解题核心在于:
- 确定等电子体:NF、NF⁺、NF⁻分别与O₂、O₂⁺、O₂⁻互为等电子体(原子数和价电子总数相同)。
- 分子轨道填充顺序:按O₂的分子轨道能级顺序(σ2s < σ2s < σ2p < π2p < π2p)填充电子。
- 键级与磁性计算:键级公式为$\text{键级} = \frac{\text{成键电子数} - \text{反键电子数}}{2}$,不成对电子数由π*轨道的电子排布决定。
NF(中性态)
- 价电子总数:氮(5)+氟(7)=12,与O₂相同。
- 电子组态:
$\text{KK}(1\sigma)^2 (2\sigma)^2 (3\sigma)^2 (1\pi)^4 (2\pi)^2$- 成键电子数:$2+2+4=8$
- 反键电子数:$2+2=4$
- 键级:$\frac{8-4}{2}=2$
- 不成对电子数:$2$(来自两个π*轨道各1个单电子)
- 磁性:顺磁性。
NF⁺(失去1电子)
- 价电子总数:12−1=11,与O₂⁺相同。
- 电子组态:
$\text{KK}(1\sigma)^2 (2\sigma)^2 (3\sigma)^2 (1\pi)^4 (2\pi)^1$- 成键电子数:$2+2+4=8$
- 反键电子数:$2+1=3$
- 键级:$\frac{8-3}{2}=2.5$
- 不成对电子数:$1$(来自1个π*轨道的单电子)
- 磁性:顺磁性。
NF⁻(获得1电子)
- 价电子总数:12+1=13,与O₂⁻相同。
- 电子组态:
$\text{KK}(1\sigma)^2 (2\sigma)^2 (3\sigma)^2 (1\pi)^4 (2\pi)^3$- 成键电子数:$2+2+4=8$
- 反键电子数:$2+3=5$
- 键级:$\frac{8-5}{2}=1.5$
- 不成对电子数:$1$(来自1个π*轨道的单电子)
- 磁性:顺磁性。