题目
用HCl溶液滴定某碱液,量取两份碱液。一份以甲基橙为指示剂,消耗HCl体积为-|||-V1;另一份以酚酞为指示剂,消耗HCl体积为V2。若 _(1)=(V)_(2) ,则该碱液为 ()-|||-A.Na2CO3 B.NaHCO3-|||-C.NaOH D.NaOH与Na2CO3

题目解答
答案
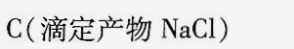
解析
本题考查酸碱滴定中指示剂的选择与反应终点的关系。关键点在于理解不同指示剂的变色范围及对应的不同反应阶段。酚酞变色范围在弱碱性区域(pH 8.2~4.4),甲基橙在酸性区域(pH 3.1~4.4)。对于不同碱性物质(如强碱、碳酸盐、碳酸氢盐),滴定终点对应的反应程度不同,导致消耗HCl的体积关系发生变化。当V₁=V₂时,说明两种指示剂的终点消耗HCl体积相同,对应反应一步完成,无中间阶段。
选项分析
-
Na₂CO₃(选项A)
与HCl反应分两步:- 酚酞终点:Na₂CO₃ + HCl → NaHCO₃ + NaCl(消耗1 mol HCl)
- 甲基橙终点:NaHCO₃ + HCl → NaCl + CO₂↑ + H₂O(额外消耗1 mol HCl)
因此,V₁(甲基橙)= 2V₂(酚酞),不符合V₁=V₂。
-
NaHCO₃(选项B)
与HCl反应一步完成:
NaHCO₃ + HCl → NaCl + CO₂↑ + H₂O
理论上需等物质的量HCl。但酚酞在弱碱性条件下可能提前变色,导致实际V₂ < V₁,故V₁≠V₂。 -
NaOH(选项C)
与HCl反应一步完成:
NaOH + HCl → NaCl + H₂O
无论终点在中性(酚酞)还是弱酸性(甲基橙),所需HCl物质的量相同,故V₁=V₂。 -
NaOH与Na₂CO₃混合物(选项D)
滴定时,HCl先中和NaOH,再与Na₂CO₃反应。两种指示剂的终点对应不同阶段,导致V₁≠V₂。