题目
含有rm( Fe^3+) 的某药物溶解后,加入显色剂KSCN溶液,生成红色配合物,用1.00cm吸收池在分光光度计420nm波长处测定,已知该配合物在上述条件下值为1.8times (10)^4 ,如该药物含rm( Fe^3+) 约为0.5%,现欲配制50ml试液,为使测定相对误差最小,应称取该药多少克?(rm M_(Fe)=55.85)
含有$$\rm{ Fe^{3+}} $$的某药物溶解后,加入显色剂KSCN溶液,生成红色配合物,用1.00cm吸收池在分光光度计420nm波长处测定,已知该配合物在上述条件下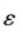 值为$$1.8\times {10}^{4} $$,如该药物含$$\rm{ Fe^{3+}} $$约为0.5%,现欲配制50ml试液,为使测定相对误差最小,应称取该药多少克?($$\rm M_{Fe}$$=55.85)
值为$$1.8\times {10}^{4} $$,如该药物含$$\rm{ Fe^{3+}} $$约为0.5%,现欲配制50ml试液,为使测定相对误差最小,应称取该药多少克?($$\rm M_{Fe}$$=55.85)
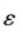 值为$$1.8\times {10}^{4} $$,如该药物含$$\rm{ Fe^{3+}} $$约为0.5%,现欲配制50ml试液,为使测定相对误差最小,应称取该药多少克?($$\rm M_{Fe}$$=55.85)
值为$$1.8\times {10}^{4} $$,如该药物含$$\rm{ Fe^{3+}} $$约为0.5%,现欲配制50ml试液,为使测定相对误差最小,应称取该药多少克?($$\rm M_{Fe}$$=55.85)题目解答
答案
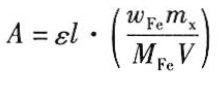
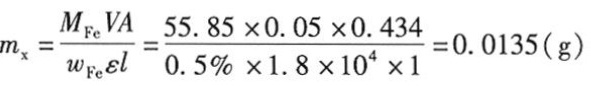
解析
步骤 1:确定吸光度与浓度的关系
根据朗伯-比尔定律,吸光度A与浓度c的关系为:$$A = \varepsilon \cdot c \cdot l$$,其中$$\varepsilon$$为摩尔吸光系数,l为光程长度,c为溶液浓度。
步骤 2:计算浓度
根据题目,$$\varepsilon = 1.8 \times 10^4$$,l = 1.00cm,A = 0.434(由题意可知,为了使测定相对误差最小,吸光度A应为0.434),代入公式计算浓度c。
步骤 3:计算所需药物的质量
根据浓度c,计算出所需药物的质量。浓度c = $$\frac{m_{x} \cdot W_{e} \cdot m_{e}}{M_{Fe} \cdot V}$$,其中$$m_{x}$$为所需药物的质量,$$W_{e}$$为药物中$$\rm{Fe^{3+}}$$的质量分数,$$m_{e}$$为$$\rm{Fe^{3+}}$$的摩尔质量,$$M_{Fe}$$为铁的摩尔质量,V为溶液体积。
根据朗伯-比尔定律,吸光度A与浓度c的关系为:$$A = \varepsilon \cdot c \cdot l$$,其中$$\varepsilon$$为摩尔吸光系数,l为光程长度,c为溶液浓度。
步骤 2:计算浓度
根据题目,$$\varepsilon = 1.8 \times 10^4$$,l = 1.00cm,A = 0.434(由题意可知,为了使测定相对误差最小,吸光度A应为0.434),代入公式计算浓度c。
步骤 3:计算所需药物的质量
根据浓度c,计算出所需药物的质量。浓度c = $$\frac{m_{x} \cdot W_{e} \cdot m_{e}}{M_{Fe} \cdot V}$$,其中$$m_{x}$$为所需药物的质量,$$W_{e}$$为药物中$$\rm{Fe^{3+}}$$的质量分数,$$m_{e}$$为$$\rm{Fe^{3+}}$$的摩尔质量,$$M_{Fe}$$为铁的摩尔质量,V为溶液体积。