碳、氢、氧3种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子个数为氧的5倍. 一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团.且B的核磁共振氢谱显示有3组不同的峰.(1)A的分子式是 C5H10O2 .(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量与生成水的量均相等的是 BC (填序号).A.C5H12O3 B.C4H10 C.6H10O44 D.C6H10O(3)B的结构简式是 .A. C B. Cu 1s22s22p63s23p63d104s1C. B D. Zn [Ar]4s23.“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是( )A. 泡利原理 B. 洪特规则 C. 构造原理 D. 能量最低原理4. 价层电子排布为3d34s2的元素属于下列哪一类元素( )A. 稀有气体 B. 主族元素 C. 过渡元素 D. 卤族元素5.下列物质从固态转变成气态只需克服范德华力的是( )A. 冰 B. KCl C. 金属钠 D. 碘6.金属晶体的下列性质中,不能用金属键加以解释的是( ) A. 有金属光泽 B. 易被氧化 C.有延展性 D. 易导电7.下列说法中不正确的是( )A. 一般情况下,σ键比π键重叠程度大,形成的共价键强B. 两个原子间形成共价键时,最多有一个σ键C. 只含极性键的分子一定是极性分子D. 碳碳双键中一定有一个σ键,一个π键,碳碳三键中一定有一个σ键,二个π键8.下列晶体中,化学键种类完全相同,晶体类型也相同的是( )A. CO2与SiO2 B. CCl4与SiCl4 C. SO2与MgO D. NaCl与HCl9.用价层电子对互斥理论预测PCl3和CO32-的空间构型,结论正确的是( )A. 直线形;三角锥形 B. 三角锥形;平面三角形C. V形;三角锥形 D. 直线形;平面三角形10.下列事实,不能用氢键知识解释的是 ( )A. 氟化氢的沸点高于氯化氢 B. 水和乙醇可以完全互溶(4)A还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,其中一种水解产物分子中有2个甲基,该异构体的结构简式是 CH3COOCH(CH3)2 ..
碳、氢、氧3种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子个数为氧的5倍. 一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团.且B的核磁共振氢谱显示有3组不同的峰.
(1)A的分子式是 C5H10O2 .
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量与生成水的量均相等的是 BC (填序号).
A.C5H12O3 B.C4H10 C.6H10O44 D.C6H10O
(3)B的结构简式是 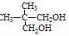 .
.
A. C  B. Cu 1s22s22p63s23p63d104s1
B. Cu 1s22s22p63s23p63d104s1
C. B  D. Zn [Ar]4s2
D. Zn [Ar]4s2
3.“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是( )
A. 泡利原理 B. 洪特规则 C. 构造原理 D. 能量最低原理
4. 价层电子排布为3d34s2的元素属于下列哪一类元素( )
A. 稀有气体 B. 主族元素 C. 过渡元素 D. 卤族元素
5.下列物质从固态转变成气态只需克服范德华力的是( )
A. 冰 B. KCl C. 金属钠 D. 碘
6.金属晶体的下列性质中,不能用金属键加以解释的是( ) A. 有金属光泽 B. 易被氧化 C.有延展性 D. 易导电
7.下列说法中不正确的是( )
A. 一般情况下,σ键比π键重叠程度大,形成的共价键强
B. 两个原子间形成共价键时,最多有一个σ键
C. 只含极性键的分子一定是极性分子
D. 碳碳双键中一定有一个σ键,一个π键,碳碳三键中一定有一个σ键,二个π键
8.下列晶体中,化学键种类完全相同,晶体类型也相同的是( )
A. CO2与SiO2 B. CCl4与SiCl4 C. SO2与MgO D. NaCl与HCl
9.用价层电子对互斥理论预测PCl3和CO32-的空间构型,结论正确的是( )
A. 直线形;三角锥形 B. 三角锥形;平面三角形
C. V形;三角锥形 D. 直线形;平面三角形
10.下列事实,不能用氢键知识解释的是 ( )
A. 氟化氢的沸点高于氯化氢 B. 水和乙醇可以完全互溶
(4)A还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,其中一种水解产物分子中有2个甲基,该异构体的结构简式是 CH3COOCH(CH3)2 .
.题目解答
答案
[解答]解:(1)有机物A相对分子质量为氢气的51倍,则有机物A的相对分子质量=51×2=102,含氢的质量分数为9.8%,则分子中含有的N(H)=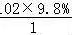 =10,分子中氢原子个数为氧个数的5倍,则N(O)=
=10,分子中氢原子个数为氧个数的5倍,则N(O)=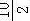 =5,N(C)=
=5,N(C)=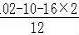 =5,所以有机物A的分子式为C5H10O2,
=5,所以有机物A的分子式为C5H10O2,
故答案为:C5H10O2;
(2)设烃及烃的含氧衍生物组成通式为CxHyOz,总物质的量一定时,以任意比混合,有机物完全燃烧消耗氧气的物质的量和生成水的物质的量不变,则化学式中的氢原子个数相同,每摩尔有机物耗氧量(x+ ﹣
﹣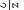 )mol相同即符合题意,符合条件的有机物是C4H10和C6H10O4,
)mol相同即符合题意,符合条件的有机物是C4H10和C6H10O4,
故选BC;
(3)一定条件下,A与一定氢气反应生成B,B分子的结构可视为一个碳原子上连接两个甲基和另外两个结构相同的基团,B的核磁共振氢谱显示有3组不同的峰,有三种氢原子,则B为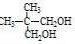 ,反应为
,反应为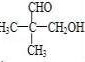 →
→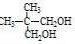 ,
,
故答案为: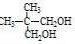 ;
;
(4)B为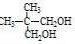 ,反应为
,反应为 →
→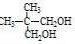 ,
,
则A( )还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,则为乙酸与丙醇,其中一种的分子中有2个甲基,则为2﹣丙醇,A的同分异构体为CH3COOCH(CH3)2,
)还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,则为乙酸与丙醇,其中一种的分子中有2个甲基,则为2﹣丙醇,A的同分异构体为CH3COOCH(CH3)2,
故答案为:CH3COOCH(CH3)2.
.