题目
一、电解质和非电解质-|||-1.电解质:在 __ 里或 __ 状态下能导电的化合物。-|||-2.非电解质:在 __ 里和 __ 状态下都不导电的化-|||-合物。-|||-3.电解质与非电解质的比较-|||-电解质 非电解质-|||-相同点 均为 __-|||-不同点 能导电-|||-水溶液或熔融状态 水溶液和熔融状态都不能导电-|||-本质 在水溶液里和熔融状态下自身 __-|||-在水溶液里或熔融-|||-区别 状态下自身能发生-|||-发生电离-|||-电离-|||-酸:H2SO4、H2 CO3等;-|||-碱:NaOH、NH3· 非金属氧化物:SO 2、SO3、CO2、-|||-H2O等; CO、P2 O5等;-|||-所含物-|||-质类型-|||-盐:NaCl、CaCO3等; 非酸性气态氢化物:NH3;-|||-活泼金属氧化物: 部分有机物:蔗糖、酒精、CH4、-|||-Na2O等 CCl4等。-|||-水。
题目解答
答案
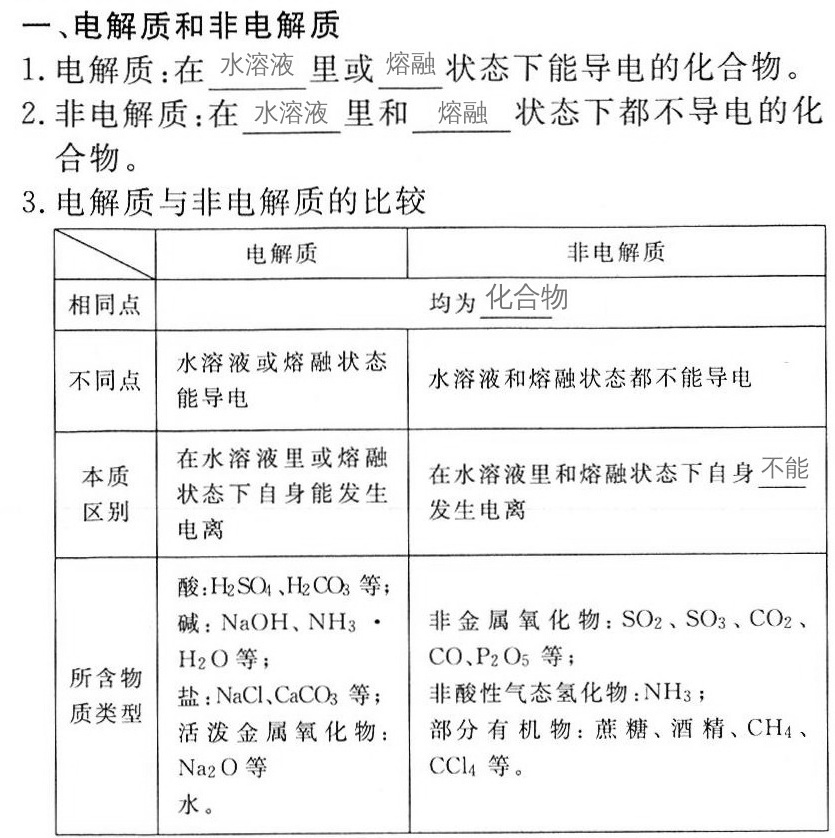
解析
本题考查电解质与非电解质的基本概念及比较,需掌握以下关键点:
- 电解质:必须是化合物,且在水溶液或熔融状态下自身能导电。
- 非电解质:必须是化合物,且在水溶液和熔融状态下均不能自身导电。
- 核心区别:是否能通过自身电离产生离子或H⁺、OH⁻。
1. 电解质的定义
关键:化合物在特定状态下导电且必须是自身电离。
答案:水溶液里或熔融状态下能导电的化合物。
2. 非电解质的定义
关键:化合物在两种状态下均不能自身导电。
答案:水溶液里和熔融状态下都不导电的化合物。
3. 电解质与非电解质的比较
相同点
均为化合物(本质属性)。
不同点
- 导电条件:电解质需水溶液或熔融状态,非电解质两种状态均不能导电。
- 本质区别:电解质能自身电离,非电解质不能。
物质类型
- 电解质:酸(如H₂SO₄)、碱(如NaOH)、盐(如NaCl)、活泼金属氧化物(如Na₂O)、水(H₂O)。
- 非电解质:非酸性气态氢化物(如NH₃)、非金属氧化物(如CO₂)、部分有机物(如蔗糖)。