题目
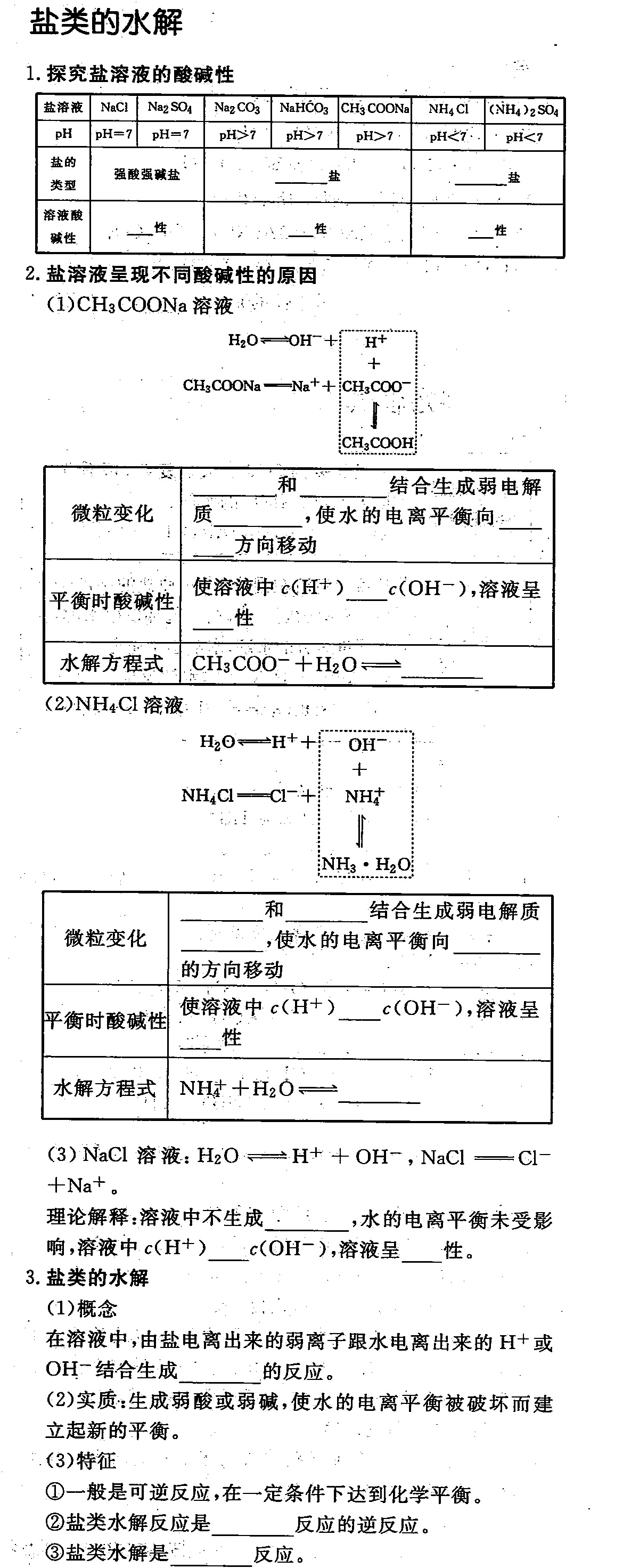
1.探究盐溶液的酸碱性-|||-盐溶液 NaCl Na2SO4 Na2CO3 NaHCO3 CH3COONa NH4Cl (NH4)2SO4-|||-pH =7 i =7 i gt 7 gt 7 i gt 7 i lt 7 .pH
题目解答
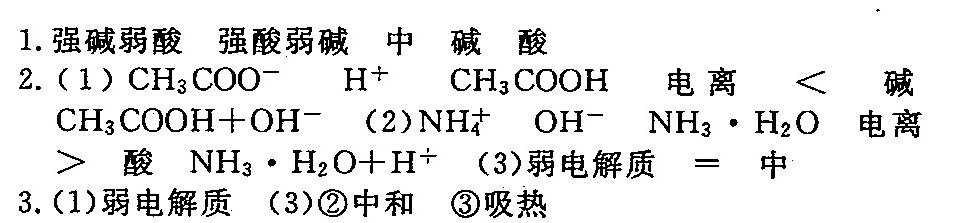
答案
解析
题目1:盐溶液的酸碱性及类型
- 盐的类型判断:根据盐的组成,NaCl、Na₂SO₄由强酸(HCl、H₂SO₄)和强碱(NaOH)组成,属于强酸强碱盐;Na₂CO₃、NaHCO₃、CH₃COONa由强碱(NaOH)和弱酸(H₂CO₃、CH₃COOH)组成,属于强碱弱酸盐;NH₄Cl、(NH₄)₂SO₄由强酸(HCl、H₂SO₄)和弱碱(NH₃·H₂O)组成,属于强酸弱碱盐。
- 溶液酸碱性:强酸强碱盐(如NaCl、Na₂SO₄)溶液中,阴阳离子均不水解,水的电离平衡未受影响,c(H⁺)=c(OH⁻),溶液呈中性;强碱弱酸盐(如Na₂CO₃等)溶液中,弱酸根离子水解结合H⁺,促进水的电离,c(OH⁻)>c(H⁺),溶液呈碱性;强酸弱碱盐(如NH₄Cl等)溶液中,弱碱阳离子水解结合OH⁻,促进水的电离,c(H⁺)>c(OH⁻),溶液呈酸性。
题目2:盐溶液呈现不同酸碱性的原因
(1) CH₃COONa溶液(强碱弱酸盐)
- 微粒变化:CH₃COONa电离出的CH₃COO⁻与水电离出的H⁺结合生成弱电解质CH₃COOH,使水的电离平衡(H₂O⇌H⁺+OH⁻)向电离方向移动(促进电离)。
- 平衡时酸碱性:溶液中c(OH⁻)>c(H⁺),呈碱性。
- 水解方程式:CH₃COO⁻+H₂O⇌CH₃COOH+OH⁻。
(2) NH₄Cl溶液(强酸弱碱盐)
- 微粒变化:NH₄Cl电离出的NH₄⁺与水电离出的OH⁻结合生成弱电解质NH₃·H₂O,使水的电离平衡向电离方向移动(促进电离)。
- 平衡时酸碱性:溶液中c(H⁺)>c(OH⁻),呈酸性。
- 水解方程式:NH₄⁺+H₂O⇌NH₃·H₂O+H⁺。
(3) NaCl溶液(强酸强碱盐)
- 理论解释:NaCl电离出的Na⁺和Cl⁻均不与水电离出的H⁺或OH⁻结合生成弱电解质,水的电离平衡未受影响,c(H⁺)=c(OH⁻),溶液呈中性。
题目3:盐类的水解
- 概念:在溶液中,由盐电离出来的弱离子跟水电离出来的H⁺或OH⁻结合生成弱电解质的反应。
- 特征:
② 盐类水解是中和反应的逆反应(中和反应:酸+碱→盐+水;水解反应:盐+水⇌酸+碱)。
③ 盐类水解是吸热反应(中和反应放热,逆反应吸热)。