题目
97.11℃时,含3% 乙醇水溶液的蒸气压为p,该温下纯水的蒸气压为0.901p,计算97.11℃时,在乙醇摩尔分数为0.02的水溶液上面乙醇和水的蒸气压各是多少?
97.11℃时,含3% 乙醇水溶液的蒸气压为p,该温下纯水的蒸气压为0.901p,
计算97.11℃时,在乙醇摩尔分数为0.02的水溶液上面乙醇和水的蒸气压各是多少?
题目解答
答案
解: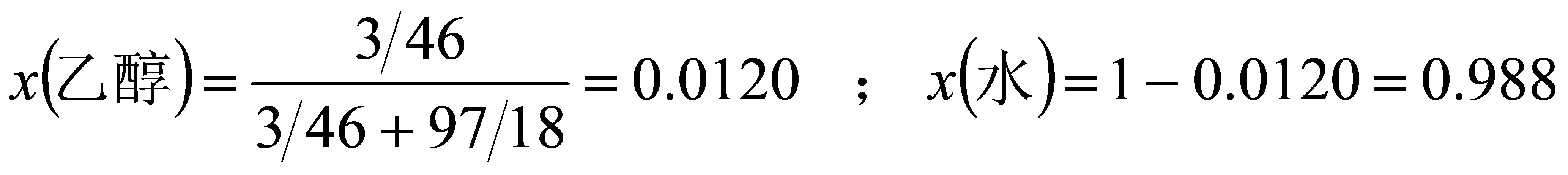
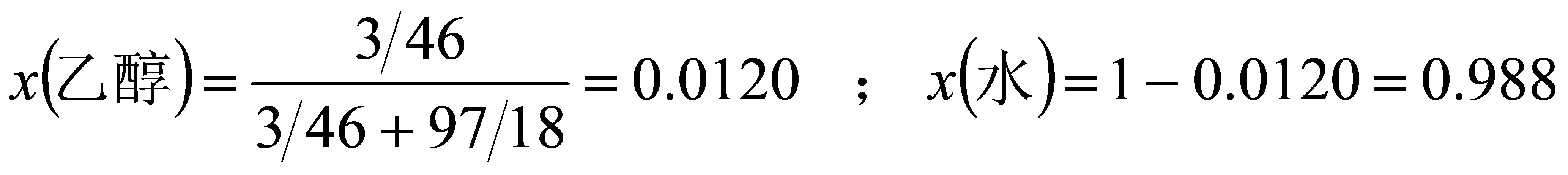
p = p*·x(水) + KH·x(乙) = 0.901 × 0.988 + KH × 0.0120 = 1.0
KH = 9.15 p,当 x(乙) = 0.02 ,x(水) = 0.98 时
p(乙) = 9.15 × 0.02 = 0.183 p, p(水) = 0.902 × 0.98 = 0.883 p
解析
步骤 1:计算乙醇的摩尔分数
根据题目,含3%乙醇水溶液的蒸气压为p,该温下纯水的蒸气压为0.901p。首先,需要计算乙醇的摩尔分数。乙醇的摩尔分数可以通过乙醇的质量分数和水的摩尔质量来计算。
步骤 2:计算乙醇和水的蒸气压
根据拉乌尔定律,溶液的蒸气压等于各组分的蒸气压乘以其摩尔分数。因此,可以计算出乙醇和水的蒸气压。
步骤 3:计算乙醇摩尔分数为0.02时的蒸气压
根据步骤2的结果,可以计算出乙醇摩尔分数为0.02时的蒸气压。
根据题目,含3%乙醇水溶液的蒸气压为p,该温下纯水的蒸气压为0.901p。首先,需要计算乙醇的摩尔分数。乙醇的摩尔分数可以通过乙醇的质量分数和水的摩尔质量来计算。
步骤 2:计算乙醇和水的蒸气压
根据拉乌尔定律,溶液的蒸气压等于各组分的蒸气压乘以其摩尔分数。因此,可以计算出乙醇和水的蒸气压。
步骤 3:计算乙醇摩尔分数为0.02时的蒸气压
根据步骤2的结果,可以计算出乙醇摩尔分数为0.02时的蒸气压。