题目
下列关于判断过程的方向的说法正确的是( )A. 所有自发进行的化学反应都是放热反应B. 高温高压下可以使石墨转化为金刚石是自发的化学反应C. 由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程D. 同一物质的固、液、气三种状态的熵值相同
下列关于判断过程的方向的说法正确的是( )
A. 所有自发进行的化学反应都是放热反应
B. 高温高压下可以使石墨转化为金刚石是自发的化学反应
C. 由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
D. 同一物质的固、液、气三种状态的熵值相同
A. 所有自发进行的化学反应都是放热反应
B. 高温高压下可以使石墨转化为金刚石是自发的化学反应
C. 由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
D. 同一物质的固、液、气三种状态的熵值相同
题目解答
答案
C
解:在给定的条件下,无须外界做功,一经引发即能自动进行的化学反应,为自发反应.从热力学上判断就是: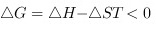 .
.
A.反应能否自发取决于焓变和熵变的复合判据,对于吸热反应,在一定温度下也能进行,故A错误;
B、C(石墨)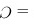 (金刚石);通常状况下
(金刚石);通常状况下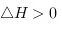 ,
,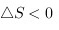 ,反应是不自发的,而且将金刚石加热到
,反应是不自发的,而且将金刚石加热到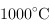 可以变成石墨.故B错误;
可以变成石墨.故B错误;
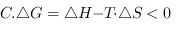 时,反应能自发进行,适合于所有的过程,所以C选项是正确的;
时,反应能自发进行,适合于所有的过程,所以C选项是正确的;
D.同一物质的固、液、气三种状态的熵值依次增大,故D错误;
所以C选项是正确的.
解:在给定的条件下,无须外界做功,一经引发即能自动进行的化学反应,为自发反应.从热力学上判断就是:
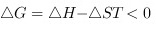 .
.A.反应能否自发取决于焓变和熵变的复合判据,对于吸热反应,在一定温度下也能进行,故A错误;
B、C(石墨)
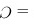 (金刚石);通常状况下
(金刚石);通常状况下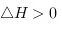 ,
,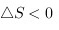 ,反应是不自发的,而且将金刚石加热到
,反应是不自发的,而且将金刚石加热到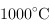 可以变成石墨.故B错误;
可以变成石墨.故B错误;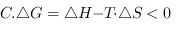 时,反应能自发进行,适合于所有的过程,所以C选项是正确的;
时,反应能自发进行,适合于所有的过程,所以C选项是正确的;D.同一物质的固、液、气三种状态的熵值依次增大,故D错误;
所以C选项是正确的.
解析
本题考查化学反应方向的判据,核心在于理解焓变(ΔH)和熵变(ΔS)的复合判据。正确选项需满足以下条件:
- 自发反应的判断需综合考虑ΔH和ΔS,而非单一因素;
- 熵变与物质状态的关系(固态 < 液态 < 气态);
- 复合判据(ΔG = ΔH - TΔS)的适用性。
选项A
错误。自发反应的判断需结合ΔH和ΔS,吸热反应在特定条件下也可能自发进行(如熔化、溶解等)。例如,冰在室温下熔化是吸热反应,但因熵增显著而自发。
选项B
错误。石墨转化为金刚石的反应(C(石墨) → C(金刚石))在常温下ΔH > 0且ΔS < 0,导致ΔG > 0,反应非自发。即使高温高压下转化,也需外界做功,仍为非自发过程。
选项C
正确。复合判据(ΔG = ΔH - TΔS)综合了焓变和熵变,适用于所有过程的方向判断。当ΔG < 0时,反应自发;ΔG = 0时达平衡;ΔG > 0时非自发。
选项D
错误。同一物质的熵值随状态变化而增大:固态 < 液态 < 气态。例如,H₂O(s) → H₂O(l) → H₂O(g),熵值逐渐增大。