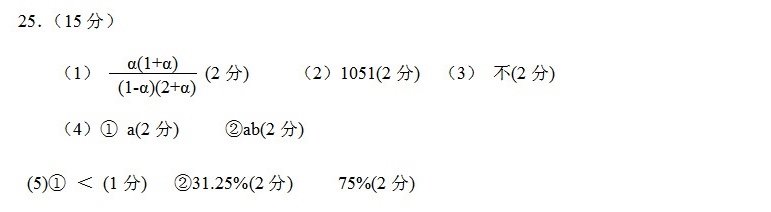题目
25.(15分)天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料-|||-和化工原料。回答下列问题:-|||-(1)乙烷在一定条件可发生如下反应: _(2)(H)_(6)(g)leftharpoons (C)_(2)(H)_(4)(g)+(H)_(2)(g)2L 密闭容-|||-器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平-|||-衡转化率为α。反应的平衡常数 _(x)= __ 用物质的量分数代替平衡-|||-浓度计算)。-|||-(2)已知反应 (O)_(3)(s)=CaO(s)+C(O)_(2)(g) Delta H(20g1)=+1788.2kJcdot mo(l)^-1-|||-Delta S(298k)=+169.61.mo(l)^-1cdot (k)^-1 则该反应能自发进行的最低温度为-|||-__ 假设反应的焓变与熵变不随温度变化而变化,结果保留整数)。-|||-(3)恒温条件下,在体积可变的密闭容器中发生反应 (g)+2(H)_(2)(g)leftharpoons -|||-CH3OH(g),达到平衡时,测得CO、H 2、CH3OH分别为1mol、1 mol、1mol,容器-|||-的体积为3L。再往容器中通入3molCO,此时平衡将 __ 移动(填"向-|||-右"、"向左"或"不")。-|||-(4)工业合成氨中制取氢气的原理如下:-|||-1:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.4kJ·mol^(-1)-|||-Ⅱ:CO(g)+H2O(g)=CO2(g)+H 2(g) △H=-41.2kJ·mol^(-1)-|||-①对于反应I,一定可以提高平衡体系中H2百分含量,又能加快反应速率的-|||-是 __ 填字母)。-|||-a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强-|||-②下列措施可以提高CH4转化率的是 __ 填字母)。-|||-a.适当升高温度-|||-b.将H2从反应体系中分离出来-|||-c.保持体积不变充入He,使体系总压强增大-|||-d.按原比例再充入CH4(g)和H2O(g)-|||-(5)乙烯(C2H4)是重要的化工原料,∠M(C2H2)选择性加氢合成乙烯是科学家-|||-当前关注的热点。70 ℃时,反应 _(2)(H)_(2)(g)+(H)_(2)(g)leftharpoons (C)_(2)(H)_(4)(g) Delta H=-|||-cdot mo(L)^-1 在刚性容器中达到平衡。-|||-①测得在某催化剂上生成乙烯速率方程为 =0.585([ p({C)_(2)(H)_(2))] }^-0.36-|||-p(H2)]^8,y(H2)一定时,若 _(1)((C)_(2)(H)_(2))gt (P)_(2)((C)_(2)(H)_(2)), 则V1 V2(填-|||-__-|||-">""

题目解答
答案