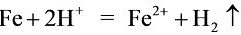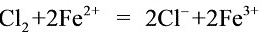(10分)铁是人类较早使用的金属之一。运用所学知识,回答下列问题。(1)鉴别Fe(OH)3胶体和FeCl3溶液最好的方法是__________________(写出具体实验操作,结论)。(2)电子工业用FeCl3溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________。C.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移电子数为4NAD.22.4L的CO气体与1molN2所含的电子数为14NA7、下列物质的分类合理的是A.碱性氧化物:Na2O、CaO、Mn2O7、Al2O3B.氧化物:CO2、NO、SO2、H2OC.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2OD.碱:NaOH、KOH、Ba(OH)2、Na2CO38、 “安全无小事”,对危险化学品要在包装标签上印有警示性标志。高锰酸钾(KMnO4)应选用的标志是A. B. C. D.9、设NA表示阿伏加德罗常数,下列说法正确的是A.1 mol氦气中有2NA个氦原子B.2 L 0.3 mol·L-1Na2SO4溶液中含0.6NA个Na+C.14 g氮气中含NA个氮原子D.18 g水中所含的电子数为8NA10、用NA表示阿伏加德罗常数的值,下列叙述正确的是A.1mol 铁和高温水蒸气完全反应转移的电子数为3NAB.常温常压下,1mol 氦气含有的原子数为NAC.标准状况下,11. 2 L 乙醇含有的分子数目为0. 5NAD.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA11、在无色溶液中加入适量 Na2O2后仍能大量共存的离子组是( )A.MnO、Ba2+、Cl-、NOB.Na+、Cl-、 CO、HCOC.a2+、Mg2+、NO、COD.K+、OH-、Cl-、SO12、用H3PO2将溶液中的银离子还原为银单质,该反应中氧化剂与还原剂的物质的量之比为4:1,则氧化产物为A.PH3 B.H3PO3 C.P D.H3PO413、有600mL某种混合物溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现将此溶液分成三等份,进行如下实验:(1)向第一份中加入AgNO3溶液,有沉淀产生;(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是______。②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得到21.525g白色沉淀。则溶液中c(Cl-)=______ mol∙L−1。③验证该溶液中是否含有Fe2+,正确的实验方法是______(填序号)。A.观察溶液是否呈浅绿色B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+C.试管中加入待测液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:①滤渣C中物质的化学式为______。②加过量D发生反应的离子方程式为__________________。③通入F发生反应的离子方程式为__________________。.
(10分)铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液最好的方法是__________________(写出具体实验操作,结论)。
(2)电子工业用FeCl3溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________。
C.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移电子数为4NA
D.22.4L的CO气体与1molN2所含的电子数为14NA
7、下列物质的分类合理的是
A.碱性氧化物:Na2O、CaO、Mn2O7、Al2O3
B.氧化物:CO2、NO、SO2、H2O
C.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2O
D.碱:NaOH、KOH、Ba(OH)2、Na2CO3
8、 “安全无小事”,对危险化学品要在包装标签上印有警示性标志。高锰酸钾(KMnO4)应选用的标志是
A. B.
B. C.
C. D.
D.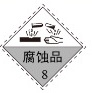
9、设NA表示阿伏加德罗常数,下列说法正确的是
A.1 mol氦气中有2NA个氦原子
B.2 L 0.3 mol·L-1Na2SO4溶液中含0.6NA个Na+
C.14 g氮气中含NA个氮原子
D.18 g水中所含的电子数为8NA
10、用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol 铁和高温水蒸气完全反应转移的电子数为3NA
B.常温常压下,1mol 氦气含有的原子数为NA
C.标准状况下,11. 2 L 乙醇含有的分子数目为0. 5NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
11、在无色溶液中加入适量 Na2O2后仍能大量共存的离子组是( )
A.MnO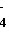 、Ba2+、Cl-、NO
、Ba2+、Cl-、NO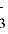
B.Na+、Cl-、 CO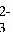 、HCO
、HCO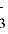
C.a2+、Mg2+、NO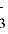 、CO
、CO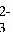
D.K+、OH-、Cl-、SO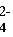
12、用H3PO2将溶液中的银离子还原为银单质,该反应中氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
A.PH3 B.H3PO3 C.P D.H3PO4
13、有600mL某种混合物溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现将此溶液分成三等份,进行如下实验:
(1)向第一份中加入AgNO3溶液,有沉淀产生;
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是______。
②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得到21.525g白色沉淀。则溶液中c(Cl-)=______ mol∙L−1。
③验证该溶液中是否含有Fe2+,正确的实验方法是______(填序号)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.试管中加入待测液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
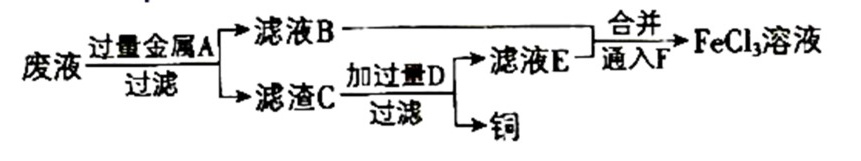
①滤渣C中物质的化学式为______。
②加过量D发生反应的离子方程式为__________________。
③通入F发生反应的离子方程式为__________________。
.题目解答
答案
[答案]用一束光照射两种溶液,出现光亮通路的是Fe(OH)3胶体,不出现光亮通路的是FeCl3溶液 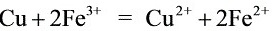 Fe3+、Cu2+、Fe2+ 3 B Fe、Cu
Fe3+、Cu2+、Fe2+ 3 B Fe、Cu