题目
利用下图所示仪器、试剂及其他必要物品进行实验并利用下图所示仪器、试剂及其他必要物品进行实验并利用下图所示仪器、试剂及其他必要物品进行实验并
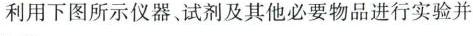

题目解答
答案


解析
步骤 1:实验现象对比
将少量二氧化锰加入盛有过氧化氢溶液的试管中,会迅速产生大量氧气,因为二氧化锰作为催化剂,会立即加速过氧化氢的分解。而将过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中,氧气的产生会随着过氧化氢溶液的加入而逐渐产生,这样可以得到平稳的氧气流。
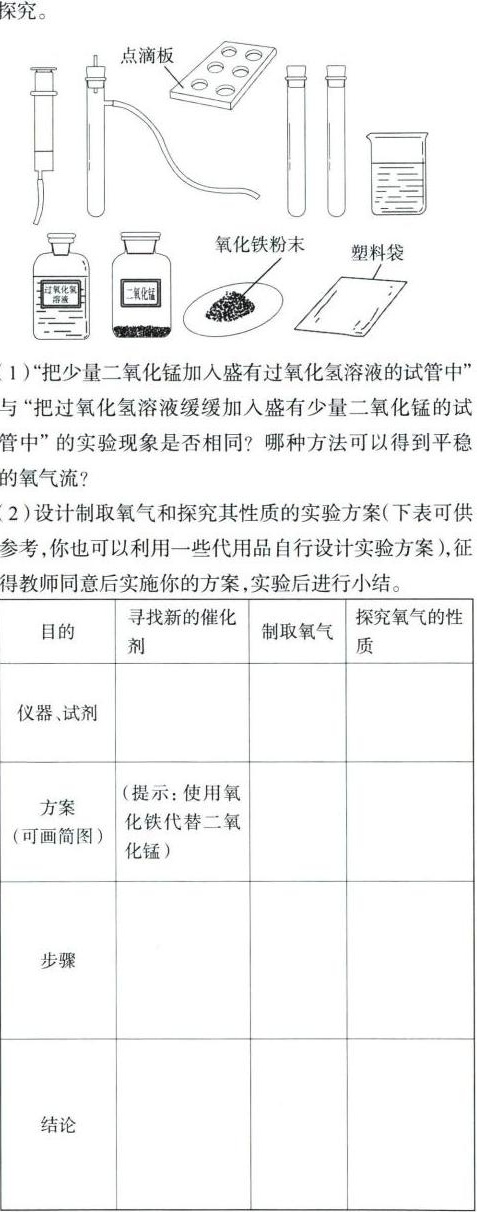
步骤 2:制取氧气和探究其性质的实验方案
1. 制取氧气
仪器、试剂:过氧化氢溶液、二氧化锰、试管、橡胶塞、导管、集气瓶、水槽。
步骤:将少量二氧化锰加入试管中,然后缓缓加入过氧化氢溶液,用橡胶塞塞紧试管,将导管插入集气瓶中,集气瓶中装满水,倒置在水槽中,收集氧气。
结论:过氧化氢在二氧化锰的催化下分解产生氧气。
2. 探究氧气的性质
仪器、试剂:氧气、木炭、燃烧匙。
步骤:将烧红的木炭伸入盛满氧气的集气瓶中。
结论:氧气的化学性质比较活泼,可以支持燃烧。
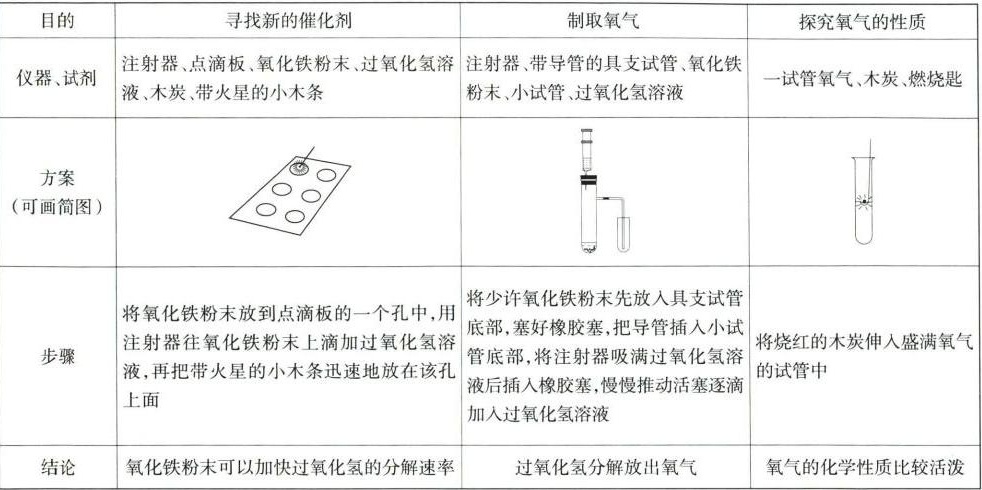
3. 寻找新的催化剂
仪器、试剂:氧化铁粉末、过氧化氢溶液、点滴板。
步骤:将氧化铁粉末放到点滴板的一个孔中,用注射器往氧化铁粉末上滴加过氧化氢溶液,再把带火星的小木条迅速地放在该孔上面。
结论:氧化铁粉末可以加快过氧化氢的分解速率,可以作为过氧化氢分解的催化剂。
步骤 3:制取氧气的方法
1. 过氧化氢氧化铁水+氧气
2. 过氧化氢氧化铜水+氧气
3. 过氧化氢硫酸铜水+氧气
4. 过氧化氢二氧化锰水+氧气
5. 高锰酸钾加热,锰酸钾+二氧化锰+氧气
6. 氯酸钾二氯化锰氯化钾+氧气
7. 水通电,氢气+氧气
将少量二氧化锰加入盛有过氧化氢溶液的试管中,会迅速产生大量氧气,因为二氧化锰作为催化剂,会立即加速过氧化氢的分解。而将过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中,氧气的产生会随着过氧化氢溶液的加入而逐渐产生,这样可以得到平稳的氧气流。
步骤 2:制取氧气和探究其性质的实验方案
1. 制取氧气
仪器、试剂:过氧化氢溶液、二氧化锰、试管、橡胶塞、导管、集气瓶、水槽。
步骤:将少量二氧化锰加入试管中,然后缓缓加入过氧化氢溶液,用橡胶塞塞紧试管,将导管插入集气瓶中,集气瓶中装满水,倒置在水槽中,收集氧气。
结论:过氧化氢在二氧化锰的催化下分解产生氧气。
2. 探究氧气的性质
仪器、试剂:氧气、木炭、燃烧匙。
步骤:将烧红的木炭伸入盛满氧气的集气瓶中。
结论:氧气的化学性质比较活泼,可以支持燃烧。
3. 寻找新的催化剂
仪器、试剂:氧化铁粉末、过氧化氢溶液、点滴板。
步骤:将氧化铁粉末放到点滴板的一个孔中,用注射器往氧化铁粉末上滴加过氧化氢溶液,再把带火星的小木条迅速地放在该孔上面。
结论:氧化铁粉末可以加快过氧化氢的分解速率,可以作为过氧化氢分解的催化剂。
步骤 3:制取氧气的方法
1. 过氧化氢氧化铁水+氧气
2. 过氧化氢氧化铜水+氧气
3. 过氧化氢硫酸铜水+氧气
4. 过氧化氢二氧化锰水+氧气
5. 高锰酸钾加热,锰酸钾+二氧化锰+氧气
6. 氯酸钾二氯化锰氯化钾+氧气
7. 水通电,氢气+氧气