题目
某化学兴趣小组为了探究在相同条件下,草酸根(C2(O)_(4)^2-)的还原性是否强于Fe2+,进行了如下三个实验。【实验1】通过Fe3+和C2(O)_(4)^2-在溶液中的反应比较Fe2+和C2(O)_(4)^2-的还原性强弱。实验操作与现象如下:在避光处,向10mL0.5mol⋅L-1FeCl3溶液中缓慢加入0.5mol⋅L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色溶液a待用。已知:Ⅰ.草酸 (H2C2O4)为二元弱酸。Ⅱ.三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2(O)_(4)^2- K=6.3×10-21。请回答:(1)实验室配制FeCl3溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请用离子方程式说明原因 ____ 。(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是 ____ 。(3)经检验,翠绿色晶体为K3Fe(C2O4)3⋅3H2O。为了确认实验1中是否发生了氧化还原反应,取少量翠绿色溶液a,向其中滴加 ____ (填序号)末见明显现象。A.少量KSCN溶液B.少量K3[Fe(CN)6]溶液C.少量HCl溶液该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因 ____ 。【实验2】通过比较H2O2与Fe2+、C2(O)_(4)^2-反应的难易,判断二者还原性的强弱。实验操作与现象如下:①向1mL0.5mol⋅L-1FeSO4溶液中加入1mL0.5mol⋅L-1K2C2O4溶液,过滤,立即产生黄色沉淀;②洗涤①中的黄色沉淀(已知:FeC2O4⋅2H2O为黄色固体,微溶于水,可溶于强酸),向其中加入过量的6%H2O2溶液,振荡,静置,反应剧烈放热,产生大量的红褐色沉淀和无色气体;③待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。请回答:(4)证明Fe2+被氧化的实验现象是 ____ 。(5)以上现象能否说明C2(O)_(4)^2-没有被氧化。请判断并说明理由: ____ 。【实验3】利用电化学装置进行实验,其装置如图:G 盐桥-|||-石墨 石墨-|||-6-|||-.5molcdot (L)^-1 0.5mol·L^(-1)-|||-FeCl3溶液 K2C2O4溶液(6)用FeCl3溶液、K2C2O4溶液和其他试剂,设计图的装置进行实验比较Fe2+和C2(O)_(4)^2-的还原性强弱,一段时间的实验后,该小组依据实验所观察到的现象做出了C2(O)_(4)^2-比Fe2+还原性强的实验结论。则下列实验现象描述能支持这一结论的有: ____ 。(填序号)A.电流表指针发生偏转B.取左侧烧杯内溶液滴加氢氧化钠溶液,出现红褐色沉淀C.取左侧烧杯内溶液滴加K3[Fe(CN)6]溶液,有蓝色沉淀生成D.右侧烧杯的电极附近有无色气泡生成,经实验,该气体能使澄清石灰水变浑浊。
某化学兴趣小组为了探究在相同条件下,草酸根(C2${O}_{4}^{2-}$)的还原性是否强于Fe2+,进行了如下三个实验。
【实验1】通过Fe3+和C2${O}_{4}^{2-}$在溶液中的反应比较Fe2+和C2${O}_{4}^{2-}$的还原性强弱。实验操作与现象如下:
在避光处,向10mL0.5mol⋅L-1FeCl3溶液中缓慢加入0.5mol⋅L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色溶液a待用。
已知:Ⅰ.草酸 (H2C2O4)为二元弱酸。
Ⅱ.三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$ K=6.3×10-21。
请回答:
(1)实验室配制FeCl3溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请用离子方程式说明原因 ____ 。
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是 ____ 。
(3)经检验,翠绿色晶体为K3Fe(C2O4)3⋅3H2O。为了确认实验1中是否发生了氧化还原反应,取少量翠绿色溶液a,向其中滴加 ____ (填序号)末见明显现象。
A.少量KSCN溶液
B.少量K3[Fe(CN)6]溶液
C.少量HCl溶液
该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因 ____ 。
【实验2】通过比较H2O2与Fe2+、C2${O}_{4}^{2-}$反应的难易,判断二者还原性的强弱。实验操作与现象如下:
①向1mL0.5mol⋅L-1FeSO4溶液中加入1mL0.5mol⋅L-1K2C2O4溶液,过滤,立即产生黄色沉淀;
②洗涤①中的黄色沉淀(已知:FeC2O4⋅2H2O为黄色固体,微溶于水,可溶于强酸),向其中加入过量的6%H2O2溶液,振荡,静置,反应剧烈放热,产生大量的红褐色沉淀和无色气体;
③待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。
请回答:
(4)证明Fe2+被氧化的实验现象是 ____ 。
(5)以上现象能否说明C2${O}_{4}^{2-}$没有被氧化。请判断并说明理由: ____ 。
【实验3】利用电化学装置进行实验,其装置如图:
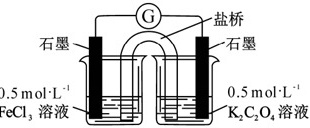
(6)用FeCl3溶液、K2C2O4溶液和其他试剂,设计图的装置进行实验比较Fe2+和C2${O}_{4}^{2-}$的还原性强弱,一段时间的实验后,该小组依据实验所观察到的现象做出了C2${O}_{4}^{2-}$比Fe2+还原性强的实验结论。则下列实验现象描述能支持这一结论的有: ____ 。(填序号)
A.电流表指针发生偏转
B.取左侧烧杯内溶液滴加氢氧化钠溶液,出现红褐色沉淀
C.取左侧烧杯内溶液滴加K3[Fe(CN)6]溶液,有蓝色沉淀生成
D.右侧烧杯的电极附近有无色气泡生成,经实验,该气体能使澄清石灰水变浑浊。
【实验1】通过Fe3+和C2${O}_{4}^{2-}$在溶液中的反应比较Fe2+和C2${O}_{4}^{2-}$的还原性强弱。实验操作与现象如下:
在避光处,向10mL0.5mol⋅L-1FeCl3溶液中缓慢加入0.5mol⋅L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色溶液a待用。
已知:Ⅰ.草酸 (H2C2O4)为二元弱酸。
Ⅱ.三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$ K=6.3×10-21。
请回答:
(1)实验室配制FeCl3溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请用离子方程式说明原因 ____ 。
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是 ____ 。
(3)经检验,翠绿色晶体为K3Fe(C2O4)3⋅3H2O。为了确认实验1中是否发生了氧化还原反应,取少量翠绿色溶液a,向其中滴加 ____ (填序号)末见明显现象。
A.少量KSCN溶液
B.少量K3[Fe(CN)6]溶液
C.少量HCl溶液
该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因 ____ 。
【实验2】通过比较H2O2与Fe2+、C2${O}_{4}^{2-}$反应的难易,判断二者还原性的强弱。实验操作与现象如下:
①向1mL0.5mol⋅L-1FeSO4溶液中加入1mL0.5mol⋅L-1K2C2O4溶液,过滤,立即产生黄色沉淀;
②洗涤①中的黄色沉淀(已知:FeC2O4⋅2H2O为黄色固体,微溶于水,可溶于强酸),向其中加入过量的6%H2O2溶液,振荡,静置,反应剧烈放热,产生大量的红褐色沉淀和无色气体;
③待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。
请回答:
(4)证明Fe2+被氧化的实验现象是 ____ 。
(5)以上现象能否说明C2${O}_{4}^{2-}$没有被氧化。请判断并说明理由: ____ 。
【实验3】利用电化学装置进行实验,其装置如图:

(6)用FeCl3溶液、K2C2O4溶液和其他试剂,设计图的装置进行实验比较Fe2+和C2${O}_{4}^{2-}$的还原性强弱,一段时间的实验后,该小组依据实验所观察到的现象做出了C2${O}_{4}^{2-}$比Fe2+还原性强的实验结论。则下列实验现象描述能支持这一结论的有: ____ 。(填序号)
A.电流表指针发生偏转
B.取左侧烧杯内溶液滴加氢氧化钠溶液,出现红褐色沉淀
C.取左侧烧杯内溶液滴加K3[Fe(CN)6]溶液,有蓝色沉淀生成
D.右侧烧杯的电极附近有无色气泡生成,经实验,该气体能使澄清石灰水变浑浊。
题目解答
答案
解:(1)FeCl3为强酸弱碱盐,Fe3+水解生成红褐色Fe(OH)3,水解离子方程式为Fe3++3H2O⇌Fe(OH)3+3H+,所以实验室配制FeCl3溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,
故答案为:Fe3++3H2O⇌Fe(OH)3+3H+;
(2)Fe3+和KSCN反应生成络合物Fe(SCN)3而使溶液呈血红色,三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]在水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$,加入稀硫酸,C2${O}_{4}^{2-}$能和H+反应生成H2C2O4,使平衡正向移动,c(Fe3+)增大,遇KSCN溶液变红色,
故答案为:三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]在水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$,加入稀硫酸,强酸制取弱酸,C2${O}_{4}^{2-}$能和H+反应生成H2C2O4,使平衡正向移动,c(Fe3+)增大,遇KSCN溶液变红色;
(3)为了确认实验1中是否发生了氧化还原反应,实际上是Fe2+,Fe2+和铁氰化钾溶液反应生成蓝色沉淀,和KSCN溶液、KCl溶液不反应,所以可以用铁氰化钾溶液检验Fe2+;Fe3+和C2${O}_{4}^{2-}$反应生成稳定的[Fe(C2O4)3]3-,浓度降低,Fe3+ 的氧化性、C2${O}_{4}^{2-}$的还原性都减弱,所以氧化还原反应没有发生,
故答案为:B;Fe3+和C2${O}_{4}^{2-}$反应生成稳定的[Fe(C2O4)3]3-,浓度降低,Fe3+ 的氧化性、C2${O}_{4}^{2-}$的还原性都减弱;
(4)如果Fe2+被氧化,则生成Fe3+或[Fe(C2O4)3]3-,实验②中产生大量的红褐色沉淀、实验③得到翠绿色溶液,说明Fe2+被氧化生成Fe3+、[Fe(C2O4)3]3-,
故答案为:实验②中产生大量的红褐色沉淀、实验③得到翠绿色溶液;
(5)草酸根离子中C元素化合价为+3价,在反应中C元素失电子化合价升高才能说明草酸根离子被氧化,如果有+4价碳的化合物生成,才能说明C2${O}_{4}^{2-}$被氧化,根据实验现象无法判断是否有+4价碳的化合物生成,所以不能说明C2${O}_{4}^{2-}$是否被氧化,
故答案为:有+4价碳的化合物生成,才能说明C2${O}_{4}^{2-}$被氧化,根据实验现象无法判断是否有+4价碳的化合物生成,所以不能说明C2${O}_{4}^{2-}$是否被氧化;
(6)A.如果还原性Fe2+>C2${O}_{4}^{2-}$,该装置能自发进行氧化还原反应而构成原电池,放电时有电流产生,电流计指针偏转,故A正确;
B.如果能发生氧化还原反应而构成原电池,则Fe3+生成Fe2+,应该检验Fe2+,用铁氰化钾溶液检验,故B错误;
C.Fe2+和K3[Fe(CN)6]溶液反应生成蓝色沉淀,取左侧烧杯内溶液滴加K3[Fe(CN)6]溶液,有蓝色沉淀生成,说明有Fe2+生成,亚铁离子为还原产物,草酸根离子为还原剂,则还原性Fe2+>C2${O}_{4}^{2-}$,故C正确;
D.右侧烧杯的电极附近有无色气泡生成,该气体能使澄清石灰水变浑浊,说明有二氧化碳生成,C元素化合价由+3价变为+4价,草酸根离子为还原剂,亚铁离子为还原产物,则还原性Fe2+>C2${O}_{4}^{2-}$,故D正确;
故答案为:ACD。
故答案为:Fe3++3H2O⇌Fe(OH)3+3H+;
(2)Fe3+和KSCN反应生成络合物Fe(SCN)3而使溶液呈血红色,三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]在水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$,加入稀硫酸,C2${O}_{4}^{2-}$能和H+反应生成H2C2O4,使平衡正向移动,c(Fe3+)增大,遇KSCN溶液变红色,
故答案为:三水三草酸合铁酸钾[K3Fe(C2O4)3⋅3H2O]在水溶液中存在:[Fe(C2O4)3]3-⇌Fe3++3C2${O}_{4}^{2-}$,加入稀硫酸,强酸制取弱酸,C2${O}_{4}^{2-}$能和H+反应生成H2C2O4,使平衡正向移动,c(Fe3+)增大,遇KSCN溶液变红色;
(3)为了确认实验1中是否发生了氧化还原反应,实际上是Fe2+,Fe2+和铁氰化钾溶液反应生成蓝色沉淀,和KSCN溶液、KCl溶液不反应,所以可以用铁氰化钾溶液检验Fe2+;Fe3+和C2${O}_{4}^{2-}$反应生成稳定的[Fe(C2O4)3]3-,浓度降低,Fe3+ 的氧化性、C2${O}_{4}^{2-}$的还原性都减弱,所以氧化还原反应没有发生,
故答案为:B;Fe3+和C2${O}_{4}^{2-}$反应生成稳定的[Fe(C2O4)3]3-,浓度降低,Fe3+ 的氧化性、C2${O}_{4}^{2-}$的还原性都减弱;
(4)如果Fe2+被氧化,则生成Fe3+或[Fe(C2O4)3]3-,实验②中产生大量的红褐色沉淀、实验③得到翠绿色溶液,说明Fe2+被氧化生成Fe3+、[Fe(C2O4)3]3-,
故答案为:实验②中产生大量的红褐色沉淀、实验③得到翠绿色溶液;
(5)草酸根离子中C元素化合价为+3价,在反应中C元素失电子化合价升高才能说明草酸根离子被氧化,如果有+4价碳的化合物生成,才能说明C2${O}_{4}^{2-}$被氧化,根据实验现象无法判断是否有+4价碳的化合物生成,所以不能说明C2${O}_{4}^{2-}$是否被氧化,
故答案为:有+4价碳的化合物生成,才能说明C2${O}_{4}^{2-}$被氧化,根据实验现象无法判断是否有+4价碳的化合物生成,所以不能说明C2${O}_{4}^{2-}$是否被氧化;
(6)A.如果还原性Fe2+>C2${O}_{4}^{2-}$,该装置能自发进行氧化还原反应而构成原电池,放电时有电流产生,电流计指针偏转,故A正确;
B.如果能发生氧化还原反应而构成原电池,则Fe3+生成Fe2+,应该检验Fe2+,用铁氰化钾溶液检验,故B错误;
C.Fe2+和K3[Fe(CN)6]溶液反应生成蓝色沉淀,取左侧烧杯内溶液滴加K3[Fe(CN)6]溶液,有蓝色沉淀生成,说明有Fe2+生成,亚铁离子为还原产物,草酸根离子为还原剂,则还原性Fe2+>C2${O}_{4}^{2-}$,故C正确;
D.右侧烧杯的电极附近有无色气泡生成,该气体能使澄清石灰水变浑浊,说明有二氧化碳生成,C元素化合价由+3价变为+4价,草酸根离子为还原剂,亚铁离子为还原产物,则还原性Fe2+>C2${O}_{4}^{2-}$,故D正确;
故答案为:ACD。