题目
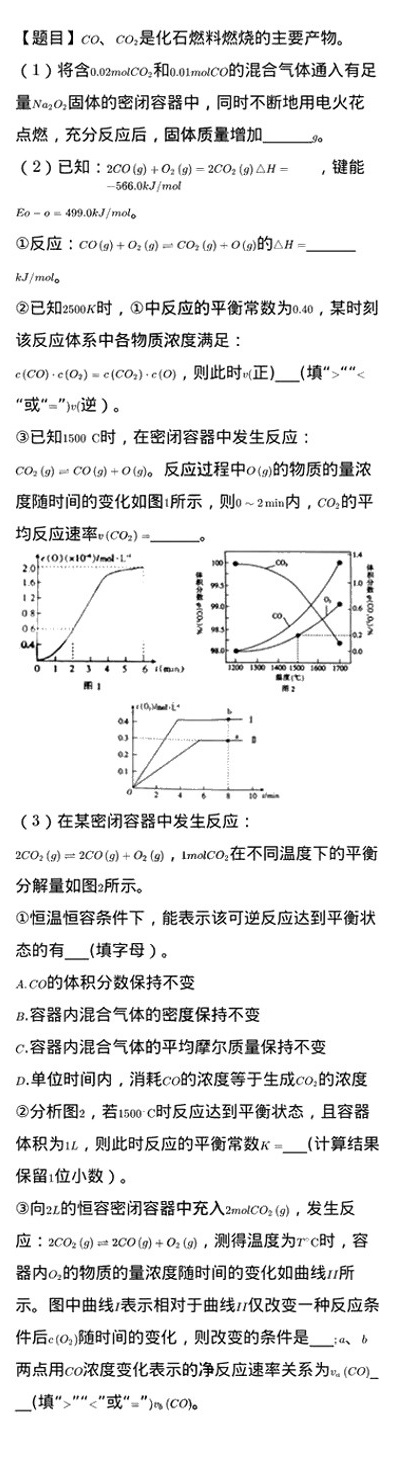
[题目]CO、CO2是化石燃料燃烧的主要产物。-|||-(1)将含0.02molCO2和0.01molCO的混合气体通入有足-|||-量Na2O2固体的密闭容器中,同时不断地用电火花-|||-点燃,充分反应后,固体质量增加 __ 。-|||-(2)已知: (g)+(O)_(2)(g)=2C(O)_(2)(g)Delta H=, 键能-|||--566.0km/mol-|||--0=499.0kg/mo(d)_(0)-|||-①反应: (g)+(O)_(2)(g)leftharpoons C(O)_(2)(g)+O(g) 的Delta H= __-|||-/mo(d)_(0)-|||-②已知2500K时,①中反应的平衡常数为0.40,某时刻-|||-该反应体系中各物质浓度满足:-|||-(CO)cdot c((O)_(2))=c(C(O)_(2))cdot c(O), 则此时v(正) __ (填">""<-|||-"或"=")v(逆)。-|||-③已知1500c时,在密闭容器中发生反应:-|||-(O)_(2)(g)=!=!= CO(g)+O(g) 反应过程中O(g)的物质的量浓-|||-度随时间的变化如图1所示,则 (log )_(2)n-2min 内,CO2的平-|||-均反应速率 (C(O)_(2))= __ _。-|||-1×(0)(x104)y=1.-|||-20 .00-|||-1.6-|||-12-|||-0 ∞、 e-|||-06-|||-a4 100-|||-o 2) 4 5 6 then 高南-|||-第1 at-|||-m:-|||-1400kmel →1-|||-04-|||-.-|||-0.-|||-(3)在某密闭容器中发生反应:-|||-(O)_(2)(g)leftharpoons 2CO(g)+(O)_(2)(g), 1molCO2在不同温度下的平衡-|||-分解量如图2所示。-|||-①恒温恒容条件下,能表示该可逆反应达到平衡状-|||-态的有 __ (填字母)。-|||-A.CO的体积分数保持不变-|||-B.容器内混合气体的密度保持不变-|||-C.容器内混合气体的平均摩尔质量保持不变-|||-D.单位时间内,消耗CO的浓度等于生成CO2的浓度-|||-②分析图2,若1500℃时反应达到平衡状态,且容器-|||-体积为1L,则此时反应的平衡常数 K=_ __ (计算结果-|||-保留1位小数)。-|||-③向2L的恒容密闭容器中充入2molCO2 (9),发生反-|||-应: (O)_(2)(g)=!=!= 2CO(g)+(O)_(2)(g), 测得温度为rc时,容-|||-器内O2的物质的量浓度随时间的变化如曲线u所-|||-示。图中曲线l表示相对于曲线∥仪改变一种反应条-|||-件后c(O2)随时间的变化,则改变的条件是 ___;a、b-|||-两点用co浓度变化表示的净反应速率关系为va(CO)
题目解答
答案
