题目
写出下列原子的基态光谱支项的符号:-|||-(1)Si,(2)Mn,(3)Br,(4)Nb,(5)Ni。

题目解答
答案

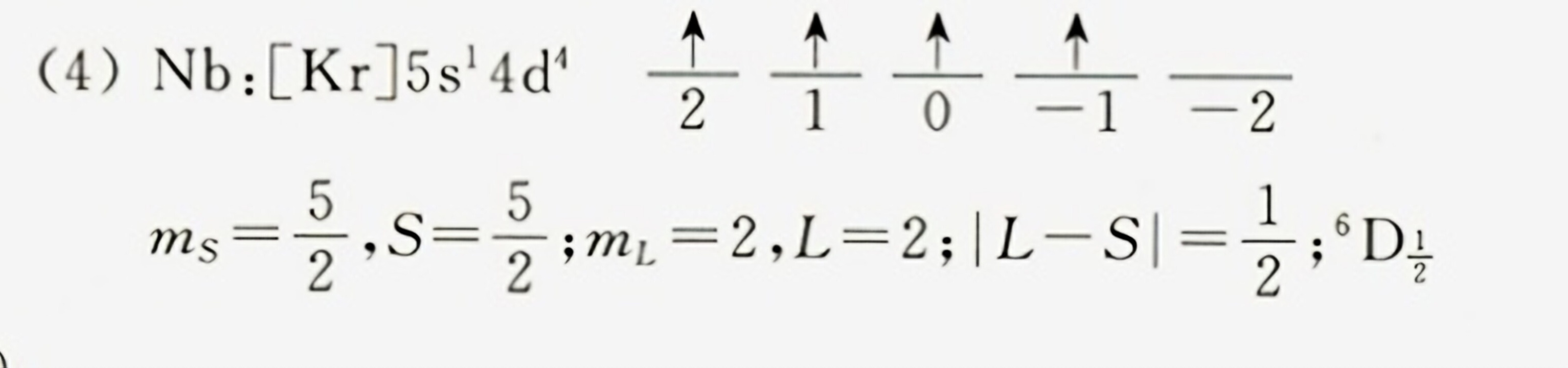
解析
基态原子的光谱支项符号由电子排布的自旋量子数S、轨道角动量量子数L和总角动量量子数J决定。解题核心在于:
- 写出基态电子排布式,特别关注价电子层;
- 应用Hund规则确定S和L:
- S:未配对电子数决定,$S = \frac{\text{未配对电子数}}{2}$;
- L:未配对电子的轨道角动量矢量和;
- 计算J:$J = |L-S|, |L-S+1|, \dots, L+S$,选择最稳定的支项(通常取$J$最大值)。
(1) Si(硅)
- 电子排布:$[{\rm Ne}]3s^2 3p^2$,3p²为价电子。
- Hund规则:p轨道有3个简并态,2个电子分占两轨道,自旋平行。
- S:未配对电子数为2,$S = \frac{2}{2} = 1$;
- L:两电子轨道角动量方向相同,$L = 1$(p轨道)。
- J:$J = L+S = 2$(最稳定)。
- 光谱支项:$^4P_2$(符号简写为$^4P$)。
(2) Mn(锰)
- 电子排布:$[{\rm Ar}]3d^5 4s^2$,3d⁵为价电子。
- Hund规则:d轨道有5个简并态,5个电子分占5轨道,自旋平行。
- S:未配对电子数为5,$S = \frac{5}{2}$;
- L:轨道角动量相互抵消,$L = 0$。
- J:$J = S = \frac{5}{2}$。
- 光谱支项:$^6S_{\frac{5}{2}}$。
(3) Br(溴)
- 电子排布:$[{\rm Ar}]4s^2 3d^{10} 4p^5$,4p⁵为价电子。
- Hund规则:p轨道填5个电子,3个轨道各填2、2、1电子。
- S:未配对电子数为1,$S = \frac{1}{2}$;
- L:单电子轨道角动量,$L = 1$(p轨道)。
- J:$J = L+S = \frac{3}{2}$。
- 光谱支项:$^2P_{\frac{3}{2}}$。
(4) Nb(铌)
- 电子排布:$[{\rm Kr}]4d^4 5s^1$,4d⁴为价电子。
- Hund规则:d轨道有4个电子分占4轨道,自旋平行。
- S:未配对电子数为4,$S = 2$;
- L:轨道角动量矢量和,$L = 2$(d轨道)。
- J:$J = |L-S| = \frac{1}{2}$(最稳定)。
- 光谱支项:$^5D_{\frac{1}{2}}$。
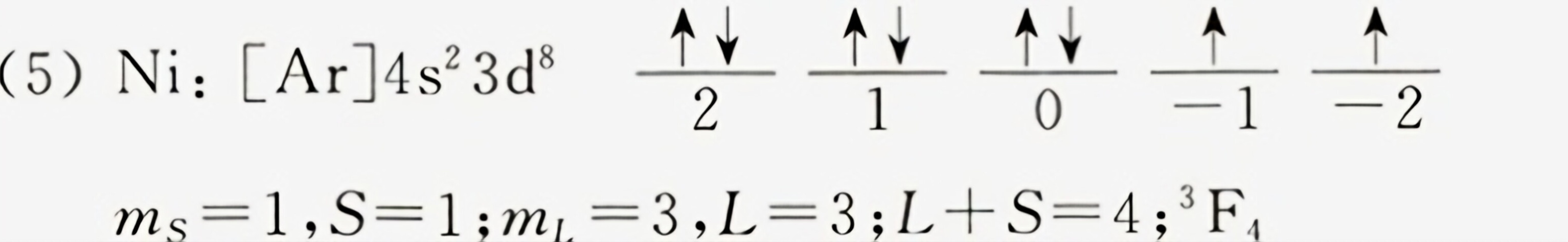
(5) Ni(镍)
- 电子排布:$[{\rm Ar}]3d^8 4s^2$,3d⁸为价电子。
- Hund规则:d轨道有8个电子,4对成对,1对未配对。
- S:未配对电子数为2,$S = 1$;
- L:轨道角动量矢量和,$L = 3$(d轨道)。
- J:$J = L+S = 4$(最稳定)。
- 光谱支项:$^3F_4$。