题目
某小组同学做镁在空气中燃烧的实验时,仔细观察发现生成物中有少许黑色固体,针对这一现象,进行了以下实验探究。 【探究目的】探究黑色固体是什么。 【实验一】镁带与氧气的反应 (一)制取氧气并探究氯酸钾和二氧化锰制氧气反应物与催化剂的最佳质量比。 实验中采用如图1、2所示装置,取10支试管,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所消耗的时间。实验数据如表: 实验编号 1 2 3 4 5 6 7 8 9 10 二氧化锰与氯酸钾的质量比 1:20 1:10 1:6 1:5 1:4 1:3 1:2 2:3 1:1 3:2 生成200mL氧气时间/秒 235 186 162 147 133 117 143 160 211 244 请回答下列问题: 氧化锰-|||-氯酸钾 氧化锰-|||-氯酸钾 (1)实验开始前应先 ___________ ; (2)为了完成本实验,方框内应选择图2气体收集装置中的 ___________ (填字母); (3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为 ___________ ;该反应的化学方程式为 ___________ 。 (二)燃烧镁带 将镁带打磨,点燃,伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。 (4)点燃前,用砂纸打磨镁带的目的是 ___________ 。 (5)写出该反应的化学方程式: ___________ 。 实验结论:镁与氧气反应生成白色的氧化镁。 【实验二】镁与氮气的反应 (一)获取氮气: 分离空气的常用方法有以下两种: 方法Ⅰ.将空气液化后再气化。 (6)液态空气气化时首先分离出氮气,则沸点:N 2 ___________ O 2(选填“高于”、“等于”或“低于”)。在此过程中,氧分子和氮分子 ___________ 改变(选填“发生”或“不发生”)。 方法Ⅱ.用碳分子筛分离。 资料:Ⅰ.碳分子筛对不同气体的吸附强度不同,由于氧分子通过碳分子筛微孔空隙的扩散速度比氮分子快得多。因此,当加压时它对氧优先吸附。 Ⅱ.气压越大,碳分子筛吸附能力越强,反之越弱; Ⅲ.碳分子筛可以再生,能重复使用。 (7)碳分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N 2 ___________ O 2(选填“大于”、“等于”或“小于”)。 (8)根据资料,碳分子筛再生的方法是 ___________ 。 (二)燃烧镁带 打磨镁带至光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。 实验结论:镁与氮气在点燃的条件下反应生成淡黄色的氮化镁(Mg 3N 2) 【实验三】镁与水蒸气的反应 实验装置如下图所示: 氧化锰-|||-氯酸钾 (9)实验开始时,应先点燃A处酒精灯,等观察到水沸腾后,再点燃B处酒精灯,这样做的目的是 ___________ ; 生成的气体通入肥皂液中,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是 ___________ ; 实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体 【探究结论】 根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应生成的,该黑色固体是 ___________ (写出化学式)。 【拓展探究】 把燃着的镁条插入二氧化碳的集气瓶中,发现在白烟中夹杂着大量黑色物质,该反应的化学方程式为 ___________ 。 【实验反思】 本探究活动同学们对可燃物的燃烧有了新的认识,燃烧 ___________ 需要氧气(填“一定”或“不一定”)
某小组同学做镁在空气中燃烧的实验时,仔细观察发现生成物中有少许黑色固体,针对这一现象,进行了以下实验探究。
【探究目的】探究黑色固体是什么。
【实验一】镁带与氧气的反应
(一)制取氧气并探究氯酸钾和二氧化锰制氧气反应物与催化剂的最佳质量比。
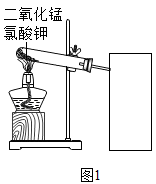
实验中采用如图1、2所示装置,取10支试管,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所消耗的时间。实验数据如表:
请回答下列问题:
(1)实验开始前应先
___________
;
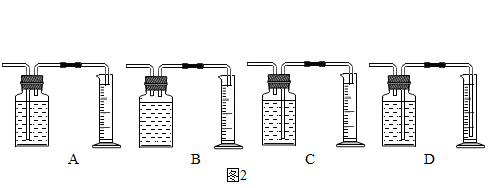
(2)为了完成本实验,方框内应选择图2气体收集装置中的
___________
(填字母);
(3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为
___________
;该反应的化学方程式为
___________
。
(二)燃烧镁带
将镁带打磨,点燃,伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
(4)点燃前,用砂纸打磨镁带的目的是
___________
。
(5)写出该反应的化学方程式:
___________
。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁与氮气的反应
(一)获取氮气:
分离空气的常用方法有以下两种:
方法Ⅰ.将空气液化后再气化。
(6)液态空气气化时首先分离出氮气,则沸点:N 2
___________
O
2(选填“高于”、“等于”或“低于”)。在此过程中,氧分子和氮分子
___________
改变(选填“发生”或“不发生”)。
方法Ⅱ.用碳分子筛分离。
资料:Ⅰ.碳分子筛对不同气体的吸附强度不同,由于氧分子通过碳分子筛微孔空隙的扩散速度比氮分子快得多。因此,当加压时它对氧优先吸附。
Ⅱ.气压越大,碳分子筛吸附能力越强,反之越弱;
Ⅲ.碳分子筛可以再生,能重复使用。
(7)碳分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N 2
___________
O
2(选填“大于”、“等于”或“小于”)。
(8)根据资料,碳分子筛再生的方法是
___________
。
(二)燃烧镁带
打磨镁带至光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
实验结论:镁与氮气在点燃的条件下反应生成淡黄色的氮化镁(Mg 3N 2)
【实验三】镁与水蒸气的反应
实验装置如下图所示:
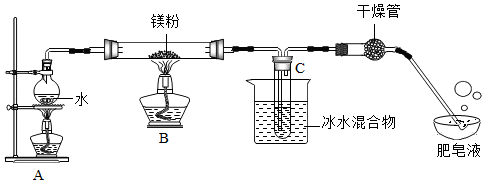
(9)实验开始时,应先点燃A处酒精灯,等观察到水沸腾后,再点燃B处酒精灯,这样做的目的是
___________
;
生成的气体通入肥皂液中,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是
___________
;
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体
【探究结论】
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应生成的,该黑色固体是
___________
(写出化学式)。
【拓展探究】
把燃着的镁条插入二氧化碳的集气瓶中,发现在白烟中夹杂着大量黑色物质,该反应的化学方程式为
___________
。
【实验反思】
本探究活动同学们对可燃物的燃烧有了新的认识,燃烧
___________
需要氧气(填“一定”或“不一定”)
【探究目的】探究黑色固体是什么。
【实验一】镁带与氧气的反应
(一)制取氧气并探究氯酸钾和二氧化锰制氧气反应物与催化剂的最佳质量比。
实验中采用如图1、2所示装置,取10支试管,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所消耗的时间。实验数据如表:
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
| 生成200mL氧气时间/秒 | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
请回答下列问题:


(1)实验开始前应先
(2)为了完成本实验,方框内应选择图2气体收集装置中的
(3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为
(二)燃烧镁带
将镁带打磨,点燃,伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
(4)点燃前,用砂纸打磨镁带的目的是
(5)写出该反应的化学方程式:
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁与氮气的反应
(一)获取氮气:
分离空气的常用方法有以下两种:
方法Ⅰ.将空气液化后再气化。
(6)液态空气气化时首先分离出氮气,则沸点:N 2
方法Ⅱ.用碳分子筛分离。
资料:Ⅰ.碳分子筛对不同气体的吸附强度不同,由于氧分子通过碳分子筛微孔空隙的扩散速度比氮分子快得多。因此,当加压时它对氧优先吸附。
Ⅱ.气压越大,碳分子筛吸附能力越强,反之越弱;
Ⅲ.碳分子筛可以再生,能重复使用。
(7)碳分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N 2
(8)根据资料,碳分子筛再生的方法是
(二)燃烧镁带
打磨镁带至光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
实验结论:镁与氮气在点燃的条件下反应生成淡黄色的氮化镁(Mg 3N 2)
【实验三】镁与水蒸气的反应
实验装置如下图所示:

(9)实验开始时,应先点燃A处酒精灯,等观察到水沸腾后,再点燃B处酒精灯,这样做的目的是
生成的气体通入肥皂液中,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体
【探究结论】
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应生成的,该黑色固体是
【拓展探究】
把燃着的镁条插入二氧化碳的集气瓶中,发现在白烟中夹杂着大量黑色物质,该反应的化学方程式为
【实验反思】
本探究活动同学们对可燃物的燃烧有了新的认识,燃烧
题目解答
答案
