题目
2.(1) Fe-Cu- 稀H2SO4组成的原电池中,负极反应为 __-|||-__ 正极反应为 __-|||-电池总反应为 口-|||-(2)由Pb、Cu与氯化铁溶液组成的原电池,其正极反应式-|||-为 __ 负极反应式为 __-|||-(3)由Al、Cu与浓硝酸组成的原电池,其负极反应式为-|||-__-|||-(4)与 (O)_(2)-Zn 电池类似, _(2)Fe(O)_(4)-Zn 也可以组成碱性电-|||-池,K2FeO4在电池中作为正极材料,其电极反应式为 __-|||-,-|||-该电池总反应的离子方程式为 __

题目解答
答案
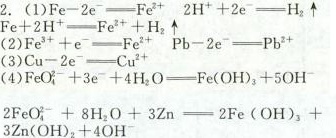
解析
原电池反应的核心思路:
- 判断正负极:根据材料的活动性,活泼金属作负极,较不活泼金属或溶液中的阳离子作正极。
- 书写电极反应:
- 负极:金属失电子发生氧化反应(如 $M - ne^- \rightarrow M^{n+}$)。
- 正极:溶液中阳离子得电子发生还原反应(如 $A^{m+} + e^- \rightarrow A^{(m-1)+}$)。
- 总反应:负极和正极反应相加,消去中间电子,注意溶液中 $H^+$、$OH^-$ 的参与。
关键点:
- 电解质溶液性质(如浓硝酸的钝化作用)。
- 离子氧化能力(如 $Fe^{3+}$ 比 $Cu^{2+}$ 更易被还原)。
第(1)题
材料:Fe(铁)、Cu(铜),电解质:稀硫酸。
- 负极(Fe):铁比铜活泼,铁失电子:
$Fe - 2e^- \rightarrow Fe^{2+}$ - 正极(Cu):溶液中 $H^+$ 得电子生成 $H_2$:
$2H^+ + 2e^- \rightarrow H_2 \uparrow$ - 总反应:两式相加,消去 $2e^-$:
$Fe + 2H^+ \rightarrow Fe^{2+} + H_2 \uparrow$
第(2)题
材料:Pb(铅)、Cu(铜),电解质:FeCl₃溶液。
- 正极(Cu):$Fe^{3+}$ 氧化能力比 $Cu^{2+}$ 强,$Fe^{3+}$ 得电子:
$Fe^{3+} + e^- \rightarrow Fe^{2+}$ - 负极(Pb):铅失电子:
$Pb - 2e^- \rightarrow Pb^{2+}$
第(3)题
材料:Al(铝)、Cu(铜),电解质:浓硝酸。
- 负极(Cu):浓硝酸使铝钝化(表面生成致密氧化膜),铜作负极:
$Cu - 2e^- \rightarrow Cu^{2+}$
第(4)题
材料:K₂FeO₄(正极)、Zn(负极),电解质:碱性溶液。
- 正极反应:$FeO_4^{2-}$ 得电子被还原:
$FeO_4^{2-} + 3e^- + 4H_2O \rightarrow Fe(OH)_3 + 5OH^-$ - 总反应:负极 $Zn$ 被氧化为 $Zn(OH)_2$,与正极反应相加:
$2FeO_4^{2-} + 8H_2O + 3Zn \rightarrow 2Fe(OH)_3 + 3Zn(OH)_2 + 4OH^-$