题目
氢是清洁能源,硼氢化钠(NaBH4)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为25℃,101kPa)NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g)ΔH<0请回答:(1)该反应能自发进行的条件是 ____ 。A.高温B.低温C.任意温度D.无法判断(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是 ____ 。A.升高溶液温度B.加入少量异丙胺[(CH3)2CHNH2]C.加入少量固体硼酸[B(OH)3]D.增大体系压强(3)为加速NaBH4水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比[n(NaBH4)/n(H2O)]之间的关系,结果如图1所示。请解释ab段变化的原因 ____ 。b-|||-出-|||-0-|||-[ n(NaB(H)_(4))/n((H)_(2)O)] -|||-用电器-|||-H2 O2-|||-(C{O)_(3)}^2--|||-图2-|||-投料比(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图2所示,正极上的电极反应式是 ____ 。该电池以3.2A恒定电流工作14分钟,消耗H2体积为0.49L,故可测得该电池将化学能转化为电能的转化率为 ____ 。[已知:该条件下H2的摩尔体积为24.5L/mol;电荷量q(C)=电流I(A)×时间(s);NA=6.0×1023mol-1;e=1.60×10-19C。](5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方法,将反应副产物偏硼酸钠(NaBO2)再生为NaBH4。(已知:ΔG是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比ΔH计算方法;当ΔG<0时,反应能自发进行。)Ⅰ.NaBH4(s)+2H2O(l)=NaBO2(s)+4H2(g)ΔG1=-320kJ/molⅡ.H2(g)+(1)/(2)O2(g)=H2O(l)ΔG2=-240kJ/molⅢ.Mg(s)+(1)/(2)O2(g)=MgO(s)ΔG3=-570kJ/mol请书写一个方程式表示NaBO2再生为NaBH4的一种制备方法,并注明ΔG ____ 。(要求:反应物不超过三种物质;氯原子利用率为100%。)
氢是清洁能源,硼氢化钠(NaBH4)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为25℃,101kPa)
NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g)ΔH<0
请回答:
(1)该反应能自发进行的条件是 ____ 。
A.高温
B.低温
C.任意温度
D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是 ____ 。
A.升高溶液温度
B.加入少量异丙胺[(CH3)2CHNH2]
C.加入少量固体硼酸[B(OH)3]
D.增大体系压强
(3)为加速NaBH4水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比[n(NaBH4)/n(H2O)]之间的关系,结果如图1所示。请解释ab段变化的原因 ____ 。
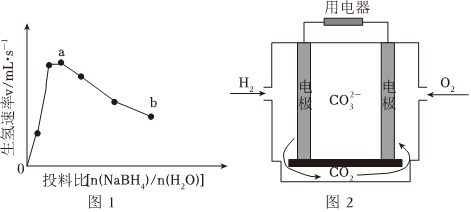
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图2所示,正极上的电极反应式是 ____ 。该电池以3.2A恒定电流工作14分钟,消耗H2体积为0.49L,故可测得该电池将化学能转化为电能的转化率为 ____ 。[已知:该条件下H2的摩尔体积为24.5L/mol;电荷量q(C)=电流I(A)×时间(s);NA=6.0×1023mol-1;e=1.60×10-19C。]
(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方法,将反应副产物偏硼酸钠(NaBO2)再生为NaBH4。(已知:ΔG是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比ΔH计算方法;当ΔG<0时,反应能自发进行。)
Ⅰ.NaBH4(s)+2H2O(l)=NaBO2(s)+4H2(g)ΔG1=-320kJ/mol
Ⅱ.H2(g)+$\frac{1}{2}$O2(g)=H2O(l)ΔG2=-240kJ/mol
Ⅲ.Mg(s)+$\frac{1}{2}$O2(g)=MgO(s)ΔG3=-570kJ/mol
请书写一个方程式表示NaBO2再生为NaBH4的一种制备方法,并注明ΔG ____ 。(要求:反应物不超过三种物质;氯原子利用率为100%。)
NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g)ΔH<0
请回答:
(1)该反应能自发进行的条件是 ____ 。
A.高温
B.低温
C.任意温度
D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是 ____ 。
A.升高溶液温度
B.加入少量异丙胺[(CH3)2CHNH2]
C.加入少量固体硼酸[B(OH)3]
D.增大体系压强
(3)为加速NaBH4水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比[n(NaBH4)/n(H2O)]之间的关系,结果如图1所示。请解释ab段变化的原因 ____ 。

(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图2所示,正极上的电极反应式是 ____ 。该电池以3.2A恒定电流工作14分钟,消耗H2体积为0.49L,故可测得该电池将化学能转化为电能的转化率为 ____ 。[已知:该条件下H2的摩尔体积为24.5L/mol;电荷量q(C)=电流I(A)×时间(s);NA=6.0×1023mol-1;e=1.60×10-19C。]
(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方法,将反应副产物偏硼酸钠(NaBO2)再生为NaBH4。(已知:ΔG是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比ΔH计算方法;当ΔG<0时,反应能自发进行。)
Ⅰ.NaBH4(s)+2H2O(l)=NaBO2(s)+4H2(g)ΔG1=-320kJ/mol
Ⅱ.H2(g)+$\frac{1}{2}$O2(g)=H2O(l)ΔG2=-240kJ/mol
Ⅲ.Mg(s)+$\frac{1}{2}$O2(g)=MgO(s)ΔG3=-570kJ/mol
请书写一个方程式表示NaBO2再生为NaBH4的一种制备方法,并注明ΔG ____ 。(要求:反应物不超过三种物质;氯原子利用率为100%。)
题目解答
答案
解:(1)由反应NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g)可知,ΔH<0,△S>0,ΔH—T△S恒小于0,任意温度下,该反应均能自发进行,
故答案为:C;
(2)A.升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,故A正确;
B.加入少量异丙胺[(CH3)2CHNH2],H2O的量减少,化学反应速率降低,故B错误;
C.加入少量固体硼酸[B(OH)3],H2O的量减少,化学反应速率降低,故C错误;
D.增大体系压强,忽略体积变化,则气体浓度不变,化学反应速率不变,故D错误;
故答案为:A;
(3)随着投料比[n(NaBH4)/n(H2O)]增大,NaBH4的水解转化率降低,因此生成氢气的速率不断减小,
故答案为:随着投料比[n(NaBH4)/n(H2O)]增大,NaBH4的水解转化率降低;
(4)根据题干信息,该燃料电池中H2为负极,O2为正极,熔融碳酸盐为电解质溶液,故正极的电极反应式为:O2+4e-+2CO2=-2${CO}_{3}^{2-}$;该条件下,0.49LH2的物质的量为n(H2)=$\frac{0.49L}{22.4L•mo{l}^{-1}}$=0.02mol,工作时,H2失去电子:H2-2e-=2H+,所带电荷量为:2×0.02mo×6.0×1023mol-1×1.60×10-19=3840C,工作电荷量为:3.2×14×60=2688C,则该电池0.49L将化学能转化为电能的转化率为:$\frac{2688C}{3840C}$×100%=70%,
故答案为:O2+4e-+2CO2=-2${CO}_{3}^{2-}$;70%;
(5)结合题干信息,要使得氢原子利用率为100%,可由(2×反应3)-(2×反应Ⅱ+反应I)得NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s),△G=2△G3-( 2△G2+△G1)=2×(-570kJ/mol)-[2×(-240kJ/mol)+(-320kJ/mol)]=-340kJ/mol,即NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s)△G=-340kJ/mol,
故答案为:NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s)△G=-340kJ/mol。
故答案为:C;
(2)A.升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,故A正确;
B.加入少量异丙胺[(CH3)2CHNH2],H2O的量减少,化学反应速率降低,故B错误;
C.加入少量固体硼酸[B(OH)3],H2O的量减少,化学反应速率降低,故C错误;
D.增大体系压强,忽略体积变化,则气体浓度不变,化学反应速率不变,故D错误;
故答案为:A;
(3)随着投料比[n(NaBH4)/n(H2O)]增大,NaBH4的水解转化率降低,因此生成氢气的速率不断减小,
故答案为:随着投料比[n(NaBH4)/n(H2O)]增大,NaBH4的水解转化率降低;
(4)根据题干信息,该燃料电池中H2为负极,O2为正极,熔融碳酸盐为电解质溶液,故正极的电极反应式为:O2+4e-+2CO2=-2${CO}_{3}^{2-}$;该条件下,0.49LH2的物质的量为n(H2)=$\frac{0.49L}{22.4L•mo{l}^{-1}}$=0.02mol,工作时,H2失去电子:H2-2e-=2H+,所带电荷量为:2×0.02mo×6.0×1023mol-1×1.60×10-19=3840C,工作电荷量为:3.2×14×60=2688C,则该电池0.49L将化学能转化为电能的转化率为:$\frac{2688C}{3840C}$×100%=70%,
故答案为:O2+4e-+2CO2=-2${CO}_{3}^{2-}$;70%;
(5)结合题干信息,要使得氢原子利用率为100%,可由(2×反应3)-(2×反应Ⅱ+反应I)得NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s),△G=2△G3-( 2△G2+△G1)=2×(-570kJ/mol)-[2×(-240kJ/mol)+(-320kJ/mol)]=-340kJ/mol,即NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s)△G=-340kJ/mol,
故答案为:NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s)△G=-340kJ/mol。