题目
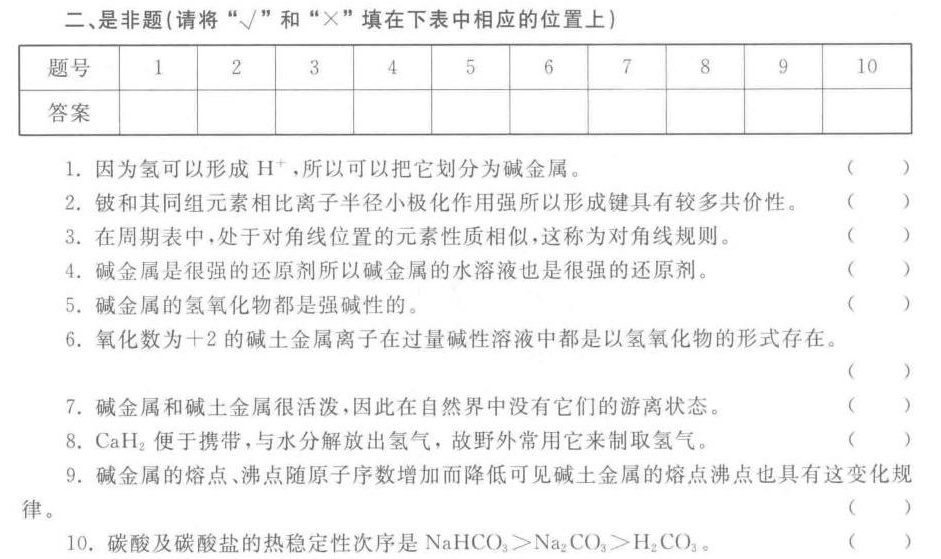
二、是非题(请将"√"和"×"填在下表中相应的位置上)-|||-题号 1 2 3 4 5 6 7 8 9 10-|||-答案-|||-1.因为氢可以形成 +, 所以可以把它划分为碱金属。 ()-|||-2. 铍和其同组元素相比离子半径小极化作用强所以形成键具有较多共价性。 ()-|||-3.在周期表中,处于对角线位置的元素性质相似,这称为对角线规则。 ()-|||-4.碱金属是很强的还原剂所以碱金属的水溶液也是很强的还原剂。 ()-|||-5.碱金属的氢氧化物都是强碱性的。 ()-|||-6.氧化数为 +2 的碱土金属离子在过量碱性溶液中都是以氢氧化物的形式存在。-|||-()-|||-7.碱金属和碱土金属很活泼,因此在自然界中没有它们的游离状态。 ()-|||-8.CaH2便于携带,与水分解放出氢气,故野外常用它来制取氢气。 ()-|||-9.碱金属的熔点、沸点随原子序数增加而降低可见碱土金属的熔点沸点也具有这变化规-|||-律。 ()-|||-10.碳酸及碳酸盐的热稳定性次序是 (O)_(3)gt (Na)_(2)C(O)_(3)gt (H)_(2)C(O)_(3) ()
题目解答
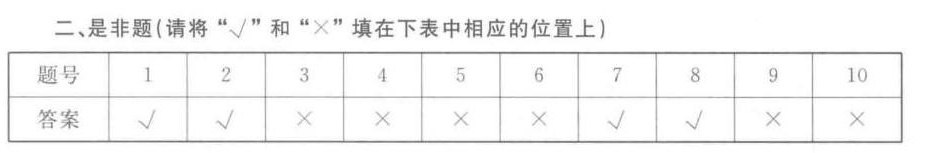
答案
解析
步骤 1:氢元素的性质
氢可以形成 ${H}^{+}$,但氢元素的性质与碱金属不同,它不具有碱金属的典型性质,如形成离子化合物的能力等。
步骤 2:铍的化学性质
铍的离子半径小,极化作用强,因此形成的化合物具有较多的共价性。
步骤 3:对角线规则
在周期表中,处于对角线位置的元素性质相似,这称为对角线规则。
步骤 4:碱金属的水溶液
碱金属是很强的还原剂,但它们的水溶液并不一定是强还原剂,因为水溶液中存在水分子的氧化还原性质。
步骤 5:碱金属的氢氧化物
碱金属的氢氧化物都是强碱性的,因为它们在水中完全电离。
步骤 6:碱土金属离子的存在形式
氧化数为 +2 的碱土金属离子在过量碱性溶液中并不一定都是以氢氧化物的形式存在,因为它们可能形成更稳定的络合物。
步骤 7:碱金属和碱土金属的游离状态
碱金属和碱土金属很活泼,因此在自然界中没有它们的游离状态。
步骤 8:CaH2的用途
CaH2便于携带,与水分解放出氢气,故野外常用它来制取氢气。
步骤 9:碱金属和碱土金属的熔点、沸点
碱金属的熔点、沸点随原子序数增加而降低,但碱土金属的熔点、沸点并不一定具有这变化规律。
步骤 10:碳酸及碳酸盐的热稳定性
碳酸及碳酸盐的热稳定性次序是 ${H}_{2}C{O}_{3}\gt NaHC{O}_{3}\gt {Na}_{2}C{O}_{3}$。
氢可以形成 ${H}^{+}$,但氢元素的性质与碱金属不同,它不具有碱金属的典型性质,如形成离子化合物的能力等。
步骤 2:铍的化学性质
铍的离子半径小,极化作用强,因此形成的化合物具有较多的共价性。
步骤 3:对角线规则
在周期表中,处于对角线位置的元素性质相似,这称为对角线规则。
步骤 4:碱金属的水溶液
碱金属是很强的还原剂,但它们的水溶液并不一定是强还原剂,因为水溶液中存在水分子的氧化还原性质。
步骤 5:碱金属的氢氧化物
碱金属的氢氧化物都是强碱性的,因为它们在水中完全电离。
步骤 6:碱土金属离子的存在形式
氧化数为 +2 的碱土金属离子在过量碱性溶液中并不一定都是以氢氧化物的形式存在,因为它们可能形成更稳定的络合物。
步骤 7:碱金属和碱土金属的游离状态
碱金属和碱土金属很活泼,因此在自然界中没有它们的游离状态。
步骤 8:CaH2的用途
CaH2便于携带,与水分解放出氢气,故野外常用它来制取氢气。
步骤 9:碱金属和碱土金属的熔点、沸点
碱金属的熔点、沸点随原子序数增加而降低,但碱土金属的熔点、沸点并不一定具有这变化规律。
步骤 10:碳酸及碳酸盐的热稳定性
碳酸及碳酸盐的热稳定性次序是 ${H}_{2}C{O}_{3}\gt NaHC{O}_{3}\gt {Na}_{2}C{O}_{3}$。