题目
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过如下反应制得:□ _(1)(O)_(2)+ □ C+|| N2 _(3)(N)_(4)+ □ CO(1)配平上述反应的化学方程式(将化学计量数填在方框内).(2)该反应中的氧化剂是____,其还原产物是____.(3)该反应的平衡常数表达式为K=____.(4)若知上述反应为放热反应,则其反应热△H____零(填“大于”“小于”或“等于”);升高温度,其平衡常数值____(填“增大”“减小”或“不变”).(5)若使压强增大,则上述平衡向____(填“正”或“逆”)反应方向移定(6)若已知CO生成速率为v(CO)=18mol·(L·min)−1,则N2消耗速率v(N2)=____mol·(L·min)−1.
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过如下反应制得:
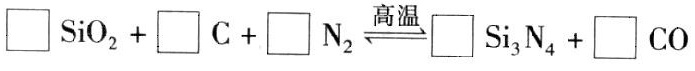
(1)配平上述反应的化学方程式(将化学计量数填在方框内).
(2)该反应中的氧化剂是____,其还原产物是____.
(3)该反应的平衡常数表达式为K=____.
(4)若知上述反应为放热反应,则其反应热△H____零(填“大于”“小于”或“等于”);升高温度,其平衡常数值____(填“增大”“减小”或“不变”).
(5)若使压强增大,则上述平衡向____(填“正”或“逆”)反应方向移定
(6)若已知CO生成速率为v(CO)=18mol·(L·min)−1,则N2消耗速率v(N2)=____mol·(L·min)−1.
题目解答
答案
解:(1)Si的化合价前后未变,N的化合价由0升为-3,C的化合价由0升为+2,生成1个氮化硅化合价降低12,生成1个CO化合价升高2,根据化合价升降总数相等以及质量守恒配平.
(2)化合价降低的反应物是氧化剂,氧化剂被还原得到的生成物是还原产物.
(3)化学平衡常数表达式为K= C6(CO)C2(N2)
(4)因反应是放热反应,所以△H<0,温度升高,平衡逆向移动,反应物的浓度增大,生成物浓度减少,平衡常数减小.
(5)压强增大,平衡向气体体积减小的方向移动,即逆反应方向.
(6)速率之比等于化学计量数之比.
故答案为:(1)3、6、2、1、6(2)N2;Si3N4(3) C6(CO)C2(N2)(4)小于;减小(5)逆(6)6
解析
步骤 1:配平化学方程式
氮化硅(Si3N4)的制备反应中,氮气(N2)作为氧化剂,将碳(C)氧化为一氧化碳(CO),同时氮气被还原为氮化硅(Si3N4)。根据化合价变化,氮气中的氮原子从0价变为-3价,每个氮化硅分子中有4个氮原子,因此氮气的系数为2。碳的化合价从0价变为+2价,生成一氧化碳(CO),因此碳的系数为6。硅的化合价未变,因此二氧化硅(SiO2)的系数为3,氮化硅(Si3N4)的系数为1,一氧化碳(CO)的系数为6。配平后的化学方程式为:3SiO2 + 6C + 2N2 → Si3N4 + 6CO。
步骤 2:确定氧化剂和还原产物
氮气(N2)作为氧化剂,被还原为氮化硅(Si3N4)。因此,氮化硅(Si3N4)是氮气的还原产物。
步骤 3:写出平衡常数表达式
平衡常数K的表达式为生成物浓度的乘积除以反应物浓度的乘积,且各物质的浓度均以化学计量数为指数。因此,K = [CO]^6 / [N2]^2。
步骤 4:分析反应热和温度对平衡常数的影响
由于反应是放热反应,反应热△H小于零。升高温度,平衡向吸热方向移动,即逆反应方向,因此平衡常数K减小。
步骤 5:分析压强对平衡的影响
压强增大,平衡向气体体积减小的方向移动,即逆反应方向。
步骤 6:计算N2的消耗速率
速率之比等于化学计量数之比,因此v(N2) = v(CO) / 3 = 18 mol·(L·min)^-1 / 3 = 6 mol·(L·min)^-1。
氮化硅(Si3N4)的制备反应中,氮气(N2)作为氧化剂,将碳(C)氧化为一氧化碳(CO),同时氮气被还原为氮化硅(Si3N4)。根据化合价变化,氮气中的氮原子从0价变为-3价,每个氮化硅分子中有4个氮原子,因此氮气的系数为2。碳的化合价从0价变为+2价,生成一氧化碳(CO),因此碳的系数为6。硅的化合价未变,因此二氧化硅(SiO2)的系数为3,氮化硅(Si3N4)的系数为1,一氧化碳(CO)的系数为6。配平后的化学方程式为:3SiO2 + 6C + 2N2 → Si3N4 + 6CO。
步骤 2:确定氧化剂和还原产物
氮气(N2)作为氧化剂,被还原为氮化硅(Si3N4)。因此,氮化硅(Si3N4)是氮气的还原产物。
步骤 3:写出平衡常数表达式
平衡常数K的表达式为生成物浓度的乘积除以反应物浓度的乘积,且各物质的浓度均以化学计量数为指数。因此,K = [CO]^6 / [N2]^2。
步骤 4:分析反应热和温度对平衡常数的影响
由于反应是放热反应,反应热△H小于零。升高温度,平衡向吸热方向移动,即逆反应方向,因此平衡常数K减小。
步骤 5:分析压强对平衡的影响
压强增大,平衡向气体体积减小的方向移动,即逆反应方向。
步骤 6:计算N2的消耗速率
速率之比等于化学计量数之比,因此v(N2) = v(CO) / 3 = 18 mol·(L·min)^-1 / 3 = 6 mol·(L·min)^-1。