题目
【题文】某同学利用30mL0.5mol/LCuSO4溶液和36mL0.5mol/LNa2CO3溶液反应制备Cu2(OH)2CO3,欲采用以下2种方案,实验操作及现象如下。序号实验操作实验现象Ⅰ将CuSO4溶液与Na2CO3溶液分别在75℃水浴锅中加热15分钟,再混合混合后,产生蓝色沉淀,有气泡产生Ⅱ将CuSO4溶液与Na2CO3溶液混合,再在75℃水浴锅中加热15分钟加热时,产生绿色沉淀,有气泡产生已知:Cu2(OH)2CO3在水中是绿色沉淀,Cu4(SO4)(OH)6在水中是蓝色沉淀。下列说法不正确的是A.为达到实验目的,应采用方案ⅡB.方案I中,混合前存在平衡:Cu2++2H2O雷Cu(OH)2+2H+C.制备原理是:2Cu2++2CO雷+H2O雷Cu2(OH)2CO3↓+CO2↑D.对比Ⅰ、Ⅱ可知,II中CO雷水解程度较大
【题文】某同学利用30mL0.5mol/LCuSO4溶液和36mL0.5mol/LNa2CO3溶液反应制备Cu2(OH)2CO3,欲采用以下2种方案,实验操作及现象如下。
已知:Cu2(OH)2CO3在水中是绿色沉淀,Cu4(SO4)(OH)6在水中是蓝色沉淀。下列说法不正确的是
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 将CuSO4溶液与Na2CO3溶液分别在75℃水浴锅中加热15分钟,再混合 | 混合后,产生蓝色沉淀,有气泡产生 |
| Ⅱ | 将CuSO4溶液与Na2CO3溶液混合,再在75℃水浴锅中加热15分钟 | 加热时,产生绿色沉淀,有气泡产生 |
| A.为达到实验目的,应采用方案Ⅱ |
B.方案I中,混合前存在平衡:Cu2++2H2O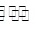 Cu(OH)2+2H+ Cu(OH)2+2H+ |
C.制备原理是:2Cu2++2CO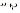 +H2O +H2O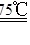 Cu2(OH)2CO3↓+CO2↑ Cu2(OH)2CO3↓+CO2↑ |
D.对比Ⅰ、Ⅱ可知,II中CO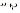 水解程度较大 水解程度较大 |
题目解答
答案
【答案】D
解析
本题考查难溶物制备条件的选择及盐类水解的影响因素。解题关键在于:
- 明确产物颜色差异:Cu₂(OH)₂CO₃为绿色沉淀,Cu₄(SO₄)(OH)₆为蓝色沉淀,实验现象直接反映产物类型。
- 分析水解条件:Cu²⁺和CO₃²⁻的水解相互影响,加热促进水解,但混合顺序不同会导致反应路径差异。
- 对比方案差异:方案I先加热再混合,方案II先混合再加热,需判断哪种条件更有利于目标产物生成。
选项分析
选项A
方案II生成绿色沉淀(目标产物),而方案I生成蓝色沉淀(副产物),因此应选择方案II。正确。
选项B
Cu²⁺在水中存在水解平衡:
$\text{Cu}^{2+} + 2\text{H}_2\text{O} \rightleftharpoons \text{Cu(OH)}_2 + 2\text{H}^+$
加热会促进该平衡右移,正确。
选项C
反应式配平正确,且符合实验现象(生成CO₂气泡和绿色沉淀),正确。
选项D
关键点:
- 方案II中,混合后加热,虽然温度升高会促进CO₃²⁻水解,但Cu²⁺与CO₃²⁻迅速反应消耗部分CO₃²⁻,导致水解程度反而较小。
- 方案I中,Na₂CO₃溶液单独加热时,CO₃²⁻水解更充分,生成更多HCO₃⁻和CO₂。
因此,方案I中CO₃²⁻的水解程度更大,选项D错误。