题目
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:ΔcH(298 K)(CH3OH(g))=-763.9 kJ·mol-1 (1)ΔcH(298 K)(C(s))=-393.5 kJ·mol-1 (2)ΔcH(298 K)(H2(g))=-285.8 kJ·mol-1 (3)ΔcH(298 K)(CO(g))=-283.0 kJ·mol-1 (4)
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:
ΔcH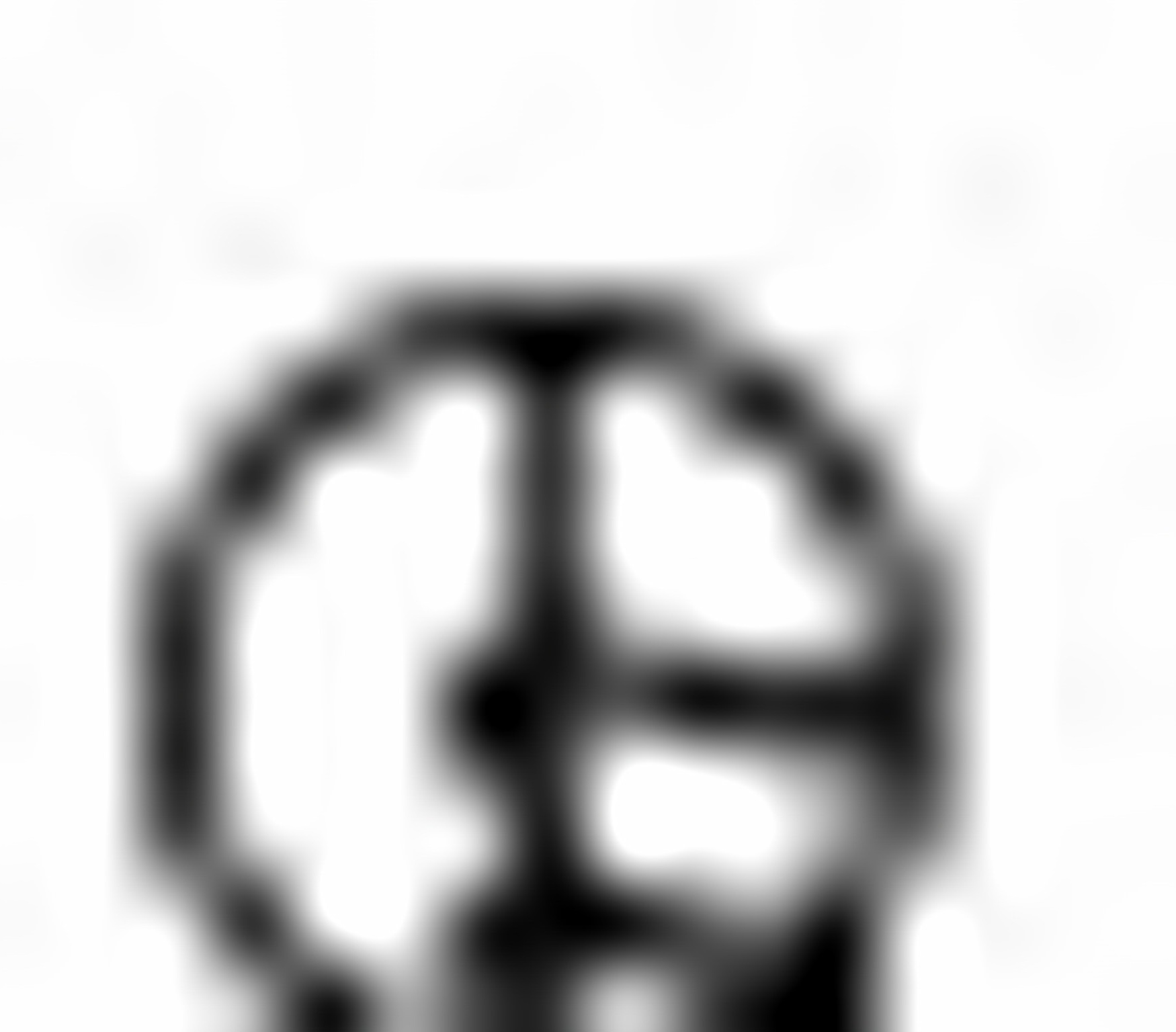 (298 K)(CH3OH(g))=-763.9 kJ·mol-1 (1)
(298 K)(CH3OH(g))=-763.9 kJ·mol-1 (1)
ΔcH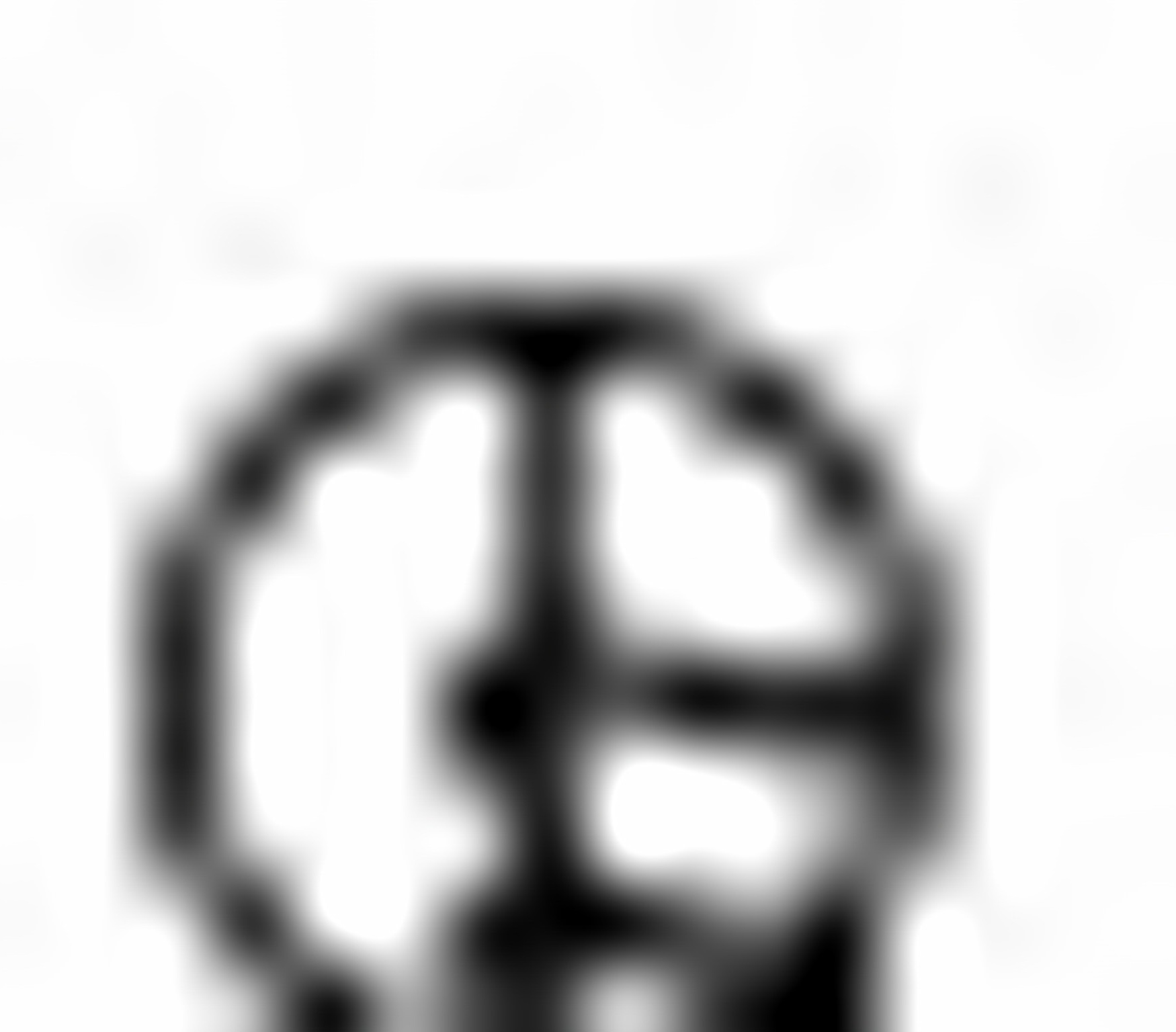 (298 K)(C(s))=-393.5 kJ·mol-1 (2)
(298 K)(C(s))=-393.5 kJ·mol-1 (2)
ΔcH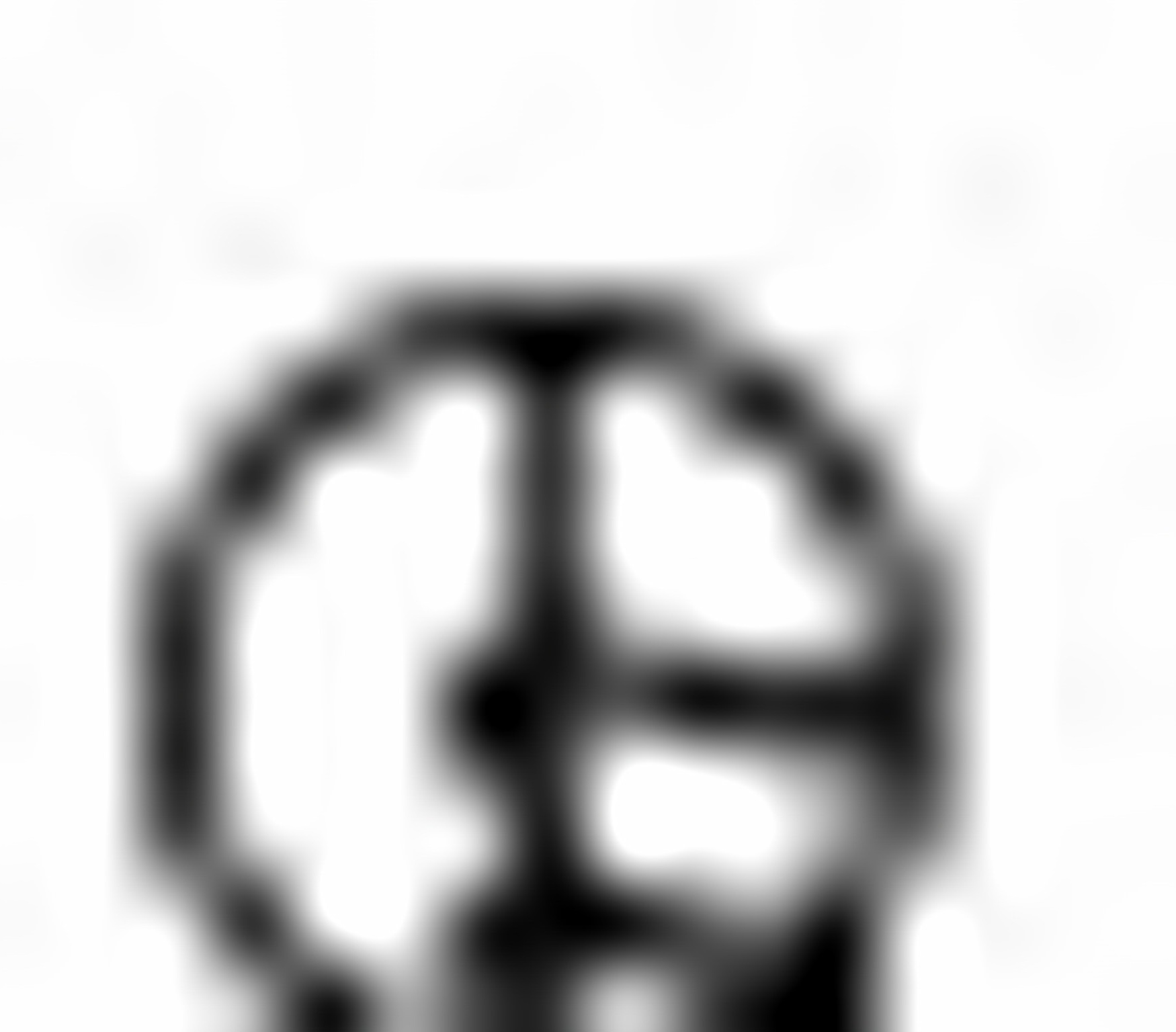 (298 K)(H2(g))=-285.8 kJ·mol-1 (3)
(298 K)(H2(g))=-285.8 kJ·mol-1 (3)
ΔcH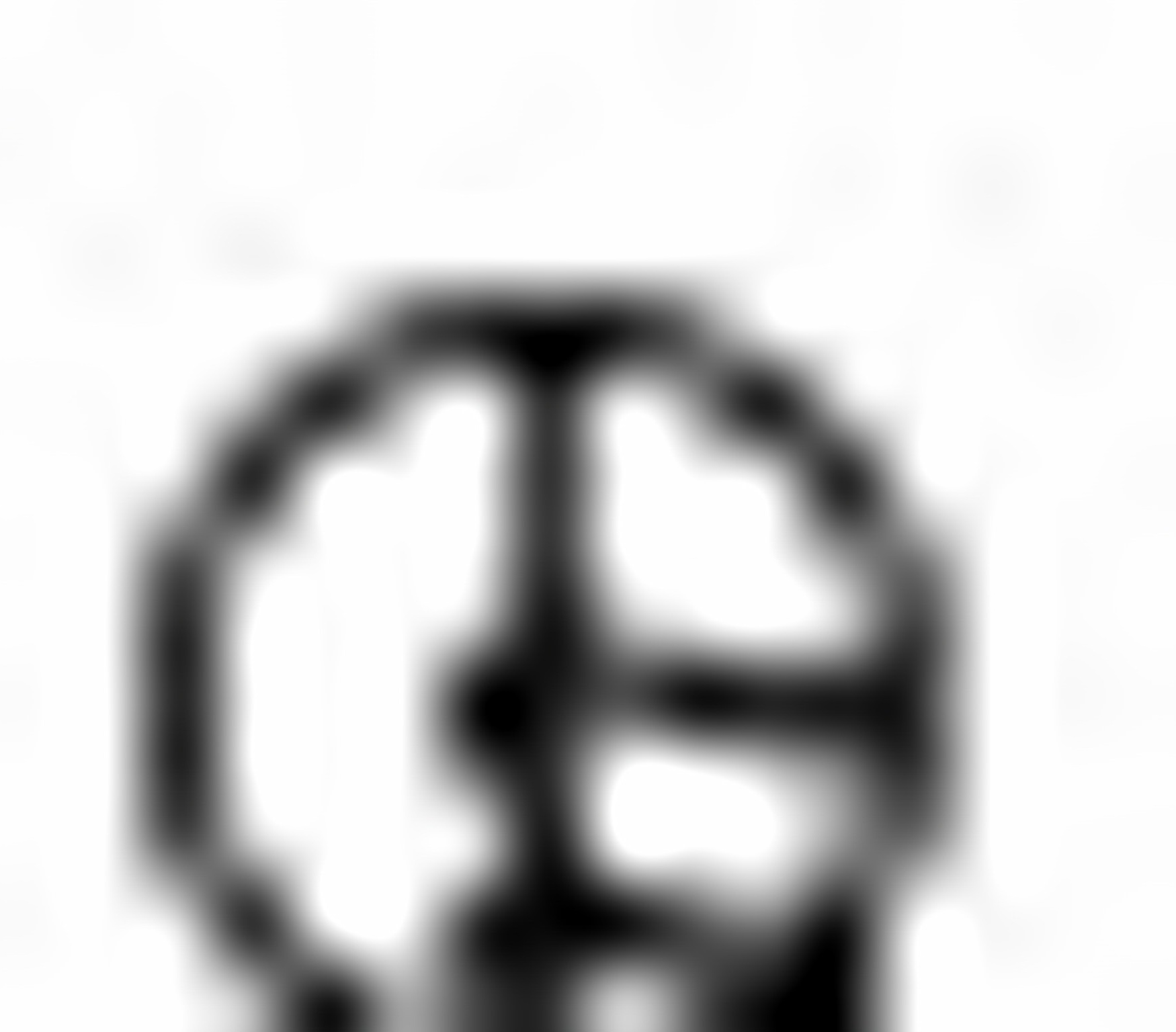 (298 K)(CO(g))=-283.0 kJ·mol-1 (4)
(298 K)(CO(g))=-283.0 kJ·mol-1 (4)
题目解答
答案
:
得ΔH(298 K,CO(g))=-110.5 kJ·mol
ΔH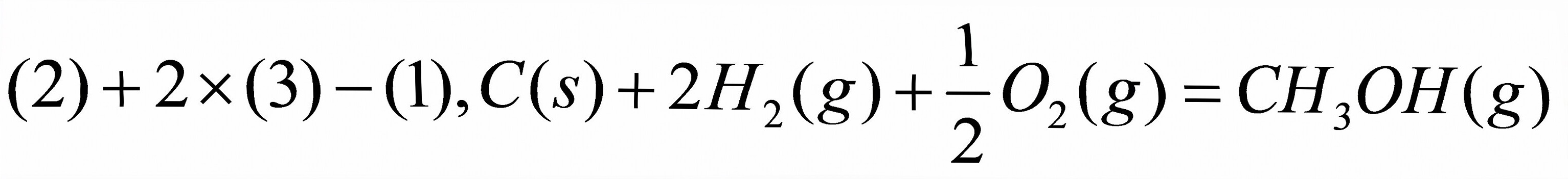 (298 K,CHOH(g))=-201.2 kJ·mol
(298 K,CHOH(g))=-201.2 kJ·mol
反应 CO(g)+2H(g)=CHOH(g)
ΔH(298 K)=-90.7 kJ·mol
解析
步骤 1:计算CO(g)的标准生成焓
根据燃烧焓数据,CO(g)的燃烧反应为:
\[ CO(g) + \frac{1}{2}O_2(g) \rightarrow CO_2(g) \]
其标准生成焓为:
\[ \Delta_cH(298 K)(CO(g)) = -283.0 \, kJ \cdot mol^{-1} \]
由于CO(g)的生成反应为:
\[ C(s) + \frac{1}{2}O_2(g) \rightarrow CO(g) \]
其标准生成焓为:
\[ \Delta_fH(298 K)(CO(g)) = \Delta_cH(298 K)(C(s)) - \Delta_cH(298 K)(CO(g)) \]
代入已知数据:
\[ \Delta_fH(298 K)(CO(g)) = -393.5 \, kJ \cdot mol^{-1} - (-283.0 \, kJ \cdot mol^{-1}) = -110.5 \, kJ \cdot mol^{-1} \]
步骤 2:计算CH3OH(g)的标准生成焓
根据燃烧焓数据,CH3OH(g)的燃烧反应为:
\[ CH_3OH(g) + \frac{3}{2}O_2(g) \rightarrow CO_2(g) + 2H_2O(l) \]
其标准生成焓为:
\[ \Delta_cH(298 K)(CH_3OH(g)) = -763.9 \, kJ \cdot mol^{-1} \]
由于CH3OH(g)的生成反应为:
\[ C(s) + 2H_2(g) + \frac{1}{2}O_2(g) \rightarrow CH_3OH(g) \]
其标准生成焓为:
\[ \Delta_fH(298 K)(CH_3OH(g)) = \Delta_cH(298 K)(C(s)) + 2 \times \Delta_cH(298 K)(H_2(g)) - \Delta_cH(298 K)(CH_3OH(g)) \]
代入已知数据:
\[ \Delta_fH(298 K)(CH_3OH(g)) = -393.5 \, kJ \cdot mol^{-1} + 2 \times (-285.8 \, kJ \cdot mol^{-1}) - (-763.9 \, kJ \cdot mol^{-1}) = -201.2 \, kJ \cdot mol^{-1} \]
步骤 3:计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变
根据标准生成焓,反应的标准焓变为:
\[ \Delta_rH(298 K) = \Delta_fH(298 K)(CH_3OH(g)) - \Delta_fH(298 K)(CO(g)) - 2 \times \Delta_fH(298 K)(H_2(g)) \]
代入已知数据:
\[ \Delta_rH(298 K) = -201.2 \, kJ \cdot mol^{-1} - (-110.5 \, kJ \cdot mol^{-1}) - 2 \times 0 \, kJ \cdot mol^{-1} = -90.7 \, kJ \cdot mol^{-1} \]
根据燃烧焓数据,CO(g)的燃烧反应为:
\[ CO(g) + \frac{1}{2}O_2(g) \rightarrow CO_2(g) \]
其标准生成焓为:
\[ \Delta_cH(298 K)(CO(g)) = -283.0 \, kJ \cdot mol^{-1} \]
由于CO(g)的生成反应为:
\[ C(s) + \frac{1}{2}O_2(g) \rightarrow CO(g) \]
其标准生成焓为:
\[ \Delta_fH(298 K)(CO(g)) = \Delta_cH(298 K)(C(s)) - \Delta_cH(298 K)(CO(g)) \]
代入已知数据:
\[ \Delta_fH(298 K)(CO(g)) = -393.5 \, kJ \cdot mol^{-1} - (-283.0 \, kJ \cdot mol^{-1}) = -110.5 \, kJ \cdot mol^{-1} \]
步骤 2:计算CH3OH(g)的标准生成焓
根据燃烧焓数据,CH3OH(g)的燃烧反应为:
\[ CH_3OH(g) + \frac{3}{2}O_2(g) \rightarrow CO_2(g) + 2H_2O(l) \]
其标准生成焓为:
\[ \Delta_cH(298 K)(CH_3OH(g)) = -763.9 \, kJ \cdot mol^{-1} \]
由于CH3OH(g)的生成反应为:
\[ C(s) + 2H_2(g) + \frac{1}{2}O_2(g) \rightarrow CH_3OH(g) \]
其标准生成焓为:
\[ \Delta_fH(298 K)(CH_3OH(g)) = \Delta_cH(298 K)(C(s)) + 2 \times \Delta_cH(298 K)(H_2(g)) - \Delta_cH(298 K)(CH_3OH(g)) \]
代入已知数据:
\[ \Delta_fH(298 K)(CH_3OH(g)) = -393.5 \, kJ \cdot mol^{-1} + 2 \times (-285.8 \, kJ \cdot mol^{-1}) - (-763.9 \, kJ \cdot mol^{-1}) = -201.2 \, kJ \cdot mol^{-1} \]
步骤 3:计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变
根据标准生成焓,反应的标准焓变为:
\[ \Delta_rH(298 K) = \Delta_fH(298 K)(CH_3OH(g)) - \Delta_fH(298 K)(CO(g)) - 2 \times \Delta_fH(298 K)(H_2(g)) \]
代入已知数据:
\[ \Delta_rH(298 K) = -201.2 \, kJ \cdot mol^{-1} - (-110.5 \, kJ \cdot mol^{-1}) - 2 \times 0 \, kJ \cdot mol^{-1} = -90.7 \, kJ \cdot mol^{-1} \]