题目
用KMnO4法测定硅酸盐样品中的Ca2+含量。称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀。将洗净的CaC2O4溶解于稀H2SO4中,用0.05052 molL1 KMnO4标准溶液滴定,消耗25.64mL。计算硅酸盐中Ca的质量分数。
用KMnO4法测定硅酸盐样品中的Ca2+含量。称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀。将洗净的CaC2O4溶解于稀H2SO4中,用0.05052 molL1 KMnO4标准溶液滴定,消耗25.64mL。计算硅酸盐中Ca的质量分数。
题目解答
答案
解: n(Ca) = n(C2O42-) = 5n(MnO4-)/2
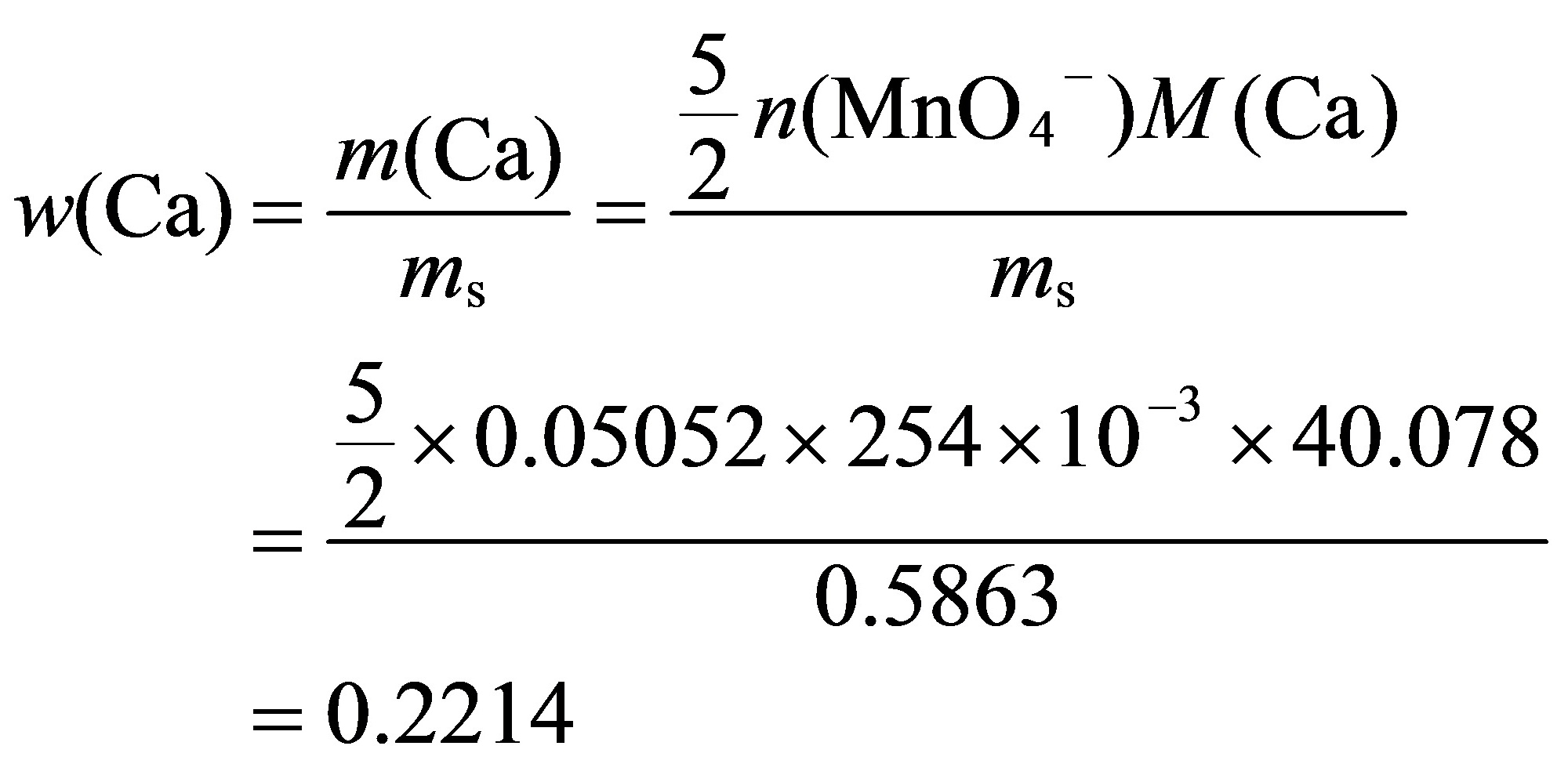
解析
步骤 1:确定反应关系
在KMnO4法测定Ca2+含量的过程中,CaC2O4溶解于稀H2SO4中,然后用KMnO4标准溶液滴定生成的C2O42-。反应关系为:
\[ 2MnO_4^- + 5C_2O_4^{2-} + 16H^+ \rightarrow 2Mn^{2+} + 10CO_2 + 8H_2O \]
步骤 2:计算CaC2O4的摩尔数
根据反应关系,n(Ca) = n(C2O42-) = 5n(MnO4-)/2。已知KMnO4的浓度为0.05052 mol/L,消耗体积为25.64 mL,可以计算出n(MnO4-):
\[ n(MnO_4^-) = 0.05052 \times 25.64 \times 10^{-3} \]
步骤 3:计算Ca的质量
根据步骤2计算出的n(MnO4-),可以计算出n(Ca),进而计算出Ca的质量:
\[ m(Ca) = n(Ca) \times M(Ca) \]
步骤 4:计算Ca的质量分数
根据步骤3计算出的Ca的质量,可以计算出Ca的质量分数:
\[ \omega(Ca) = \frac{m(Ca)}{m_{试样}} \times 100\% \]
在KMnO4法测定Ca2+含量的过程中,CaC2O4溶解于稀H2SO4中,然后用KMnO4标准溶液滴定生成的C2O42-。反应关系为:
\[ 2MnO_4^- + 5C_2O_4^{2-} + 16H^+ \rightarrow 2Mn^{2+} + 10CO_2 + 8H_2O \]
步骤 2:计算CaC2O4的摩尔数
根据反应关系,n(Ca) = n(C2O42-) = 5n(MnO4-)/2。已知KMnO4的浓度为0.05052 mol/L,消耗体积为25.64 mL,可以计算出n(MnO4-):
\[ n(MnO_4^-) = 0.05052 \times 25.64 \times 10^{-3} \]
步骤 3:计算Ca的质量
根据步骤2计算出的n(MnO4-),可以计算出n(Ca),进而计算出Ca的质量:
\[ m(Ca) = n(Ca) \times M(Ca) \]
步骤 4:计算Ca的质量分数
根据步骤3计算出的Ca的质量,可以计算出Ca的质量分数:
\[ \omega(Ca) = \frac{m(Ca)}{m_{试样}} \times 100\% \]