题目
已知金属镍为A1型结构,原子间接触距离为249.2pm,请计算:(1)Ni立方晶胞参数;(2)金属镍的密度;(3)画出(100),(110),(111)面上原子能的排列方式并计算面上距离最近的原子间距。
已知金属镍为A1型结构,原子间接触距离为249.2pm,请计算:
(1)Ni立方晶胞参数;
(2)金属镍的密度;
(3)画出(100),(110),(111)面上原子能的排列方式并计算面上距离最近的原子间距。
题目解答
答案
答:(1)accp = 23/2r =23/2249.2/2 =352.4pm
(2)d=N×M /[(352.4×10-10)3×6.02×1023] =8.908g/cm3
(3)
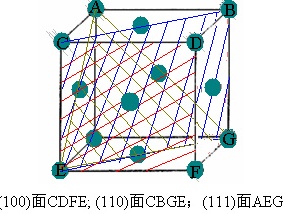
三个面上原子间最近原子间距均为249.2pm
解析
- 晶胞参数计算:A1型结构(面心立方)中,最近邻原子间距为面心原子间的面对角线距离,需通过几何关系推导晶胞边长。
- 密度计算:利用晶胞参数、阿伏伽德罗常数和摩尔质量,结合密度公式直接计算。
- 晶面分析:不同晶面(100)、(110)、(111)的原子排列遵循晶面指数规则,最近原子间距均等于接触距离。
第(1)题
结构分析
A1型结构为面心立方,每个晶胞含4个原子。最近邻原子间距为面心原子间的面对角线距离,即:
$a \cdot \frac{\sqrt{2}}{2} = r$
晶胞边长计算
解得晶胞参数:
$a = \frac{2r}{\sqrt{2}} = r \sqrt{2}$
代入 $r = 249.2 \, \text{pm}$:
$a = 249.2 \cdot \sqrt{2} \approx 352.4 \, \text{pm}$
第(2)题
密度公式
密度公式为:
$d = \frac{N \cdot M}{a^3 \cdot N_A}$
其中:
- $N = 4$(面心立方晶胞原子数)
- $M = 58.69 \, \text{g/mol}$(Ni的摩尔质量)
- $a = 352.4 \, \text{pm} = 3.524 \times 10^{-8} \, \text{cm}$
- $N_A = 6.02 \times 10^{23} \, \text{mol}^{-1}$
代入计算
$d = \frac{4 \cdot 58.69}{(3.524 \times 10^{-8})^3 \cdot 6.02 \times 10^{23}} \approx 8.908 \, \text{g/cm}^3$
第(3)题
晶面原子排列
- (100)面:原子位于面心,排列为正方形网格(如CDFE)。
- (110)面:原子排列为菱形网格(如CBGE)。
- (111)面:原子排列为六边形密堆积(如AEG)。
最近原子间距
所有晶面上最近原子间距均等于原始接触距离 $249.2 \, \text{pm}$。