铅及其化合物工业生产及日常生活具有非常广泛的用途,通过铅矿的冶炼或从含铅废料中提炼回收均可得到金属铅。 Ⅰrm(.)铅的冶炼 rm((1))瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下: rm(①2PbS(s)+3O_{2)(g)==2PbO(s)+2SO_(2)(g) Δ}rm(H) rm({,!)_(1)= a kJ·mol^-1} rm(②PbS(s)+2PbO(s)==3Pb(s)+SO_{2)(g)} rm(Δ)rm(H) rm({,!)_(2)= b kJ·mol^-1} rm(③PbS(s)+PbSO_{4)(s)==2Pb(s)+2SO_(2)(g)} rm(Δ)rm(H) rm({,!)_(3)= c kJ·mol^-1} 反应rm(3PbS(s) + 6O_{2)(g) == 3PbSO_(4)(s)} rm(Δ)rm(H)rm(=) rm(kJ·mol^-1()用含rm(a)、rm(b)、rm(c)的代数式表示rm())。 rm((2))还原法炼铅,包含反应rm(PbO(s) + CO(g)) rm(Pb(s) + CO_{2)(g) Δ}rm(H),该反应的平衡常数的对数值与温度的关系如下表 温度rm(/℃) rm(300) rm(727) rm(1227) rm(lg )rm(K) rm(6.17) rm(2.87) rm(1.24) rm(①)该还原反应的rm(Δ)rm(H) rm(0()选填“rm( > )”、“rm( < )”或“rm(=)”rm())。 rm(②)当rm(lg )rm(K)rm(=1)且起始时只通入rm(CO(PbO)足量rm()),达平衡时,混合气体中rm(CO)的体积分数为 。 Ⅱrm(.)铅的回收 从含铅废料rm((PbSO_{4)}、rm(PbO_{2)}、rm(PbO)等rm())中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下: rm((3))过程rm(I),已知:rm(25℃)时,rm(K)rm({,!)_(sp)(PbSO_(4))=1.82×10^—8}、rm(K)rm({,!)_(sp)(PbCO_(3))=1.46×10^—13};rm(Na_{2)SO_(4)}、rm(Na_{2)CO_(3)}的溶解度曲线如图rm(1)所示。 rm(①)写出过程rm(I)的离子方程式 。 rm(②)生产过程中的温度应保持在rm(40℃),若温度降低,rm(PbSO_{4)}的转化速率下降。根据图rm(1),解释可能原因:rm(i.)温度降低,反应速率降低;rm(ii). rm(()请你提出一种合理解释rm())。 rm(③)若生产过程中温度低于rm(40℃),所得固体中含有较多rm(Na_{2)SO_(4)}杂质,原因是 。 rm((4))过程Ⅱ,发生反应rm(2PbO_{2)+H_(2)C_(2)O_(4)==2PbO+H_(2)O_(2)+2CO_(2)↑}。实验中检测到有大量rm(O_{2)}放出,推测rm(PbO_{2)}氧化了rm(H_{2)O_(2)},通过实验证实了这一推测。实验方案是 。rm(()已知:rm(PbO_{2)}为棕黑色固体;rm(PbO)为橙黄色固体rm()) rm((5))过程Ⅲ,将rm(PbO)粗品溶解在rm(HCl)和rm(NaCl)的混合溶液中,得到含rm(Na_{2)PbCl_(4)}的电解液,电解rm(Na_{2)PbCl_(4)}溶液,生成rm(Pb),如图rm(2)。 rm(①)阴极的电极反应式是____________。 rm(②)电解一段时间后,rm(PbCl_{4)^2-}浓度极大下降,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是______ rm(_)。
铅及其化合物工业生产及日常生活具有非常广泛的用途,通过铅矿的冶炼或从含铅废料中提炼回收均可得到金属铅。
Ⅰ$\rm{.}$铅的冶炼
$\rm{(1)}$瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
$\rm{①2PbS(s)+3O_{2}(g)==2PbO(s)+2SO_{2}(g) Δ}$$\rm{H}$ $\rm{{\,\!}_{1}= a kJ·mol^{-1}}$
$\rm{②PbS(s)+2PbO(s)==3Pb(s)+SO_{2}(g)}$ $\rm{Δ}$$\rm{H}$ $\rm{{\,\!}_{2}= b kJ·mol^{-1}}$
$\rm{③PbS(s)+PbSO_{4}(s)==2Pb(s)+2SO_{2}(g)}$ $\rm{Δ}$$\rm{H}$ $\rm{{\,\!}_{3}= c kJ·mol^{-1}}$
反应$\rm{3PbS(s) + 6O_{2}(g) == 3PbSO_{4}(s)}$ $\rm{Δ}$$\rm{H}$$\rm{=}$ $\rm{kJ·mol^{-1}(}$用含$\rm{a}$、$\rm{b}$、$\rm{c}$的代数式表示$\rm{)}$。
$\rm{(2)}$还原法炼铅,包含反应$\rm{PbO(s) + CO(g)}$![]() $\rm{Pb(s) + CO_{2}(g) Δ}$$\rm{H}$,该反应的平衡常数的对数值与温度的关系如下表
$\rm{Pb(s) + CO_{2}(g) Δ}$$\rm{H}$,该反应的平衡常数的对数值与温度的关系如下表
温度$\rm{/℃}$ | $\rm{300}$ | $\rm{727}$ | $\rm{1227}$ |
$\rm{\lg }$$\rm{K}$ | $\rm{6.17}$ | $\rm{2.87}$ | $\rm{1.24}$ |
$\rm{①}$该还原反应的$\rm{Δ}$$\rm{H}$ $\rm{0(}$选填“$\rm{ > }$”、“$\rm{ < }$”或“$\rm{=}$”$\rm{)}$。
$\rm{②}$当$\rm{\lg }$$\rm{K}$$\rm{=1}$且起始时只通入$\rm{CO(PbO}$足量$\rm{)}$,达平衡时,混合气体中$\rm{CO}$的体积分数为 。
Ⅱ$\rm{.}$铅的回收
从含铅废料$\rm{(PbSO_{4}}$、$\rm{PbO_{2}}$、$\rm{PbO}$等$\rm{)}$中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下:
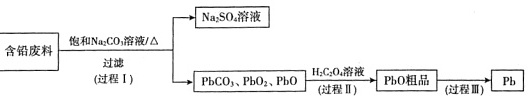
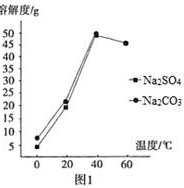
$\rm{(3)}$过程$\rm{I}$,已知:$\rm{25℃}$时,$\rm{K}$$\rm{{\,\!}_{sp}(PbSO_{4})=1.82×10^{—8}}$、$\rm{K}$$\rm{{\,\!}_{sp}(PbCO_{3})=1.46×10^{—13}}$;$\rm{Na_{2}SO_{4}}$、$\rm{Na_{2}CO_{3}}$的溶解度曲线如图$\rm{1}$所示。
$\rm{①}$写出过程$\rm{I}$的离子方程式 。
$\rm{②}$生产过程中的温度应保持在$\rm{40℃}$,若温度降低,$\rm{PbSO_{4}}$的转化速率下降。根据图$\rm{1}$,解释可能原因:$\rm{i.}$温度降低,反应速率降低;$\rm{ii}$. $\rm{(}$请你提出一种合理解释$\rm{)}$。
$\rm{③}$若生产过程中温度低于$\rm{40℃}$,所得固体中含有较多$\rm{Na_{2}SO_{4}}$杂质,原因是 。
$\rm{(4)}$过程Ⅱ,发生反应$\rm{2PbO_{2}+H_{2}C_{2}O_{4}==2PbO+H_{2}O_{2}+2CO_{2}↑}$。实验中检测到有大量$\rm{O_{2}}$放出,推测$\rm{PbO_{2}}$氧化了$\rm{H_{2}O_{2}}$,通过实验证实了这一推测。实验方案是 。$\rm{(}$已知:$\rm{PbO_{2}}$为棕黑色固体;$\rm{PbO}$为橙黄色固体$\rm{)}$
$\rm{(5)}$过程Ⅲ,将$\rm{PbO}$粗品溶解在$\rm{HCl}$和$\rm{NaCl}$的混合溶液中,得到含$\rm{Na_{2}PbCl_{4}}$的电解液,电解$\rm{Na_{2}PbCl_{4}}$溶液,生成$\rm{Pb}$,如图$\rm{2}$。
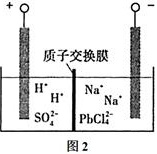
$\rm{①}$阴极的电极反应式是____________。
$\rm{②}$电解一段时间后,$\rm{PbCl_{4}^{2-}}$浓度极大下降,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是______ $\rm{\_}$。
题目解答
答案
$\rm{(1)(2a+2b-3c)}$;
$\rm{(2) < }$;$\rm{90.9\%}$;
$\rm{(3)①PbSO_{4}(s) + CO_{3}^{2-}(aq)}$![]() $\rm{PbCO_{3}}$ $\rm{(s) +SO_{4}^{2-}(aq)}$;
$\rm{PbCO_{3}}$ $\rm{(s) +SO_{4}^{2-}(aq)}$;
$\rm{②Na_{2}SO_{4}}$、$\rm{Na_{2}CO_{3}}$浓度降低,反应速率降低;
$\rm{③}$温度低于$\rm{40℃}$时,温度降低,平衡“$\rm{Na_{2}SO_{4}}$ $\rm{(s)}$![]() $\rm{2Na^{+}(aq) + SO_{4}^{2-}(aq)}$”逆向移动,产生较多$\rm{Na_{2}SO_{4}}$固体杂质;
$\rm{2Na^{+}(aq) + SO_{4}^{2-}(aq)}$”逆向移动,产生较多$\rm{Na_{2}SO_{4}}$固体杂质;
$\rm{(4)}$取少量$\rm{PbO_{2}}$于试管中,向其中滴加$\rm{H_{2}O_{2}}$溶液,产生可使带火星木条复燃的气体,同时棕黑色固体变为橙黄色,证实推测正确;
$\rm{(5)①PbCl_{4}^{2-}+2e^{-}==Pb +4Cl^{-}}$;$\rm{②}$继续向阴极区加$\rm{PbO}$粗品。