题目
聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。回答下列问题:Ⅰ.苯乙烯的制备(1)工业常采用乙苯脱氢的方法制备苯乙烯,其原理如下:反应甲:C_(6)H_(5)-CH_(2)CH_(3)(g)leftharpoons C_(6)H_(5)-CH=CH_(2)(g)+H_(2)(g) Delta H_(1)近期科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):2 C6H5-CH=C H2(g)+H2(g)-|||-1.35-|||-1 过渡态2-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)(g) 过渡态1 0.40 1.56eV-|||-要 0 -0.15 不 -0.21-|||-1.49eV-|||-0.94eV 0.73 _(6)(H)_(5)-CHC(H)_(2)+2(H)^+-|||--1 1.09. C6H5-CH2CH2× +H×-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)-|||-反应历程乙苯脱氢制苯乙烯反应的焓变Delta H_(1)______0(选填“大于”或“小于”或“等于”),该反应历程的决速步骤反应方程式为______。(2)乙苯脱氢是合成苯乙烯的关键步骤。某温度下,向2.0L恒容密闭容器中充入0.10molC_(6)H_(5)CH_(2)CH_(3)(g),测得乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:时间t/h0124816202530总压强p/100kPa4.915.586.327.318.549.509.529.539.53计算该温度下的平衡常数K=______(结果保留至小数点后两位)。(3)在913K、100kPa下,以水蒸气作稀释气。Fe_(2)O_(3)作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:反应乙:C_(6)H_(5)C_(2)H_(5)(g)leftharpoons C_(6)H_(6)(g)+CH_(2)=CH_(2)(g)反应丙:C_(6)H_(5)C_(2)H_(5)(g)+H_(2)(g)leftharpoons C_(6)H_(5)CH_(3)(g)+CH_(4)(g)以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S随乙苯转化率的变化曲线如图2所示,其中曲线b代表的产物是______,理由是______。(S=转化为目的产物所消耗乙苯的量times 100%)2 C6H5-CH=C H2(g)+H2(g)-|||-1.35-|||-1 过渡态2-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)(g) 过渡态1 0.40 1.56eV-|||-要 0 -0.15 不 -0.21-|||-1.49eV-|||-0.94eV 0.73 _(6)(H)_(5)-CHC(H)_(2)+2(H)^+-|||--1 1.09. C6H5-CH2CH2× +H×-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)-|||-反应历程(4)实验测得,乙苯脱氢反应的速率方程为v_(正)=k_(正)p_(乙苯),v_(逆)=k_(逆)p_(苯乙烯)p_(氢气)(k_(正)、k_(逆)为速率(1)/(T)常数,只与温度有关),图3中③代表lg k_(逆)随(1)/(T)的变化关系,则能代表lg k_(正)随(1)/(T)的变化关系的是______。2 C6H5-CH=C H2(g)+H2(g)-|||-1.35-|||-1 过渡态2-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)(g) 过渡态1 0.40 1.56eV-|||-要 0 -0.15 不 -0.21-|||-1.49eV-|||-0.94eV 0.73 _(6)(H)_(5)-CHC(H)_(2)+2(H)^+-|||--1 1.09. C6H5-CH2CH2× +H×-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)-|||-反应历程Ⅱ.苯乙烯的聚合(5)苯乙烯聚合有多种方法,其中一种方法的关键步骤是某Cu(I)的配合物促进,CuCl是合成该Cu(I)的配合物的关键物质。在CuCl的晶胞中,Cl^-的位置如图4所示。Cu^+填充于Cl^-构成的四面体空隙中,则Cu^+的配位数为______;若N_(A)为阿伏加德罗常数的值,该晶体的密度为rho gcdot cm^-3,则该晶胞中Cu^+之间的距离为______nm(用含rho 、N_(A)的代数式表示)。2 C6H5-CH=C H2(g)+H2(g)-|||-1.35-|||-1 过渡态2-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)(g) 过渡态1 0.40 1.56eV-|||-要 0 -0.15 不 -0.21-|||-1.49eV-|||-0.94eV 0.73 _(6)(H)_(5)-CHC(H)_(2)+2(H)^+-|||--1 1.09. C6H5-CH2CH2× +H×-|||-_(6)(H)_(5)-C(H)_(2)C(H)_(3)-|||-反应历程
聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。回答下列问题:
$Ⅰ$.苯乙烯的制备
$(1)$工业常采用乙苯脱氢的方法制备苯乙烯,其原理如下:
反应甲:$C_{6}H_{5}-CH_{2}CH_{3}(g)\rightleftharpoons C_{6}H_{5}-CH=CH_{2}(g)+H_{2}(g) \Delta H_{1}$
近期科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图$1$所示(吸附在催化剂表面的物质用$*$标注):
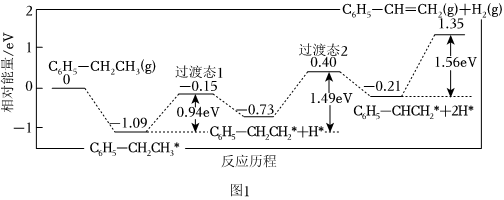
乙苯脱氢制苯乙烯反应的焓变$\Delta H_{1}$______$0(选填“大于”或“小于”或“等于”)$,该反应历程的决速步骤反应方程式为______。
$(2)$乙苯脱氢是合成苯乙烯的关键步骤。某温度下,向$2.0L$恒容密闭容器中充入$0.10molC_{6}H_{5}CH_{2}CH_{3}(g)$,测得乙苯脱氢反应时间$\left(t\right)$与容器内气体总压强$\left(p\right)$的数据见下表:
计算该温度下的平衡常数$K=\_\_\_\_\_\_(结果保留至小数点后两位)$。
$(3)$在$913K$、$100kPa$下,以水蒸气作稀释气。$Fe_{2}O_{3}$作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
反应乙:$C_{6}H_{5}C_{2}H_{5}(g)\rightleftharpoons C_{6}H_{6}(g)+CH_{2}=CH_{2}(g)$
反应丙:$C_{6}H_{5}C_{2}H_{5}(g)+H_{2}(g)\rightleftharpoons C_{6}H_{5}CH_{3}(g)+CH_{4}(g)$
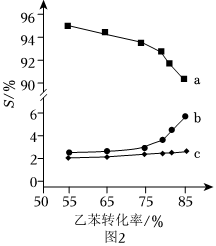
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性$S$随乙苯转化率的变化曲线如图$2$所示,其中曲线$b$代表的产物是______$,$理由是______。$(S=$转化为目的产物所消耗乙苯的量$\times 100\%)$
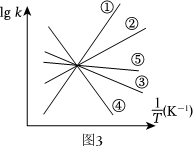
$(4)$实验测得,乙苯脱氢反应的速率方程为$v_{正}=k_{正}p_{乙苯}$,$v_{逆}=k_{逆}p_{苯乙烯}p_{氢气}(k_{正}$、$k_{逆}$为速率$\frac{1}{T}$常数,只与温度有关),图$3$中③代表$\lg k_{逆}$随$\frac{1}{T}$的变化关系,则能代表$\lg k_{正}$随$\frac{1}{T}$的变化关系的是______。
$Ⅱ$.苯乙烯的聚合
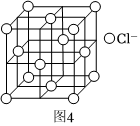
$(5)$苯乙烯聚合有多种方法,其中一种方法的关键步骤是某$Cu\left(I\right)$的配合物促进,$CuCl$是合成该$Cu\left(I\right)$的配合物的关键物质。在$CuCl$的晶胞中,$Cl^{-}$的位置如图$4$所示。$Cu^{+}$填充于$Cl^{-}$构成的四面体空隙中,则$Cu^{+}$的配位数为______;若$N_{A}$为阿伏加德罗常数的值,该晶体的密度为$\rho g\cdot cm^{-3}$,则该晶胞中$Cu^{+}$之间的距离为______$nm($用含$\rho $、$N_{A}$的代数式表示)。
$Ⅰ$.苯乙烯的制备
$(1)$工业常采用乙苯脱氢的方法制备苯乙烯,其原理如下:
反应甲:$C_{6}H_{5}-CH_{2}CH_{3}(g)\rightleftharpoons C_{6}H_{5}-CH=CH_{2}(g)+H_{2}(g) \Delta H_{1}$
近期科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图$1$所示(吸附在催化剂表面的物质用$*$标注):

乙苯脱氢制苯乙烯反应的焓变$\Delta H_{1}$______$0(选填“大于”或“小于”或“等于”)$,该反应历程的决速步骤反应方程式为______。
$(2)$乙苯脱氢是合成苯乙烯的关键步骤。某温度下,向$2.0L$恒容密闭容器中充入$0.10molC_{6}H_{5}CH_{2}CH_{3}(g)$,测得乙苯脱氢反应时间$\left(t\right)$与容器内气体总压强$\left(p\right)$的数据见下表:
| 时间$t/h$ | $0$ | $1$ | $2$ | $4$ | $8$ | $16$ | $20$ | $25$ | $30$ |
| 总压强$p/100kPa$ | $4.91$ | $5.58$ | $6.32$ | $7.31$ | $8.54$ | $9.50$ | $9.52$ | $9.53$ | $9.53$ |
$(3)$在$913K$、$100kPa$下,以水蒸气作稀释气。$Fe_{2}O_{3}$作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
反应乙:$C_{6}H_{5}C_{2}H_{5}(g)\rightleftharpoons C_{6}H_{6}(g)+CH_{2}=CH_{2}(g)$
反应丙:$C_{6}H_{5}C_{2}H_{5}(g)+H_{2}(g)\rightleftharpoons C_{6}H_{5}CH_{3}(g)+CH_{4}(g)$
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性$S$随乙苯转化率的变化曲线如图$2$所示,其中曲线$b$代表的产物是______$,$理由是______。$(S=$转化为目的产物所消耗乙苯的量$\times 100\%)$

$(4)$实验测得,乙苯脱氢反应的速率方程为$v_{正}=k_{正}p_{乙苯}$,$v_{逆}=k_{逆}p_{苯乙烯}p_{氢气}(k_{正}$、$k_{逆}$为速率$\frac{1}{T}$常数,只与温度有关),图$3$中③代表$\lg k_{逆}$随$\frac{1}{T}$的变化关系,则能代表$\lg k_{正}$随$\frac{1}{T}$的变化关系的是______。

$Ⅱ$.苯乙烯的聚合
$(5)$苯乙烯聚合有多种方法,其中一种方法的关键步骤是某$Cu\left(I\right)$的配合物促进,$CuCl$是合成该$Cu\left(I\right)$的配合物的关键物质。在$CuCl$的晶胞中,$Cl^{-}$的位置如图$4$所示。$Cu^{+}$填充于$Cl^{-}$构成的四面体空隙中,则$Cu^{+}$的配位数为______;若$N_{A}$为阿伏加德罗常数的值,该晶体的密度为$\rho g\cdot cm^{-3}$,则该晶胞中$Cu^{+}$之间的距离为______$nm($用含$\rho $、$N_{A}$的代数式表示)。

题目解答
答案
(1)乙苯脱氢制苯乙烯反应的焓变$\Delta H_{1}=\left(1.35eV-0eV\right)\times N_{A}mol^{-1}=1.35eV/mol$,由图可知,活化能最大的一步,反应速率最慢,是总反应的决速步,则该反应历程的决速步骤反应方程式为$C_{6}H_{5}-CHCH_{2}*+2H*=C_{6}H_{5}-CH=CH_{2}+H_{2}$,
故答案为:大于;$C_{6}H_{5}-CHCH_{2}*+2H*=C_{6}H_{5}-CH=CH_{2}+H_{2}$;
$(2)$恒温恒容条件下,气体的压强之比等于物质的量之比,则$\alpha ($乙苯$)=\frac{P-{P}_{0}}{P}×100\%=(\frac{P}{{P}_{0}}-1)×100\%$,平衡时,乙苯的转化率$\alpha =\frac{9.53-4.91}{4.91}×100\%=94.1\%$;在反应开始时$c(C_{6}H_{5}CH_{2}CH_{3})=0.050mol/L$,其平衡转化率为$94.1\%$,则根据反应方程式$C_{6}H_{5}CH_{2}CH_{3}(g)\rightleftharpoons C_{6}H_{5}CH=CH_{2}(g)+H_{2}(g)$可知:平衡时各种气体的浓度分别为:$c(C_{6}H_{5}CH_{2}CH_{3})=0.050mol/L\times \left(1-94.1\%\right)$,$c(C_{6}H_{5}CH=CH_{2})=c(H_{2})=0.050mol/L\times 94.1\%$,故该反应的化学平衡常数$K=\frac{c({C}_{6}{H}_{5}CH=C{H}_{2})c({H}_{2})}{c({C}_{6}{H}_{5}C{H}_{2}C{H}_{3})}=\frac{(0.050×94.1\%)^{2}}{0.050×(1-94.1\%)}mol/L=0.75mol/L$,
故答案为:$0.75$;
$(3)$反应甲为主反应,反应乙丙为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,反应乙正向移动,反应丙不移动,则曲线$b$代表产物苯,
故答案为:苯;反应甲为主反应,反应乙丙为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,反应乙正向移动,反应丙不移动,则曲线$b$代表产物苯;
$(4)$实验测得,乙苯脱氢的速率方程为$V_{正}=k_{正}p_{乙苯}$,$v_{逆}=k_{逆}p_{苯乙烯}p_{氢气}$,图$4$中③代表$\lg k_{逆}$随$\frac{1}{T}$的变化关系,达到平衡时,$V_{正}=V_{逆}$,即$k_{正}p_{乙苯}=k_{逆}p_{苯乙烯}p_{氢气}$,则有$\frac{{k}_{正}}{{k}_{_{逆}}}=\frac{{p}_{_{苯乙烯}}{p}_{_{氢气}}}{{p}_{乙苯}}=K$,由上题可知该反应正反应是一个吸热反应,故温度越高平衡正向移动,$K$增大,$\frac{1}{T}$越大,$T$越小,则$K$越小,③代表$\lg k_{逆}$随的变化关系,故能代表$\lg k_{正}$随$\frac{1}{T}$的变化关系的是④,
故答案为:④;
$(5)Cu^{+}$填充于$Cl^{-}$构成的四面体空隙中,则$Cu^{+}$的配位数为$4$;根据均摊原则,晶胞中$Cl^{-}$数为$8×\frac{1}{8}+6×\frac{1}{2}=4$,根据化学式,可知$Cu^{+}$数为$4$,若$N_{A}$为阿伏加德罗常数的值,设晶胞边长为$anm$,该晶体的密度为$pg\cdot cm^{-3}$,$\frac{4(64+35.5)}{{(a×1{0}^{-7})}^{3}×{N}_{A}}=ρ,a=\sqrt[3]{\frac{398}{ρ×{N}_{A}}}×1{0}^{7}$,则该晶胞中$Cu^{+}$之间的最短距离为面对角线的一半,距离为$\frac{\sqrt{2}}{2}×\sqrt[3]{\frac{398}{ρ{N}_{A}}}×1{0}^{7}nm$,
故答案为:$4$;$\frac{\sqrt{2}}{2}×\sqrt[3]{\frac{398}{ρ{N}_{A}}}×1{0}^{7}nm$。
故答案为:大于;$C_{6}H_{5}-CHCH_{2}*+2H*=C_{6}H_{5}-CH=CH_{2}+H_{2}$;
$(2)$恒温恒容条件下,气体的压强之比等于物质的量之比,则$\alpha ($乙苯$)=\frac{P-{P}_{0}}{P}×100\%=(\frac{P}{{P}_{0}}-1)×100\%$,平衡时,乙苯的转化率$\alpha =\frac{9.53-4.91}{4.91}×100\%=94.1\%$;在反应开始时$c(C_{6}H_{5}CH_{2}CH_{3})=0.050mol/L$,其平衡转化率为$94.1\%$,则根据反应方程式$C_{6}H_{5}CH_{2}CH_{3}(g)\rightleftharpoons C_{6}H_{5}CH=CH_{2}(g)+H_{2}(g)$可知:平衡时各种气体的浓度分别为:$c(C_{6}H_{5}CH_{2}CH_{3})=0.050mol/L\times \left(1-94.1\%\right)$,$c(C_{6}H_{5}CH=CH_{2})=c(H_{2})=0.050mol/L\times 94.1\%$,故该反应的化学平衡常数$K=\frac{c({C}_{6}{H}_{5}CH=C{H}_{2})c({H}_{2})}{c({C}_{6}{H}_{5}C{H}_{2}C{H}_{3})}=\frac{(0.050×94.1\%)^{2}}{0.050×(1-94.1\%)}mol/L=0.75mol/L$,
故答案为:$0.75$;
$(3)$反应甲为主反应,反应乙丙为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,反应乙正向移动,反应丙不移动,则曲线$b$代表产物苯,
故答案为:苯;反应甲为主反应,反应乙丙为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,反应乙正向移动,反应丙不移动,则曲线$b$代表产物苯;
$(4)$实验测得,乙苯脱氢的速率方程为$V_{正}=k_{正}p_{乙苯}$,$v_{逆}=k_{逆}p_{苯乙烯}p_{氢气}$,图$4$中③代表$\lg k_{逆}$随$\frac{1}{T}$的变化关系,达到平衡时,$V_{正}=V_{逆}$,即$k_{正}p_{乙苯}=k_{逆}p_{苯乙烯}p_{氢气}$,则有$\frac{{k}_{正}}{{k}_{_{逆}}}=\frac{{p}_{_{苯乙烯}}{p}_{_{氢气}}}{{p}_{乙苯}}=K$,由上题可知该反应正反应是一个吸热反应,故温度越高平衡正向移动,$K$增大,$\frac{1}{T}$越大,$T$越小,则$K$越小,③代表$\lg k_{逆}$随的变化关系,故能代表$\lg k_{正}$随$\frac{1}{T}$的变化关系的是④,
故答案为:④;
$(5)Cu^{+}$填充于$Cl^{-}$构成的四面体空隙中,则$Cu^{+}$的配位数为$4$;根据均摊原则,晶胞中$Cl^{-}$数为$8×\frac{1}{8}+6×\frac{1}{2}=4$,根据化学式,可知$Cu^{+}$数为$4$,若$N_{A}$为阿伏加德罗常数的值,设晶胞边长为$anm$,该晶体的密度为$pg\cdot cm^{-3}$,$\frac{4(64+35.5)}{{(a×1{0}^{-7})}^{3}×{N}_{A}}=ρ,a=\sqrt[3]{\frac{398}{ρ×{N}_{A}}}×1{0}^{7}$,则该晶胞中$Cu^{+}$之间的最短距离为面对角线的一半,距离为$\frac{\sqrt{2}}{2}×\sqrt[3]{\frac{398}{ρ{N}_{A}}}×1{0}^{7}nm$,
故答案为:$4$;$\frac{\sqrt{2}}{2}×\sqrt[3]{\frac{398}{ρ{N}_{A}}}×1{0}^{7}nm$。