题目
甲醇和乙醇形成的混合液可认为是理想物系,20℃时乙醇的蒸气压为5.93 kPa,甲醇为11.83kPa。试求:(1)两者各用100g液体,混合而成的溶液中甲醇和乙醇的摩尔分率各为多少?(2)气液平衡时系统的总压和各自的分压为多少?气相组成为多少?
甲醇和乙醇形成的混合液可认为是理想物系,20℃时乙醇的蒸气压为5.93 kPa,甲醇为11.83kPa。试求:
(1)两者各用100g液体,混合而成的溶液中甲醇和乙醇的摩尔分率各为多少?
(2)气液平衡时系统的总压和各自的分压为多少?气相组成为多少?
题目解答
答案
解 (1)甲醇摩尔质量MA=32kg/kmol,乙醇摩尔质量MB=46kg/kmol
甲醇的摩尔分率xA=100/32/(100/32+100/46)=0.59
乙醇的摩尔分率xB=1-0.59=0.41
(2)pA=pA°xA=11.83×0.59=6.98kPa
pB=pB°xB= 5.93×0.41=2.43 kPa
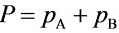 =9.41 kPa
=9.41 kPa
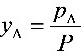 =6.98/9.41=0.74
=6.98/9.41=0.74
yB=1-0.74=0.26
解析
步骤 1:计算甲醇和乙醇的摩尔数
甲醇的摩尔质量为32g/mol,乙醇的摩尔质量为46g/mol。因此,100g甲醇的摩尔数为100g / 32g/mol = 3.125 mol,100g乙醇的摩尔数为100g / 46g/mol = 2.174 mol。
步骤 2:计算甲醇和乙醇的摩尔分率
甲醇的摩尔分率为3.125 mol / (3.125 mol + 2.174 mol) = 0.59,乙醇的摩尔分率为1 - 0.59 = 0.41。
步骤 3:计算气液平衡时的总压和各自的分压
根据拉乌尔定律,甲醇的分压为11.83 kPa * 0.59 = 6.98 kPa,乙醇的分压为5.93 kPa * 0.41 = 2.43 kPa。因此,系统的总压为6.98 kPa + 2.43 kPa = 9.41 kPa。
步骤 4:计算气相组成
气相中甲醇的摩尔分率为6.98 kPa / 9.41 kPa = 0.74,乙醇的摩尔分率为1 - 0.74 = 0.26。
甲醇的摩尔质量为32g/mol,乙醇的摩尔质量为46g/mol。因此,100g甲醇的摩尔数为100g / 32g/mol = 3.125 mol,100g乙醇的摩尔数为100g / 46g/mol = 2.174 mol。
步骤 2:计算甲醇和乙醇的摩尔分率
甲醇的摩尔分率为3.125 mol / (3.125 mol + 2.174 mol) = 0.59,乙醇的摩尔分率为1 - 0.59 = 0.41。
步骤 3:计算气液平衡时的总压和各自的分压
根据拉乌尔定律,甲醇的分压为11.83 kPa * 0.59 = 6.98 kPa,乙醇的分压为5.93 kPa * 0.41 = 2.43 kPa。因此,系统的总压为6.98 kPa + 2.43 kPa = 9.41 kPa。
步骤 4:计算气相组成
气相中甲醇的摩尔分率为6.98 kPa / 9.41 kPa = 0.74,乙醇的摩尔分率为1 - 0.74 = 0.26。