题目
2.1000K时,反应 (s)+2(H)_(2)(g)=C(H)_(4)(g) 的 (Delta )_(r)(G)_(m)^theta =19290Jcdot (mol)^-1 现有与-|||-碳反应的气体,其中含有CH4(g)10%,H2(g)80%,N 2(g)10%(体积%)。试问:-|||-(1) =1000K, =100kpa 时,甲烷能否 形 成?-|||-(2)在(1)的条件下,压力需增加到若干,上述合成甲烷的反应才可能进行?

题目解答
答案
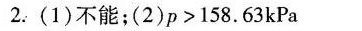
解析
步骤 1:计算反应的吉布斯自由能变化
反应 $C(s)+2{H}_{2}(g)=C{H}_{4}(g)$ 的标准吉布斯自由能变化 ${\Delta }_{r}{{G}_{m}}^{\theta }=19290J\cdot {mol}^{-1}$。这意味着在标准状态下,反应是不利的,因为吉布斯自由能变化为正值。
步骤 2:计算反应物和产物的分压
在给定的条件下,气体混合物中CH4(g)、H2(g)和N2(g)的体积百分比分别为10%、80%和10%。因此,当总压力为100kPa时,各组分的分压分别为:
- CH4(g)的分压:$p_{CH4} = 100kPa \times 10\% = 10kPa$
- H2(g)的分压:$p_{H2} = 100kPa \times 80\% = 80kPa$
- N2(g)的分压:$p_{N2} = 100kPa \times 10\% = 10kPa$
步骤 3:计算反应的吉布斯自由能变化
反应的吉布斯自由能变化可以表示为:
${\Delta }_{r}{{G}_{m}} = {\Delta }_{r}{{G}_{m}}^{\theta } + RT\ln Q$
其中,$Q$ 是反应商,对于反应 $C(s)+2{H}_{2}(g)=C{H}_{4}(g)$,$Q = \frac{p_{CH4}}{p_{H2}^2}$。将已知值代入,得到:
${\Delta }_{r}{{G}_{m}} = 19290J\cdot {mol}^{-1} + 8.314J\cdot {mol}^{-1}\cdot K^{-1} \times 1000K \times \ln \frac{10kPa}{(80kPa)^2}$
计算得到 ${\Delta }_{r}{{G}_{m}}$ 的值,判断反应是否能进行。
步骤 4:计算压力需增加到若干
当 ${\Delta }_{r}{{G}_{m}} = 0$ 时,反应达到平衡状态。此时,可以解出 $p_{H2}$ 的值,进而得到总压力 $p$ 的值。
反应 $C(s)+2{H}_{2}(g)=C{H}_{4}(g)$ 的标准吉布斯自由能变化 ${\Delta }_{r}{{G}_{m}}^{\theta }=19290J\cdot {mol}^{-1}$。这意味着在标准状态下,反应是不利的,因为吉布斯自由能变化为正值。
步骤 2:计算反应物和产物的分压
在给定的条件下,气体混合物中CH4(g)、H2(g)和N2(g)的体积百分比分别为10%、80%和10%。因此,当总压力为100kPa时,各组分的分压分别为:
- CH4(g)的分压:$p_{CH4} = 100kPa \times 10\% = 10kPa$
- H2(g)的分压:$p_{H2} = 100kPa \times 80\% = 80kPa$
- N2(g)的分压:$p_{N2} = 100kPa \times 10\% = 10kPa$
步骤 3:计算反应的吉布斯自由能变化
反应的吉布斯自由能变化可以表示为:
${\Delta }_{r}{{G}_{m}} = {\Delta }_{r}{{G}_{m}}^{\theta } + RT\ln Q$
其中,$Q$ 是反应商,对于反应 $C(s)+2{H}_{2}(g)=C{H}_{4}(g)$,$Q = \frac{p_{CH4}}{p_{H2}^2}$。将已知值代入,得到:
${\Delta }_{r}{{G}_{m}} = 19290J\cdot {mol}^{-1} + 8.314J\cdot {mol}^{-1}\cdot K^{-1} \times 1000K \times \ln \frac{10kPa}{(80kPa)^2}$
计算得到 ${\Delta }_{r}{{G}_{m}}$ 的值,判断反应是否能进行。
步骤 4:计算压力需增加到若干
当 ${\Delta }_{r}{{G}_{m}} = 0$ 时,反应达到平衡状态。此时,可以解出 $p_{H2}$ 的值,进而得到总压力 $p$ 的值。