21 . (1)① 下列各组物质性质的比较,结论正确的是 ________ 。 A.分子的极性:BCl33 B.Mn的+2价比Fe的+2价稳定 C.物质的沸点:HF D.在CS2中的溶解度:CCl42O ②MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,新生成的化学键为________键。NH3分子的空间构型为________,其中N原子的杂化轨道类型为________。 (2)下列叙述正确的有________。 A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7 B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性 D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点 (3)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是________、________。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是________,其中与乙二胺形成的化合物稳定性相对较高的是________(填“Mg2+”或“Cu2+”)。 (4)①FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为________,其中Fe的配位数为________。 ②苯胺(HN-1)与甲苯(HN-1)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。 (5)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X-射线衍射测得化合物R的晶体结构,其局部结构如图所示。 HN-1①从结构角度分析,R中两种阳离子的相同之处为________,不同之处为________。(填标号) A.中心原子的杂化轨道类型 B.中心原子的价层电子对数 C.立体结构 D.共价键类型 ②R中阴离子N中的σ键总数为________个。 ③图中虚线代表氢键,其表示式为(NH)N—H…Cl、________、________。
A.分子的极性:BCl3
B.Mn的+2价比Fe的+2价稳定
C.物质的沸点:HF
D.在CS2中的溶解度:CCl4
②MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,新生成的化学键为________键。NH3分子的空间构型为________,其中N原子的杂化轨道类型为________。
(2)下列叙述正确的有________。
A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性
D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点
(3)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是________、________。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是________,其中与乙二胺形成的化合物稳定性相对较高的是________(填“Mg2+”或“Cu2+”)。
(4)①FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为________,其中Fe的配位数为________。
②苯胺(![]() )与甲苯(
)与甲苯(![]() )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
(5)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X-射线衍射测得化合物R的晶体结构,其局部结构如图所示。
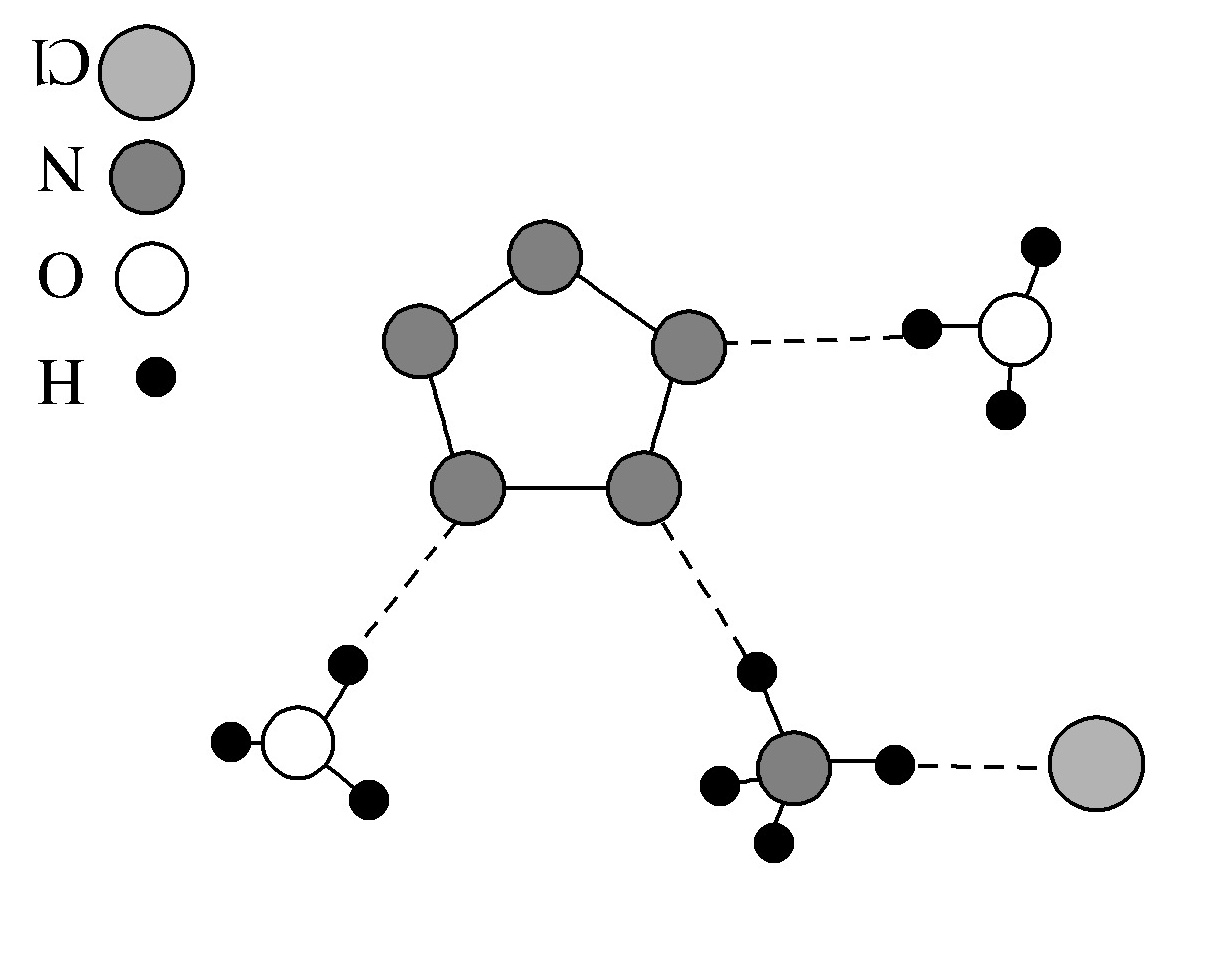
①从结构角度分析,R中两种阳离子的相同之处为________,不同之处为________。(填标号)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
②R中阴离子N中的σ键总数为________个。
③图中虚线代表氢键,其表示式为(NH)N—H…Cl、________、________。
题目解答
答案
(1)①AB ②配位 三角锥形 sp3
(2)AD
(3)sp3 sp3 乙二胺的两个N提供孤对电子与金属离子形成配位键 Cu2+
(4)①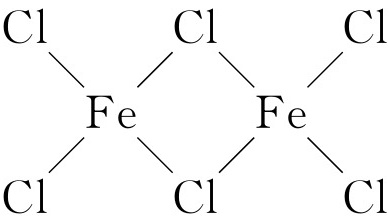 4 ②苯胺分子之间存在氢键 (5)①ABD C ②5
4 ②苯胺分子之间存在氢键 (5)①ABD C ②5
③(H3O+)O—H…N (NH)N—H…N