中和反应是化学核心概念之一。某化学兴趣小组对中和反应展开了探究。【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。【实验步骤】步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加 2 滴酚酞试液,溶液呈红色。步骤二:用仪器 A 吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至消失。步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。【思考拓展】(+ - 无水醋酸-|||-v-|||-- H^+-|||-- (int )_(a)^+1 NaOH固体 和变色硅胶-|||-OH^-) (int )(a)^+ H2O-|||-(int )(a)^+1 --|||-(int )_(a)^+1 OH^- H2O-|||-图1 图2(1)从下列仪器中选择步骤二中的“仪器 A”,名称是 。(+ - 无水醋酸-|||-v-|||-- H^+-|||-- (int )_(a)^+1 NaOH固体 和变色硅胶-|||-OH^-) (int )(a)^+ H2O-|||-(int )(a)^+1 --|||-(int )_(a)^+1 OH^- H2O-|||-图1 图2(2)兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。查阅资料:(i)酚酞试液在不同的pH时变化情况如下:(+ - 无水醋酸-|||-v-|||-- H^+-|||-- (int )_(a)^+1 NaOH固体 和变色硅胶-|||-OH^-) (int )(a)^+ H2O-|||-(int )(a)^+1 --|||-(int )_(a)^+1 OH^- H2O-|||-图1 图2(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是 。(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:(+ - 无水醋酸-|||-v-|||-- H^+-|||-- (int )_(a)^+1 NaOH固体 和变色硅胶-|||-OH^-) (int )(a)^+ H2O-|||-(int )(a)^+1 --|||-(int )_(a)^+1 OH^- H2O-|||-图1 图2【继续探究】(4)图1是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是 。(5)兴趣小组认为上述实验对反应实质缺少直观的验证。查阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。兴趣小组据此设计了图2实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。①U型管内液面左低右高说明该反应 热量(填写“放出”或“吸收”)。②无水醋酸由CH3COO−和H+构成。变色硅胶由蓝色变成红色的原因是 (用化学方程式表示)。
中和反应是化学核心概念之一。某化学兴趣小组对中和反应展开了探究。
【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加 2 滴酚酞试液,溶液呈红色。
步骤二:用仪器 A 吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至消失。
步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。
【思考拓展】
从下列仪器中选择步骤二中的“仪器 A”,名称是 。
兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。
查阅资料:(i)酚酞试液在不同的pH时变化情况如下:

(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。
兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是 。
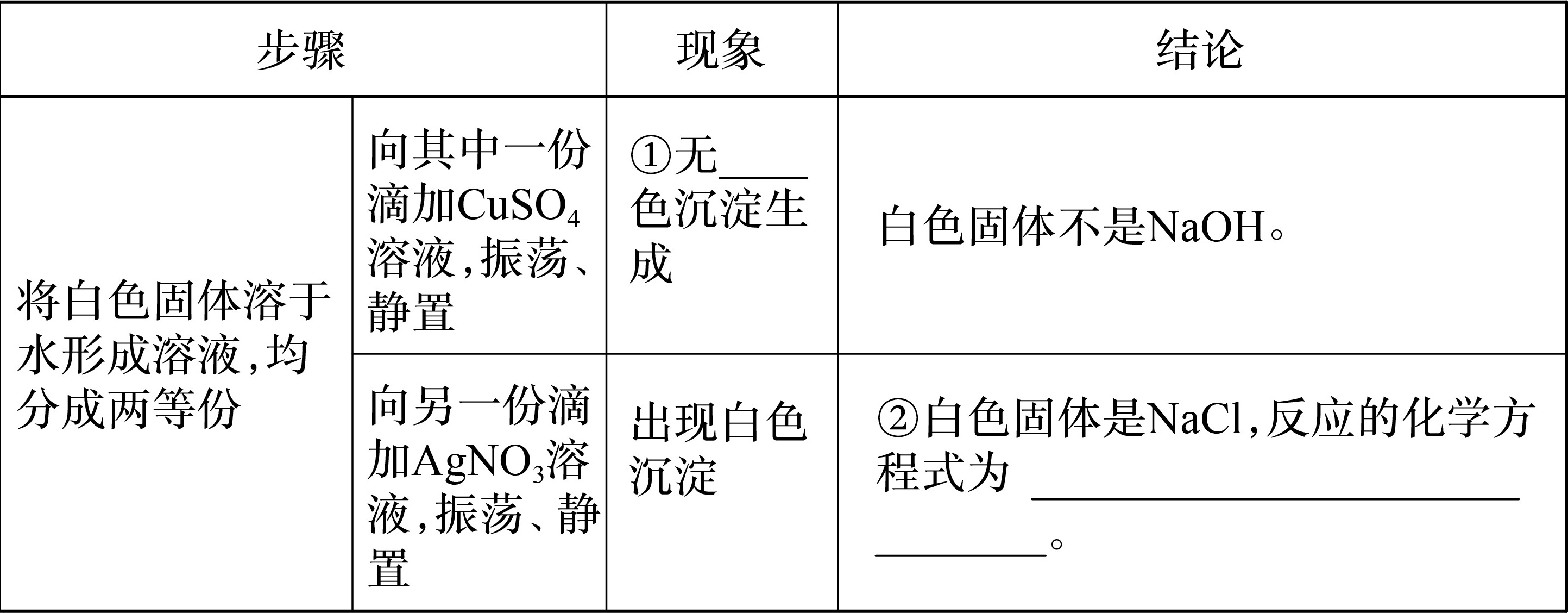
为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
【继续探究】
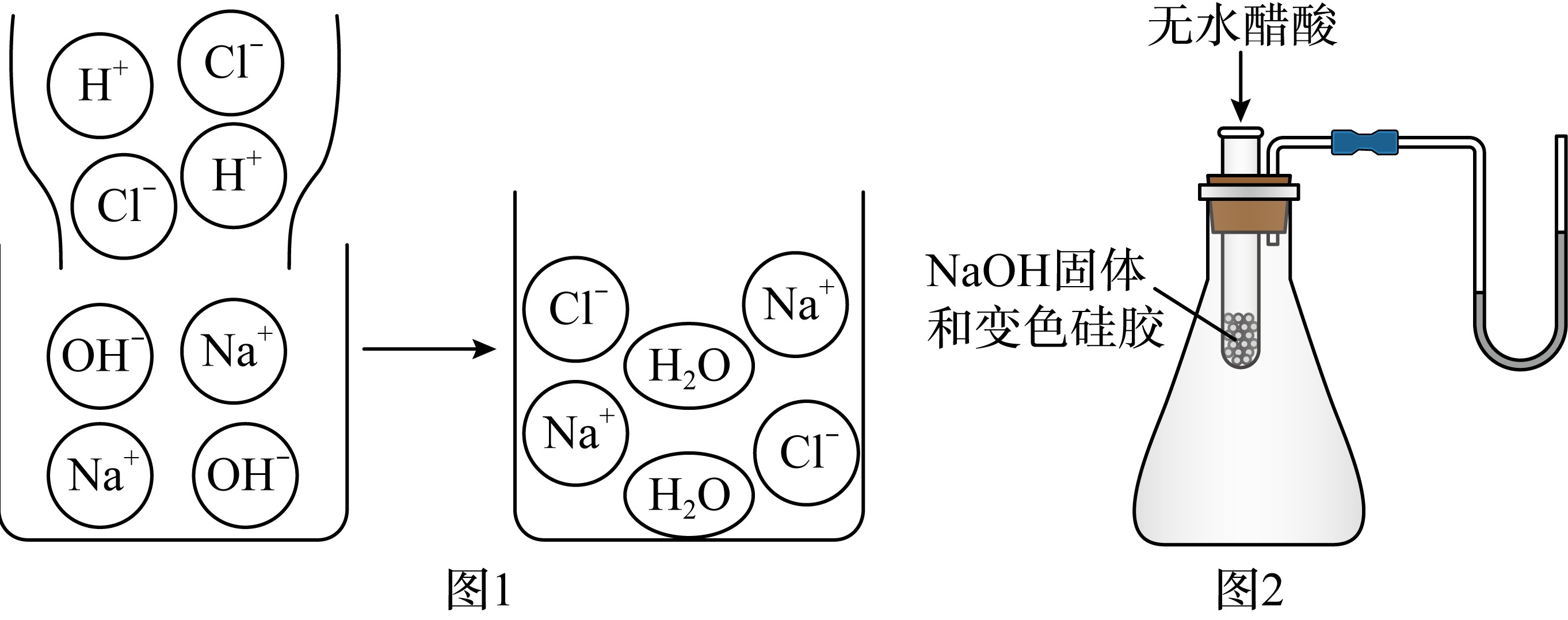
图1是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是 。
兴趣小组认为上述实验对反应实质缺少直观的验证。
查阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。
兴趣小组据此设计了图2实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。
①U型管内液面左低右高说明该反应 热量(填写“放出”或“吸收”)。
②无水醋酸由CH3COO−和H+构成。变色硅胶由蓝色变成红色的原因是 (用化学方程式表示)。
题目解答
答案
- (1)胶头滴管
- (2)用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响
- (3)蓝;NaCl+AgNO3===AgCl↓+NaNO3
- (4)H+和OH−结合生成H2O
- (5)放出;CH3COOH+NaOH===CH3COONa+H2O
解析
步骤二中需要逐滴加入稀盐酸,因此需要一种能够精确控制液体滴加量的仪器。胶头滴管是实验室中常用的滴加少量液体的工具,适合用于此实验。
【答案】
胶头滴管
(2)
【解析】
步骤 1:设计对比实验
兴趣小组认为仅从步骤二的现象难以证明盐酸与氢氧化钠发生了反应,因为红色消失可能是因为氢氧化钠溶液的浓度降低,而不是因为发生了化学反应。因此,需要设计一个对比实验,用相同量的蒸馏水代替稀盐酸进行步骤二实验,如果红色不消失,则可排除水的影响,从而证明盐酸与氢氧化钠确实发生了反应。
【答案】
用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响
(3)
【解析】
步骤 1:滴加CuSO4溶液
向其中一份溶液中滴加CuSO4溶液,振荡、静置,若无蓝色沉淀生成,则说明白色固体不是NaOH。
步骤 2:滴加AgNO3溶液
向另一份溶液中滴加AgNO3溶液,振荡、静置,若出现白色沉淀,则说明白色固体是NaCl,反应的化学方程式为NaCl + AgNO3 === AgCl↓ + NaNO3。
【答案】
蓝;NaCl + AgNO3 === AgCl↓ + NaNO3
(4)
【解析】
步骤 1:分析反应实质
从微观角度分析,氢氧化钠溶液和盐酸反应的实质是H+和OH−结合生成H2O。
【答案】
H+和OH−结合生成H2O
(5)
【解析】
步骤 1:分析U型管内液面变化
U型管内液面左低右高说明该反应放出热量。
步骤 2:分析变色硅胶变色原因
变色硅胶由蓝色变成红色的原因是无水醋酸与NaOH固体反应生成醋酸钠和水,化学方程式为CH3COOH + NaOH === CH3COONa + H2O。