第7章烃类选择性氧化7-1、分氧化过程得与作用及其特点。答:作用:可生产比原料价值更高得化学品,不仅能生产含氧化合物(醇、醛、酮、酸等),还可生产不含氧化物(丁二烯、丙烯腈等)。儿烁構劲厣頊缬。特点:(1)强放热反应。故反应热得移出就是很关键得问题,必须迅速地将热量移走,否则温度迅速上升,导致大量完全氧化反应发生,反应选择性显著下降,严重时可能导致反应温度无法控制,甚至发生爆炸。镉铭纜慪颔温雾。氧化反应放出得反应热可副产蒸汽,可回收能量。(2)反应不可逆。烃类及其它有机化合物得氧化反应得标准自由焓,故其平衡常数都很大,为不可逆反应,理论上转化率为100%,但就是为了保证较高得选择性,转化率需控制在一定范围内,否则会造成深度氧化而降低目得产物得产率。捡缑镖骓虽蘊龆。(3)氧化途径复杂多样因为目得产物都就是部分氧化中间产物,由于催化剂与反应条件得不同,氧化反应可经过不同得反应路径,转化为不同得反应产物,氧化得最终产物都就是CO2与水。这些中间产物往往比原料得反应性更强,更易发生深度氧化,因此要获得所需得目得产物,必须选用合适得催化剂与反应条件,而催化剂得选用就是决定氧化路径得关键。滎礡煙罌馋鰾轭。(4)过程易燃易爆烃类与氧或空气容易形成爆炸混合物,因此,氧化过程在设计与操作时应特别注意其安全性。7-12乙烯环氧化反应工艺条件选择得依据就是什么?答:(1)反应温度:完全氧化副反应具有强烈得竞争力,而影响竞争得主要外界因素就是反应温度。从动力学研究得到得结果就是:环氧化反应活化能小于完全氧化反应得活化能,故反应温度增高,两个反应得速率都加快,而完全氧化反应得速率增加更快。因此,选择性必然随温度得升高而下降。选择性下降,放出得热量就愈大,控制不好就会产生“飞温”。另外,温度过高,使催化剂得活性衰退,使用寿命下降。而温度过低,虽然可得到较多得环氧乙烷,但反应速率很小,无工业价值,故为达到环氧乙烷得收率最高,工业上一般选择反应温度在220~260℃。亙濫谇阒别凉騮。(2)空速:与反应温度相比,此因素就是次要得。空速减小,转化率提高,选择性下降;空速提高,可增大反应器中气体流动得线速度,减小气膜厚度,有利于传热。龜骜嵛炽摄洁鈦。工业上采用得空速与催化剂,反应器与传热速率有关,一般在4000-8000h-1左右。(3)反应压力由于氧化反应就是热力学上十分有利得反应,故压力对主副反应得平衡与选择性影响不大。但加压可提高乙烯与氧得分压,加快反应速率,提高反应器得生产能力,故工业上大都采用加压氧化法。然而压力不能过高,否则设备耐压要求提高,投资费用增加,因环氧乙烷在催化剂表面产生聚合与积碳,影响催化剂寿命。一般工业上采用2、0MPa左右。璽闯谩詁缫鲰顧。(4)原料配比及致稳气对于具有循环得乙烯环氧化过程,进入反应器得混合气由循环气与新鲜原料气混合形成,它得组成不仅影响过程得经济性,也与安全生产息息相关。趲兴鸳撐悶鹼膃。实际生产时,乙烯与O2得配比一定要在爆炸限以外。氧得含量必须低于爆炸极限浓度,乙烯得浓度也要控制。两者浓度过低时,催化剂得生产能力小;过高时,反应速度快,催化剂生产能力大,但单位时间释放得热量大,反应器得热负荷增大,若放热与移热不能平衡,就会造成飞温。因此,氧与乙烯得浓度都有一适宜值。鐙纯臠嚌巋栏钊。为了提高反应时乙烯与氧得浓度,可以用加入第三种气体来改变乙烯得爆炸限,这种气体通常称为致稳气。广泛采用N2,近年采用CH4。 紲衬櫥滥艫骡顷。(5)原料气纯度危害:①催化剂中毒。如硫(砷、卤)化物与乙炔。②增大反应热效应。H2、乙炔与烷(烯)烃发生燃烧反应,放出大量热,难以控制。同时,乙炔与高碳烯烃得存在加快催化剂表面得积碳失活。禄暫驱毁鳃缘压。③影响爆炸限。氩气与氢气含量过高,改变混合气体得爆炸限,降低氧气得最大容许浓度。④选择性下降。原料气与管道中带入得铁离子使环氧乙烷重排为乙醛。环氧乙烷在水吸收塔中要充分吸收,否则会由循环气带回反应器,使转化率明显下降。二氧化碳对环氧化反应有抑制作用,但适宜得含量会提高反应得选择性,提高氧得爆炸极限浓度。羁錒惻变哔摅淺。原料乙烯要求杂质含量:乙炔 <510-6 g/L,C3以上烃 <110-5 g/L,硫化物 <110-6 g/L,氯化物 <110-6 g/L, 氢气<510-6 g/L,二氧化碳 <9%。誉镔蕕齷衅鲮魯。(6)乙烯转化率单程转化率过高时,由于放热量大,温度升高快,会加快深度氧化,使环氧乙烷得选择性明显降低。过低时,因循环气量过大而导致能耗增加,也造成乙烯得损失。灃组緘监繩锋龜。7-13致稳气得作用就是什么?答:致稳气得作用有二:①致稳气就是惰性得,能减小混合气得爆炸限,增加体系安全性。②具有较高得比热容,能有效地移出部分反应热,增加体系稳定性。7-22为什么苯酐能在爆炸极限内生产?应采取哪些安全措施?答:因为邻二甲苯在常压下燃爆产生得压力约为0、6MPa,如果反应压力为0、15MPa,燃爆压力约为0、9MPa,这样不高得压力只要处理得当,不会造成危险,因此苯酐得生产工艺都就是在爆炸范围内操作,但必须有有效得安全防范措施。即:諗鲛顥鮚满拟鑊。①尽量缩小邻二甲苯与空气混合之处与进入装催化剂管之前得空间;②反应器壁厚略为加大,并装备防爆膜、安全阀;③采用大热容催化剂,使用高线速、防静电等措施。7-23何谓爆炸极限?其主要影响因素有哪些?答:烃类及其衍生物得气体或蒸气与空气或氧气形成混合物,在一定得浓度范围内,由于引火源如明火、高温或静电火花等因素得作用,该混合物会自动迅速发生支链型连锁反应,导致极短时间内体系温度与压力急剧上升,火焰迅速传播,最终发生爆炸。该浓度范围称为爆炸极限。栎頜銅飑狽锚鱍。爆炸极限主要与体系得温度、压力、组成等因素有关。催化剂使用时,必须在反应前对其进行活化,使其转化成具有活性得状态,应该严格按照操作规程进行活化,才能保证催化剂发挥良好得作用。黄潑嘔謫执詩峄。应严格控制操作条件:①采用结构合理得反应器,使反应温度在催化剂最佳使用温度范围内合理地分布,防止超温;②反应原料中得毒物杂质应该预先加以脱除,使毒物含量低于催化剂耐受值以下;③在有碳反应得体系中,应采用有利于防止碳得反应条件,并选用抗积碳性能高得催化剂。辋儉噓编錫傩猶。在运输与贮藏中应防止催化剂受污染与破坏;固体催化剂在装填时要防止污染与破裂,装填要均匀,避免“架桥”现象,以防止反应工况恶化;许多催化剂使用后,在停工卸出之前,需要进行钝化处理,以免烧坏催化剂与设备。鑼将豈綁鸳渙垦。2-10假设某天然气全就是甲烷,将其燃烧来加热一个管式炉,燃烧后烟道气得摩尔分数组成(干基)为86、4%N2、4、2%O2、9、4%CO2。试计算天然气与空气得摩尔比,并列出物料收支平衡表。憮礼掸赔莢瀲。
第7章烃类选择性氧化
7-1、分氧化过程得与作用及其特点。
答:作用:
可生产比原料价值更高得化学品,不仅能生产含氧化合物(醇、醛、酮、酸等),还可生产不含氧化物(丁二烯、丙烯腈等)。儿烁構劲厣頊缬。
特点:
(1)强放热反应。故反应热得移出就是很关键得问题,必须迅速地将热量移走,否则温度迅速上升,导致大量完全氧化反应发生,反应选择性显著下降,严重时可能导致反应温度无法控制,甚至发生爆炸。镉铭纜慪颔温雾。
氧化反应放出得反应热可副产蒸汽,可回收能量。
(2)反应不可逆。烃类及其它有机化合物得氧化反应得标准自由焓,故其平衡常数都很大,为不可逆反应,理论上转化率为100%,但就是为了保证较高得选择性,转化率需控制在一定范围内,否则会造成深度氧化而降低目得产物得产率。捡缑镖骓虽蘊龆。
(3)氧化途径复杂多样
因为目得产物都就是部分氧化中间产物,由于催化剂与反应条件得不同,氧化反应可经过不同得反应路径,转化为不同得反应产物,氧化得最终产物都就是CO2与水。这些中间产物往往比原料得反应性更强,更易发生深度氧化,因此要获得所需得目得产物,必须选用合适得催化剂与反应条件,而催化剂得选用就是决定氧化路径得关键。滎礡煙罌馋鰾轭。
(4)过程易燃易爆
烃类与氧或空气容易形成爆炸混合物,因此,氧化过程在设计与操作时应特别注意其安全性。
7-12乙烯环氧化反应工艺条件选择得依据就是什么?
答:(1)反应温度:
完全氧化副反应具有强烈得竞争力,而影响竞争得主要外界因素就是反应温度。从动力学研究得到得结果就是:环氧化反应活化能小于完全氧化反应得活化能,故反应温度增高,两个反应得速率都加快,而完全氧化反应得速率增加更快。因此,选择性必然随温度得升高而下降。选择性下降,放出得热量就愈大,控制不好就会产生“飞温”。另外,温度过高,使催化剂得活性衰退,使用寿命下降。而温度过低,虽然可得到较多得环氧乙烷,但反应速率很小,无工业价值,故为达到环氧乙烷得收率最高,工业上一般选择反应温度在220~260℃。亙濫谇阒别凉騮。
(2)空速:与反应温度相比,此因素就是次要得。空速减小,转化率提高,选择性下降;空速提高,可增大反应器中气体流动得线速度,减小气膜厚度,有利于传热。龜骜嵛炽摄洁鈦。
工业上采用得空速与催化剂,反应器与传热速率有关,一般在4000-8000h-1左右。
(3)反应压力
由于氧化反应就是热力学上十分有利得反应,故压力对主副反应得平衡与选择性影响不大。但加压可提高乙烯与氧得分压,加快反应速率,提高反应器得生产能力,故工业上大都采用加压氧化法。然而压力不能过高,否则设备耐压要求提高,投资费用增加,因环氧乙烷在催化剂表面产生聚合与积碳,影响催化剂寿命。一般工业上采用2、0MPa左右。璽闯谩詁缫鲰顧。
(4)原料配比及致稳气
对于具有循环得乙烯环氧化过程,进入反应器得混合气由循环气与新鲜原料气混合形成,它得组成不仅影响过程得经济性,也与安全生产息息相关。趲兴鸳撐悶鹼膃。
实际生产时,乙烯与O2得配比一定要在爆炸限以外。氧得含量必须低于爆炸极限浓度,乙烯得浓度也要控制。两者浓度过低时,催化剂得生产能力小;过高时,反应速度快,催化剂生产能力大,但单位时间释放得热量大,反应器得热负荷增大,若放热与移热不能平衡,就会造成飞温。因此,氧与乙烯得浓度都有一适宜值。鐙纯臠嚌巋栏钊。
为了提高反应时乙烯与氧得浓度,可以用加入第三种气体来改变乙烯得爆炸限,这种气体通常称为致稳气。广泛采用N2,近年采用CH4。 紲衬櫥滥艫骡顷。
(5)原料气纯度
危害:①催化剂中毒。如硫(砷、卤)化物与乙炔。
②增大反应热效应。H2、乙炔与烷(烯)烃发生燃烧反应,放出大量热,难以控制。同时,乙炔与高碳烯烃得存在加快催化剂表面得积碳失活。禄暫驱毁鳃缘压。
③影响爆炸限。氩气与氢气含量过高,改变混合气体得爆炸限,降低氧气得最大容许浓度。
④选择性下降。原料气与管道中带入得铁离子使环氧乙烷重排为乙醛。
环氧乙烷在水吸收塔中要充分吸收,否则会由循环气带回反应器,使转化率明显下降。二氧化碳对环氧化反应有抑制作用,但适宜得含量会提高反应得选择性,提高氧得爆炸极限浓度。羁錒惻变哔摅淺。
原料乙烯要求杂质含量:
乙炔 <510-6 g/L,C3以上烃 <110-5 g/L,硫化物 <110-6 g/L,氯化物 <110-6 g/L, 氢气<510-6 g/L,二氧化碳 <9%。誉镔蕕齷衅鲮魯。
(6)乙烯转化率
单程转化率过高时,由于放热量大,温度升高快,会加快深度氧化,使环氧乙烷得选择性明显降低。过低时,因循环气量过大而导致能耗增加,也造成乙烯得损失。灃组緘监繩锋龜。
7-13致稳气得作用就是什么?
答:致稳气得作用有二:
①致稳气就是惰性得,能减小混合气得爆炸限,增加体系安全性。
②具有较高得比热容,能有效地移出部分反应热,增加体系稳定性。
7-22为什么苯酐能在爆炸极限内生产?应采取哪些安全措施?
答:因为邻二甲苯在常压下燃爆产生得压力约为0、6MPa,如果反应压力为0、15MPa,燃爆压力约为0、9MPa,这样不高得压力只要处理得当,不会造成危险,因此苯酐得生产工艺都就是在爆炸范围内操作,但必须有有效得安全防范措施。即:諗鲛顥鮚满拟鑊。
①尽量缩小邻二甲苯与空气混合之处与进入装催化剂管之前得空间;
②反应器壁厚略为加大,并装备防爆膜、安全阀;
③采用大热容催化剂,使用高线速、防静电等措施。
7-23何谓爆炸极限?其主要影响因素有哪些?
答:烃类及其衍生物得气体或蒸气与空气或氧气形成混合物,在一定得浓度范围内,由于引火源如明火、高温或静电火花等因素得作用,该混合物会自动迅速发生支链型连锁反应,导致极短时间内体系温度与压力急剧上升,火焰迅速传播,最终发生爆炸。该浓度范围称为爆炸极限。栎頜銅飑狽锚鱍。
爆炸极限主要与体系得温度、压力、组成等因素有关。
催化剂使用时,必须在反应前对其进行活化,使其转化成具有活性得状态,应该严格按照操作规程进行活化,才能保证催化剂发挥良好得作用。黄潑嘔謫执詩峄。
应严格控制操作条件:①采用结构合理得反应器,使反应温度在催化剂最佳使用温度范围内合理地分布,防止超温;②反应原料中得毒物杂质应该预先加以脱除,使毒物含量低于催化剂耐受值以下;③在有碳反应得体系中,应采用有利于防止碳得反应条件,并选用抗积碳性能高得催化剂。辋儉噓编錫傩猶。
在运输与贮藏中应防止催化剂受污染与破坏;固体催化剂在装填时要防止污染与破裂,装填要均匀,避免“架桥”现象,以防止反应工况恶化;许多催化剂使用后,在停工卸出之前,需要进行钝化处理,以免烧坏催化剂与设备。鑼将豈綁鸳渙垦。
2-10假设某天然气全就是甲烷,将其燃烧来加热一个管式炉,燃烧后烟道气得摩尔分数组成(干基)为86、4%N2、4、2%O2、9、4%CO2。试计算天然气与空气得摩尔比,并列出物料收支平衡表。憮礼掸赔莢瀲。
题目解答
答案
:设烟道气(干基)得量为100mol。
反应式: CH4 + 2O2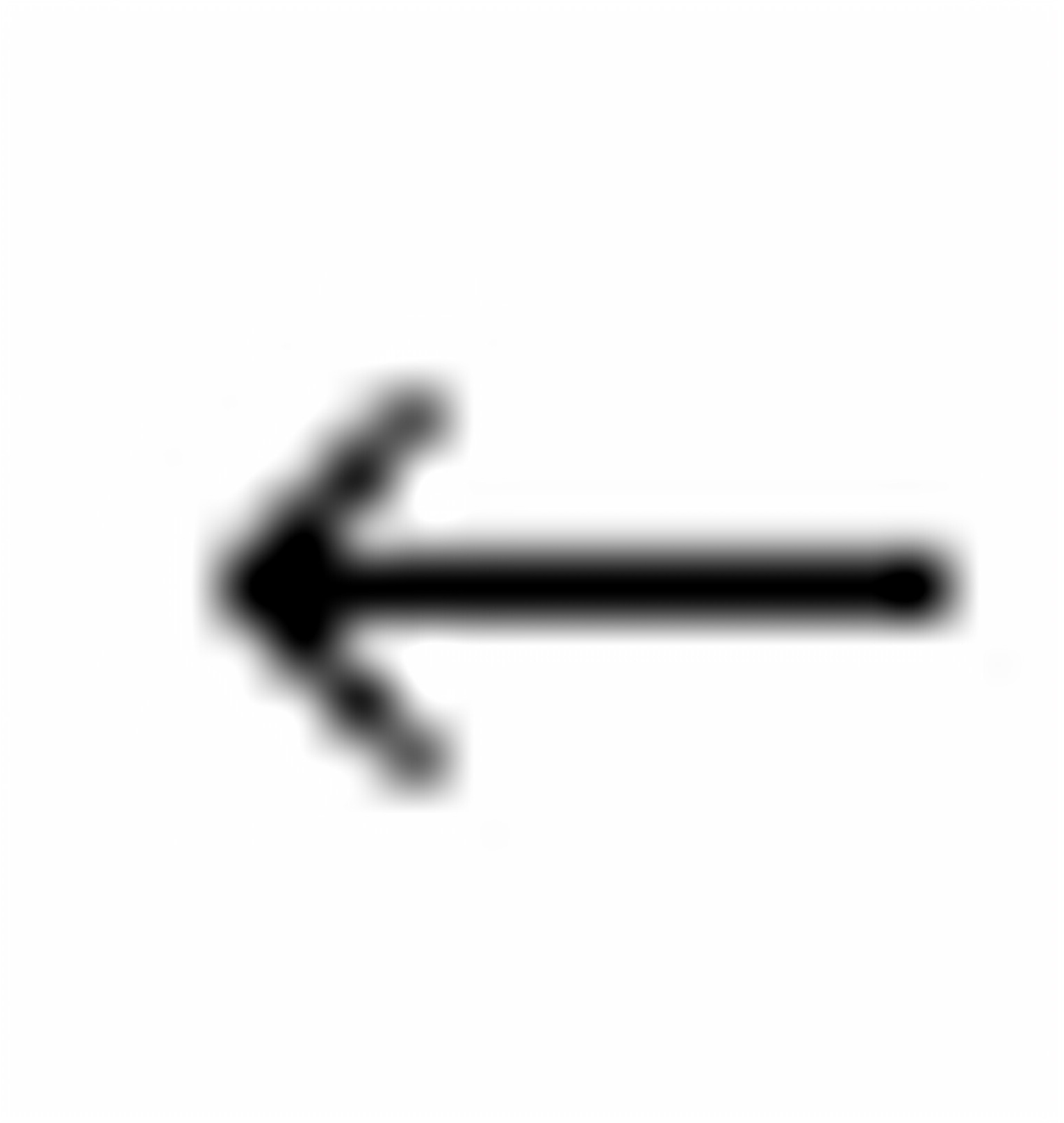 CO2 + 2H2O
CO2 + 2H2O
分子量: 16 32 44 18
反应转化得量: 9、4 2×9、4 9、4 2×9、4
则产物得量为:N2:86、4mol×28=2419、2 g
O2:4、2mol×32=134、4 g
CO2:9、4mol×44=413、6 g
H2O :2×9、4mol×18=338、4 g
原料得量为:N2:86、4mol×28=2419、2 g
O2:(4、2+2×9、4)mol×32=736 g
CH4:9、4mol×16=150、4g
CH4/空气(摩尔比)=9、4/(86、4+23)×100%=8、6%
列物料衡算表得
组分 | 输入 | 输出 | ||||||
mol | mol% | g | Wt% | mol | mol% | g | Wt% | |
N2 | 86、4 | 72、7 | 2419、2 | 73、2 | 86、4 | 72、7 | 2419、2 | 73、2 |
O2 | 23 | 19、4 | 736 | 22、3 | 4、2 | 3、5 | 134、4 | 4、1 |
H2O | 18、8 | 15、8 | 338、4 | 10、2 | ||||
CH4 | 9、4 | 7、9 | 150、4 | 4、5 | ||||
CO2 | 9、4 | 7、9 | 413、6 | 12、5 | ||||
∑ | 118、8 | 100、 | 3305、6 | 100、 | 118、8 | 99、9 | 3305、6 | 100、 |
2-13一氧化碳与水蒸气发生得变换反应为CO+H2O CO2+H2,若初始混合原料得摩尔比为H2O/CO=2/1,反应在500℃进行,此温度下反应得平衡常数Kp=P(CO2)·P(H2)/P(H2O)·P(CO)=4、88,求反应后混合物得平衡组成与CO得平衡转化率。們叠屆荛纪纈驃。
CO2+H2,若初始混合原料得摩尔比为H2O/CO=2/1,反应在500℃进行,此温度下反应得平衡常数Kp=P(CO2)·P(H2)/P(H2O)·P(CO)=4、88,求反应后混合物得平衡组成与CO得平衡转化率。們叠屆荛纪纈驃。
:设初始原料中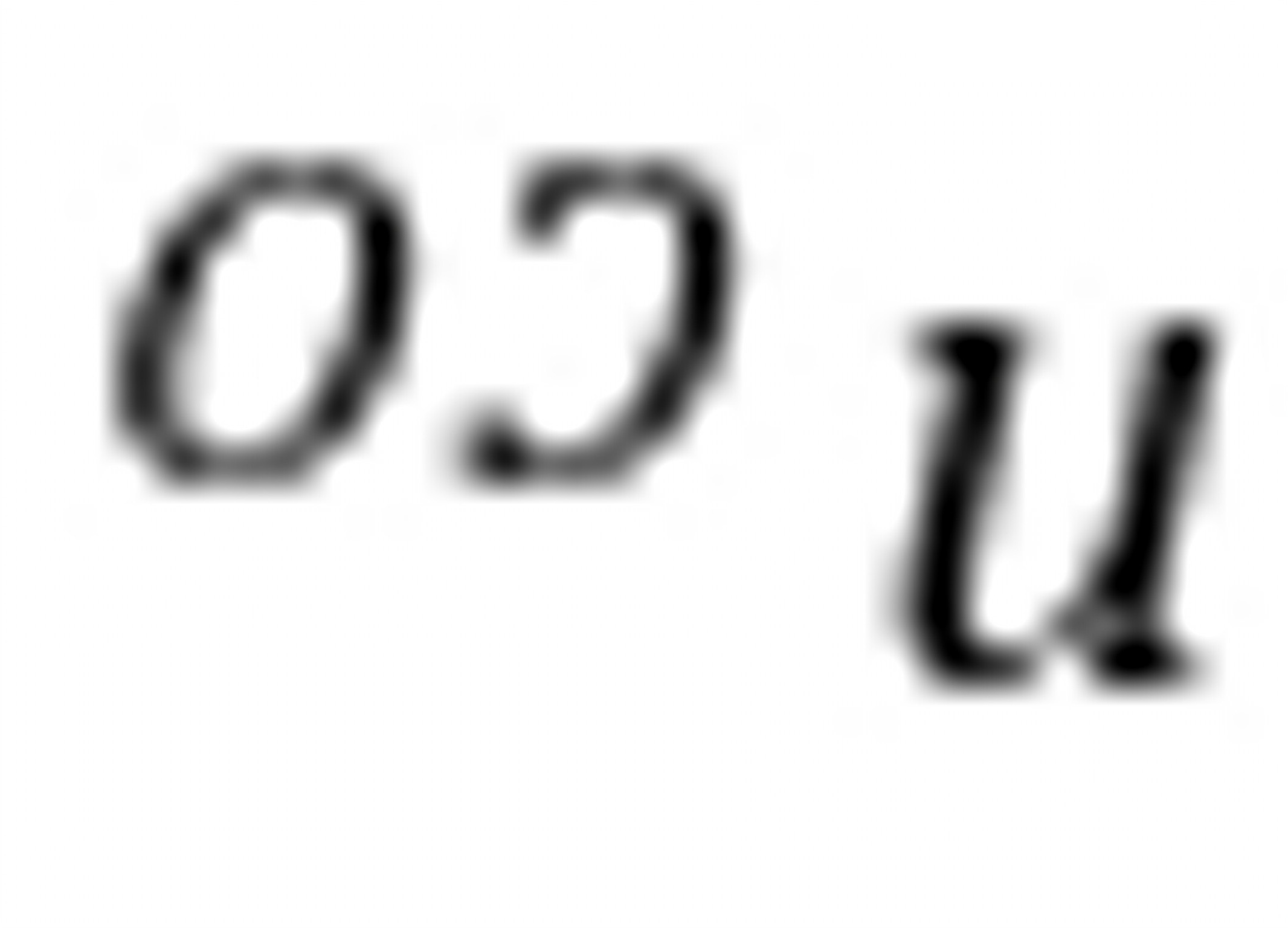 =1mol,则
=1mol,则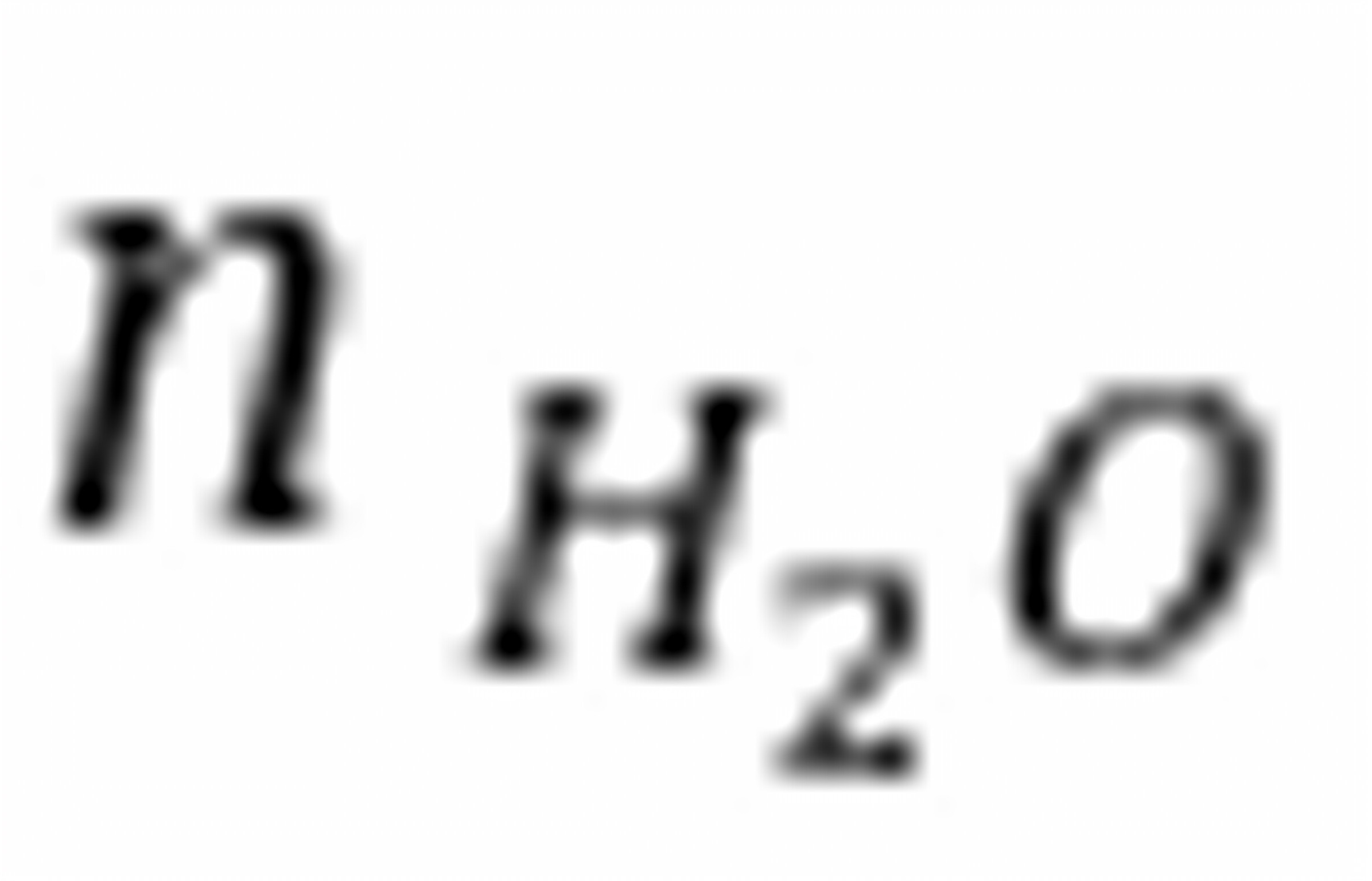 =2mol,达到平衡时,CO转化了m mol。
=2mol,达到平衡时,CO转化了m mol。
由 CO + H2O CO2+ H2
CO2+ H2
转化量 m m m m
平衡时 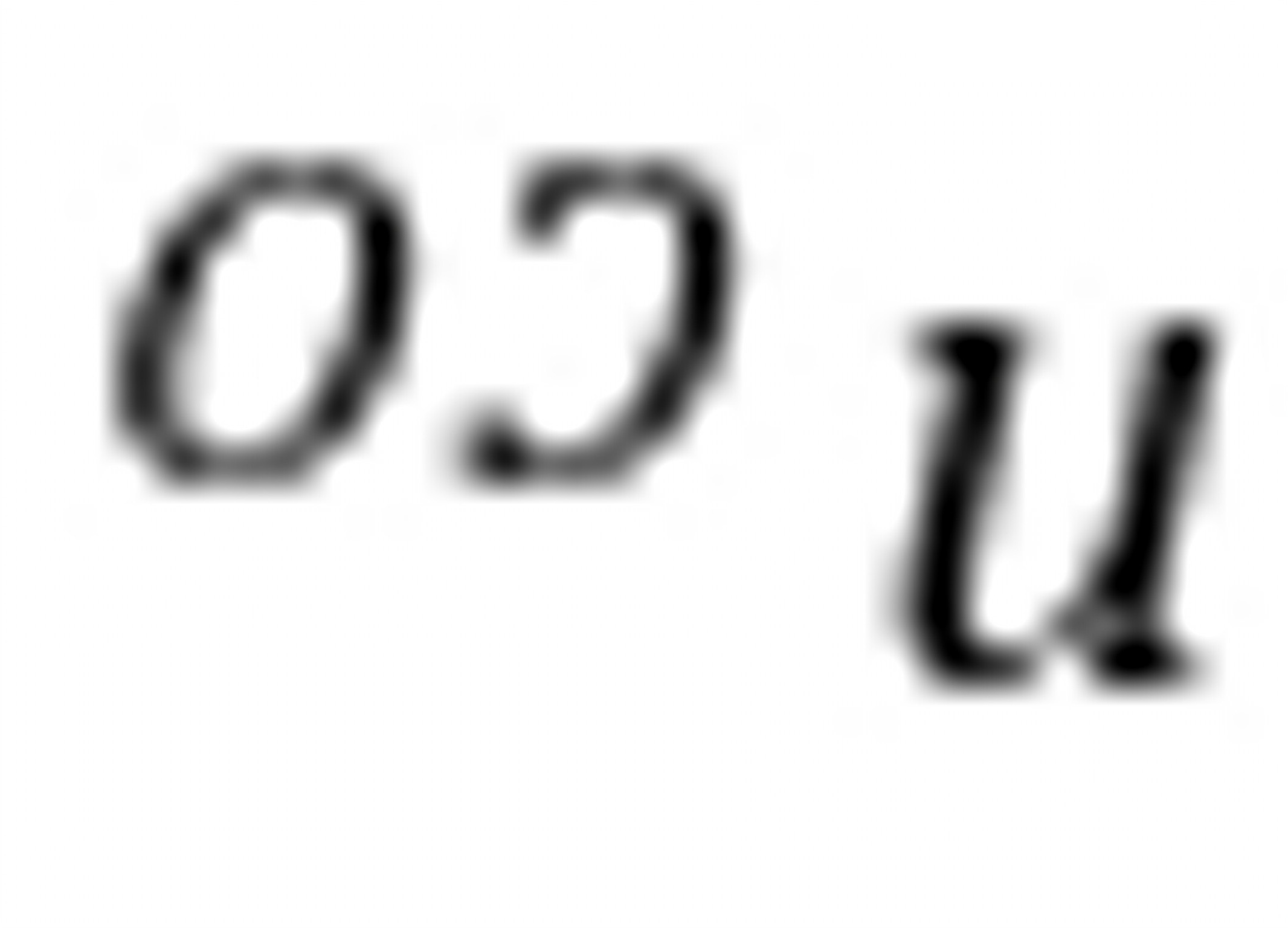 =1-m
=1-m 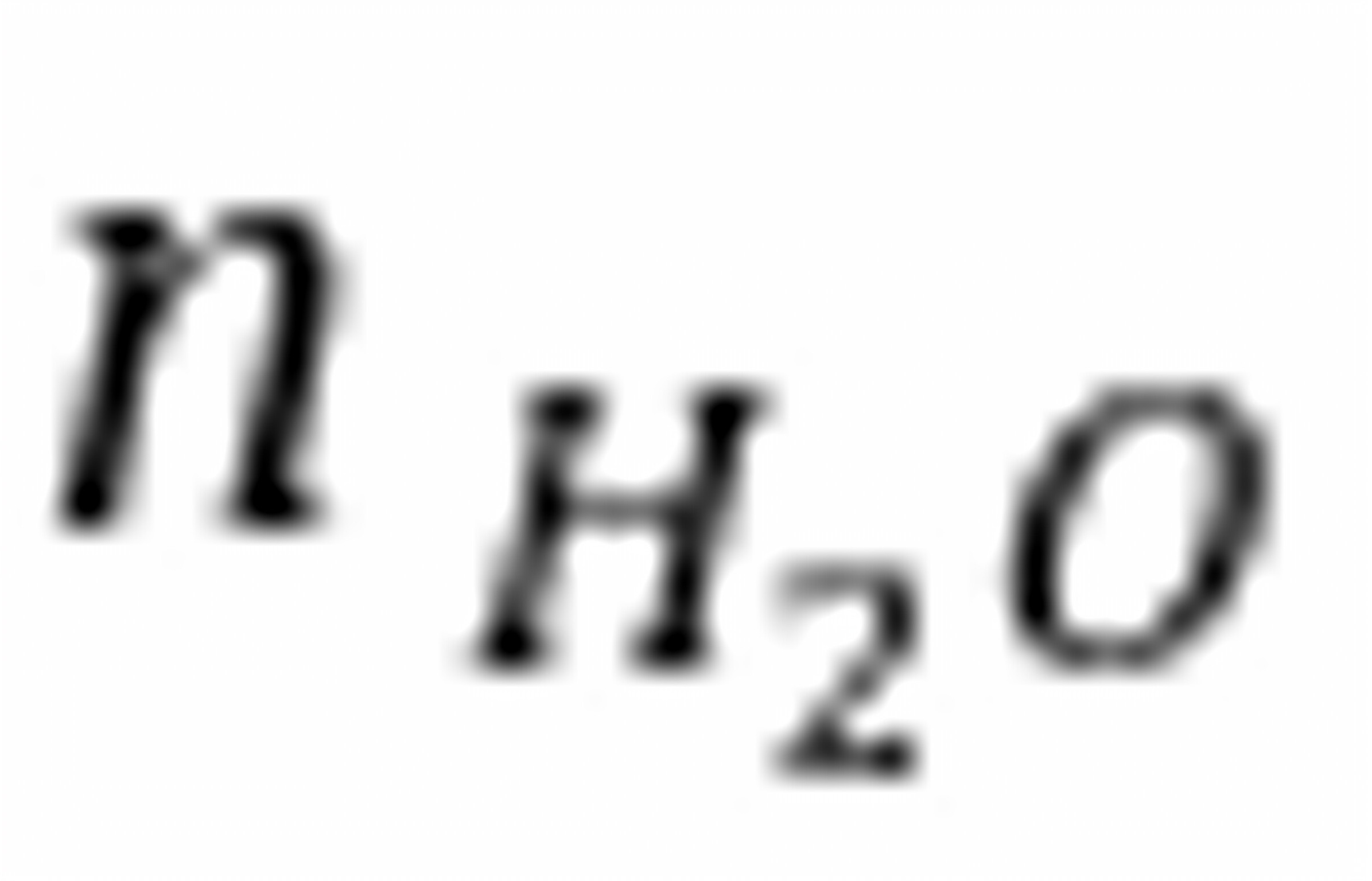 =2-m 生成
=2-m 生成 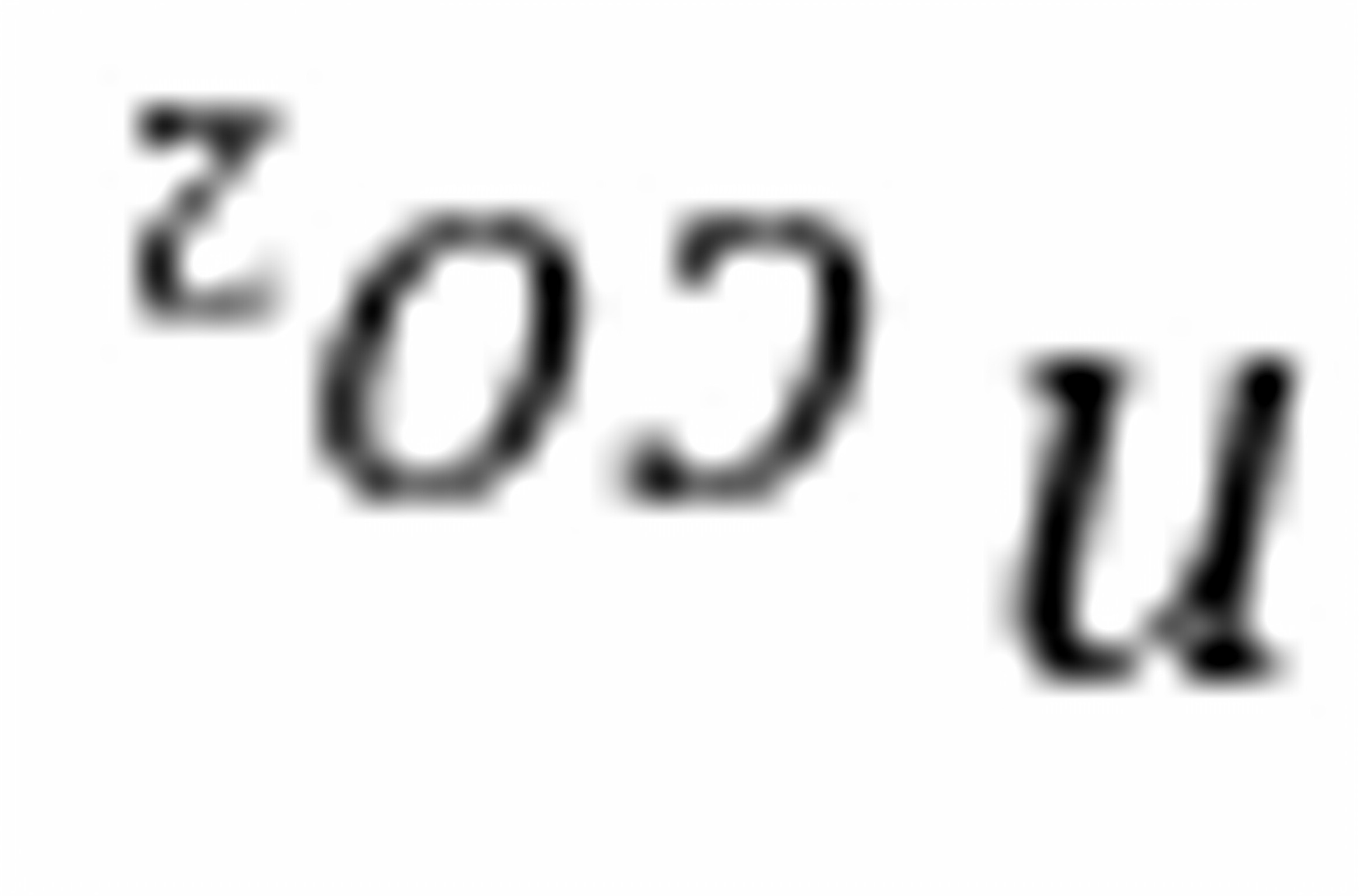 =
=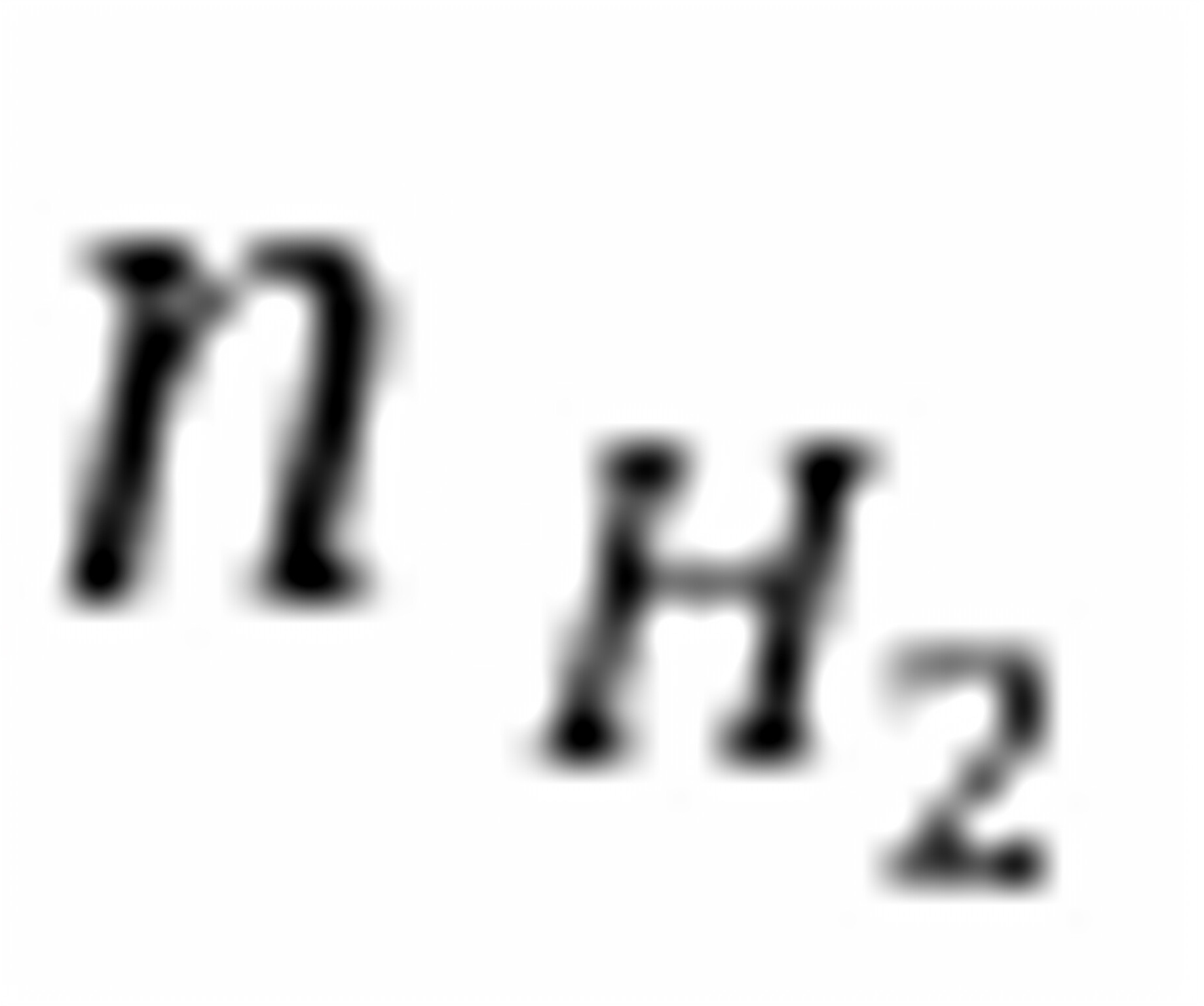 = m 产物总量n =∑
= m 产物总量n =∑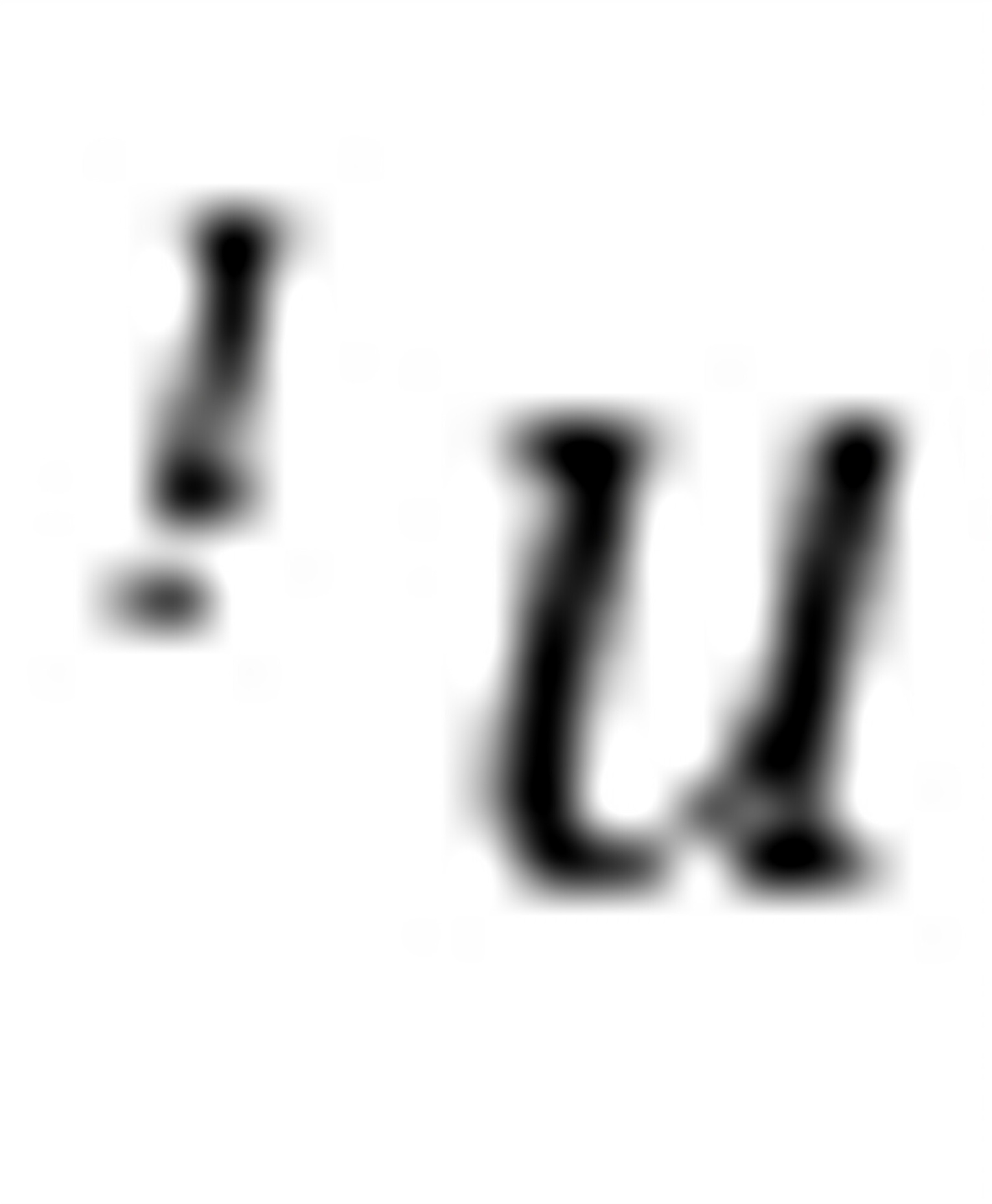 =3
=3 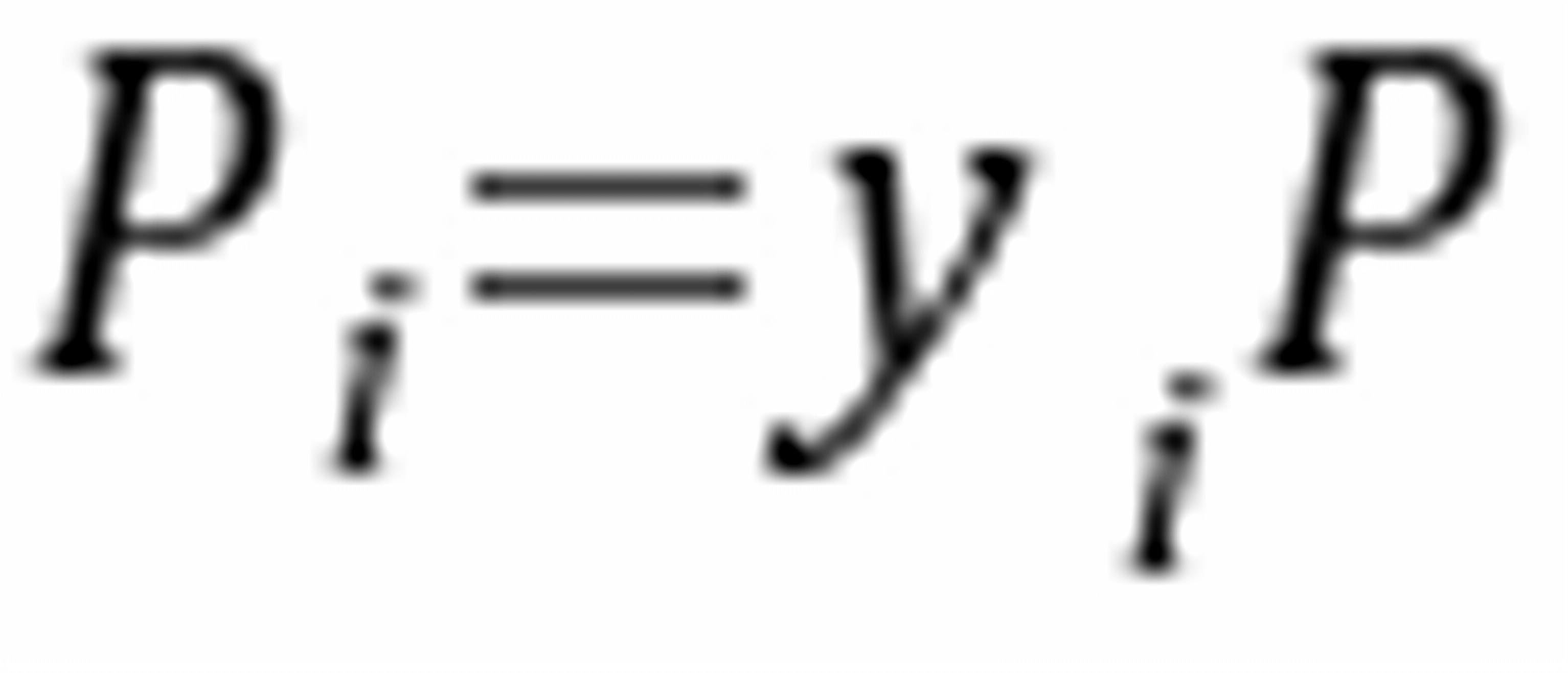 ,平衡时
,平衡时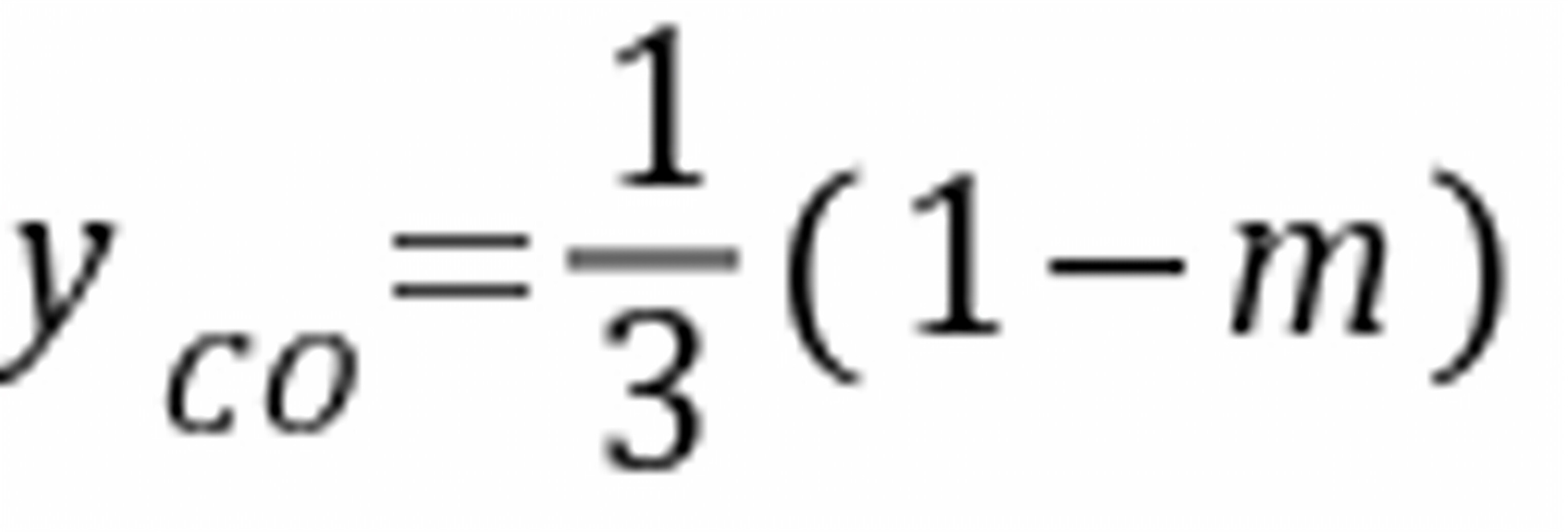
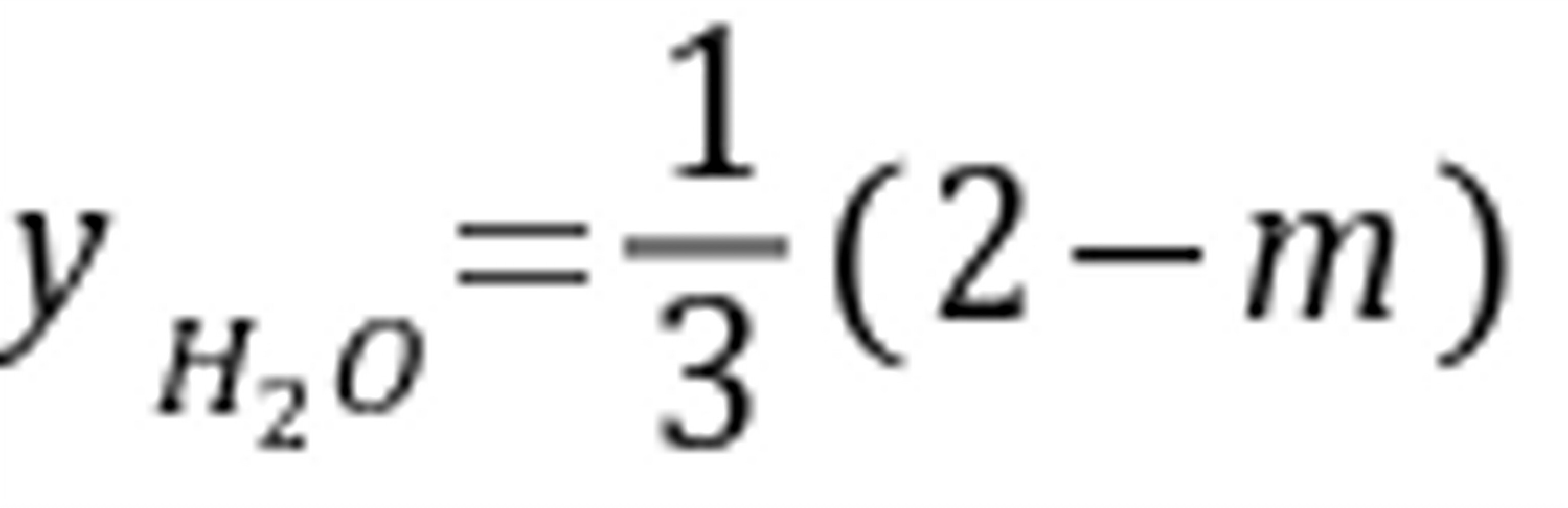
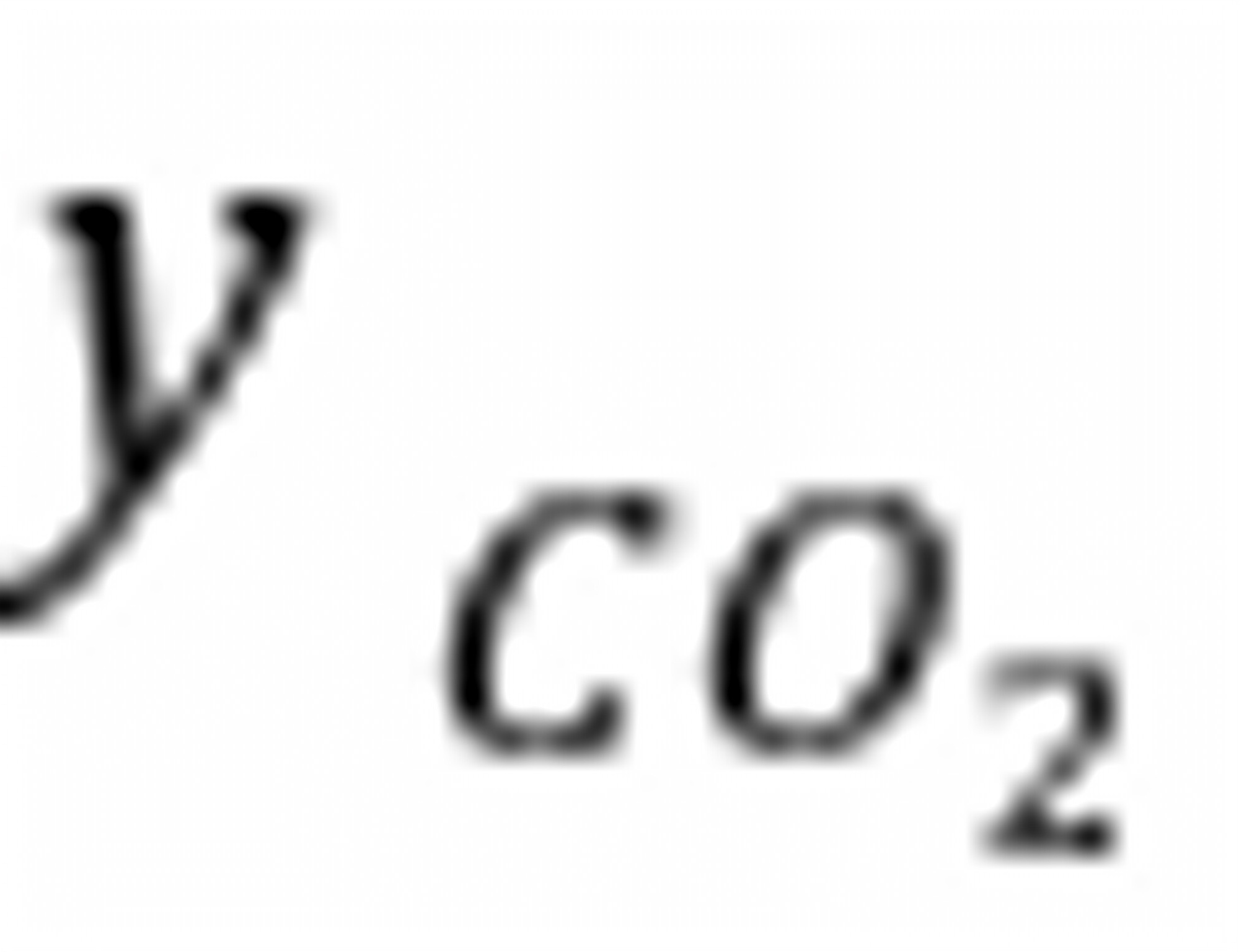 =
=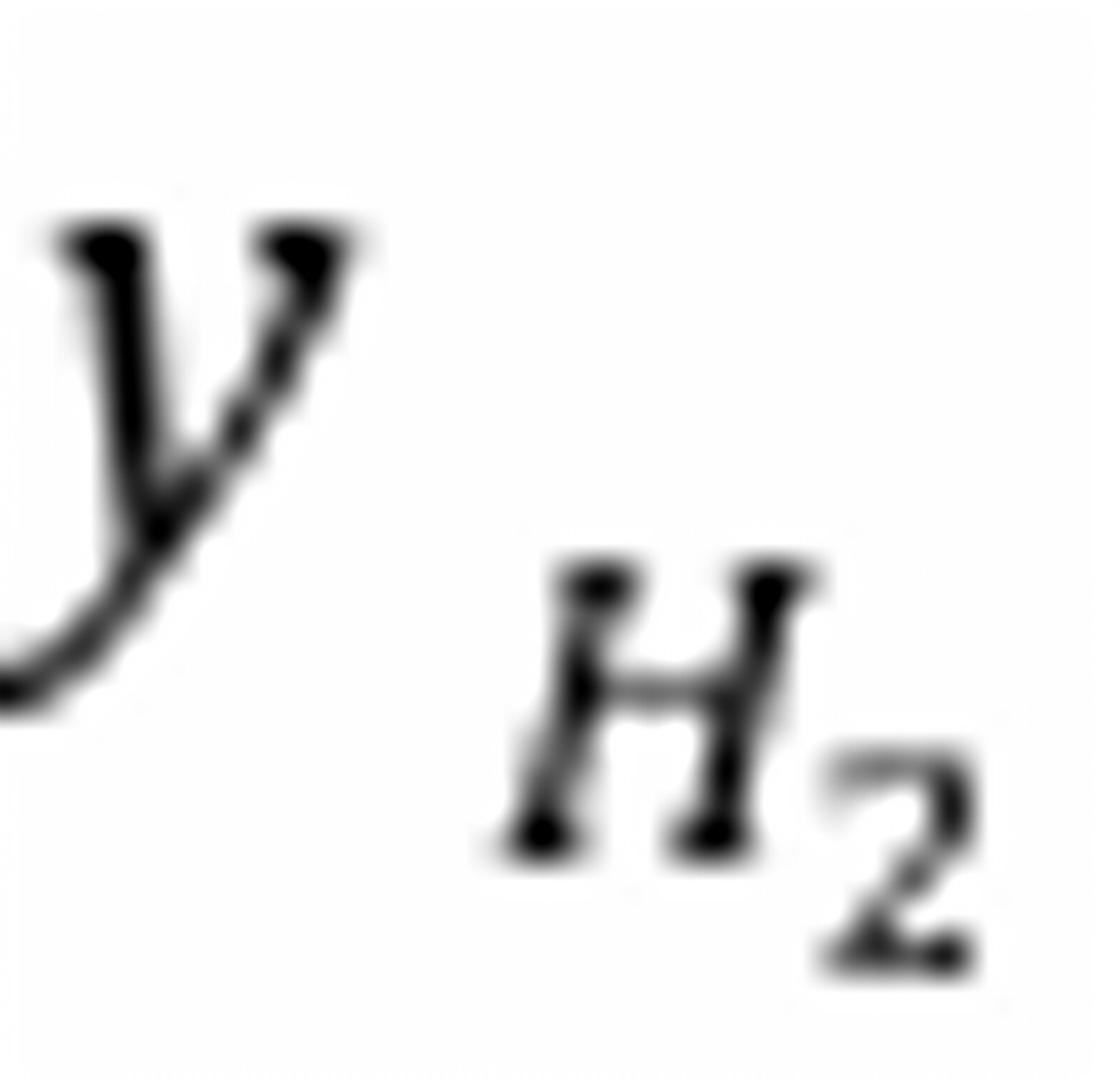 = m/3 沧臠嶼侣锞祷镣。
= m/3 沧臠嶼侣锞祷镣。
由4、88=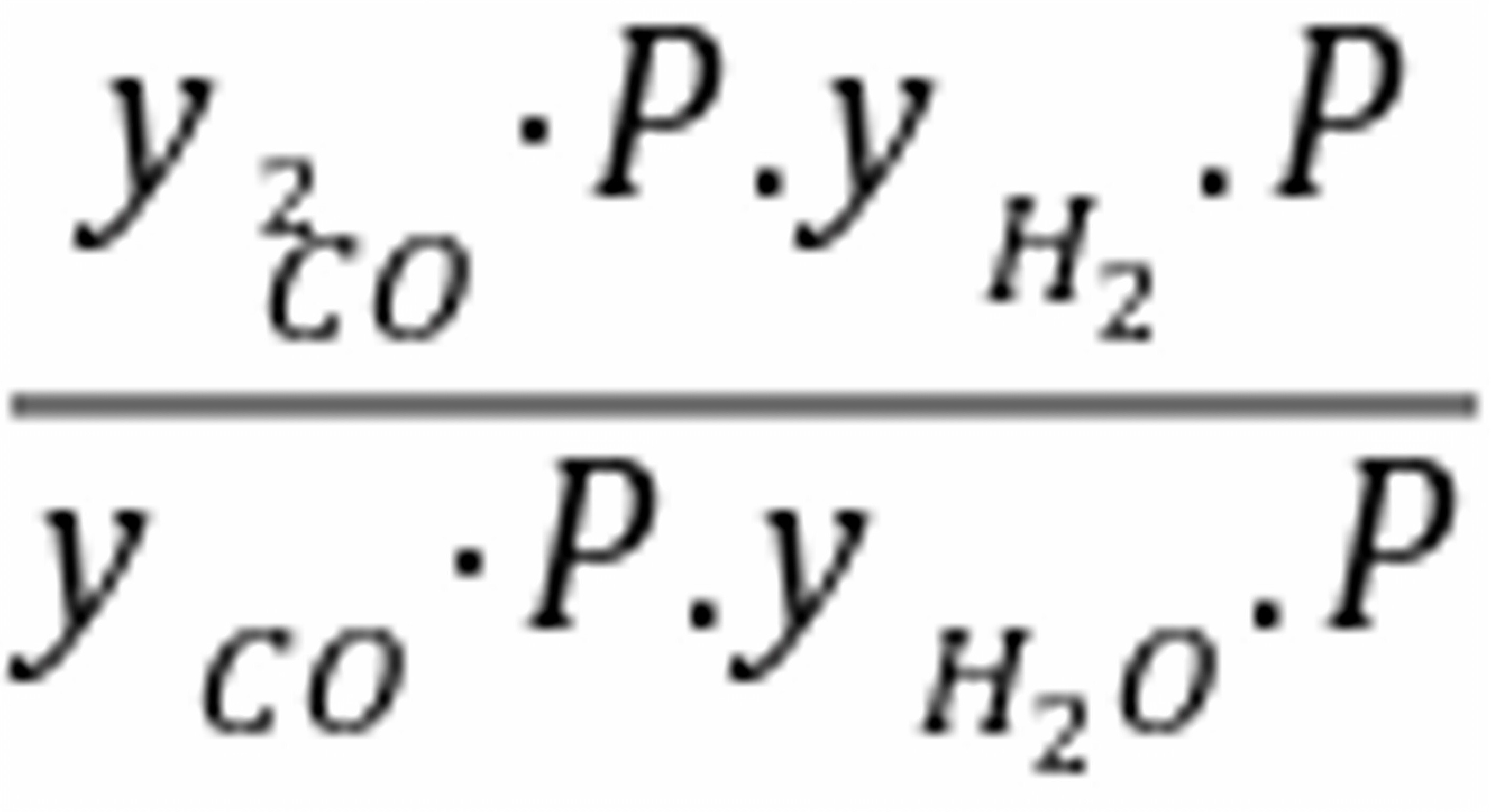 =
=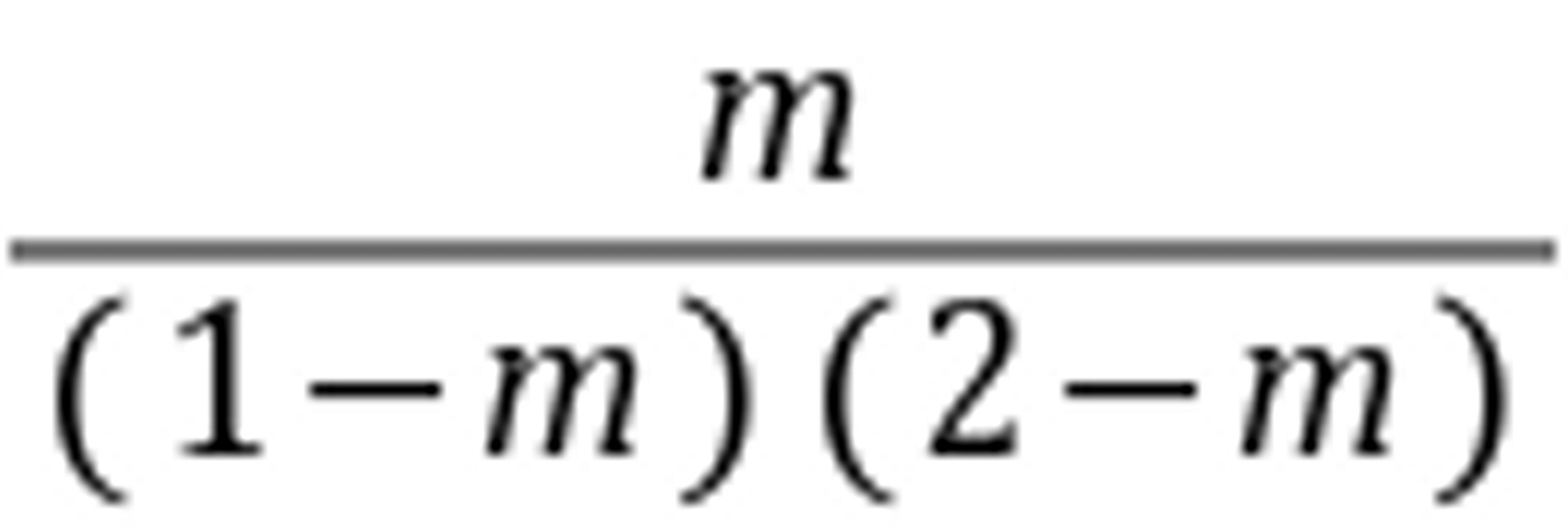 得m=0、865 Xco=0、865/1=86、5%
得m=0、865 Xco=0、865/1=86、5%
平衡组成: 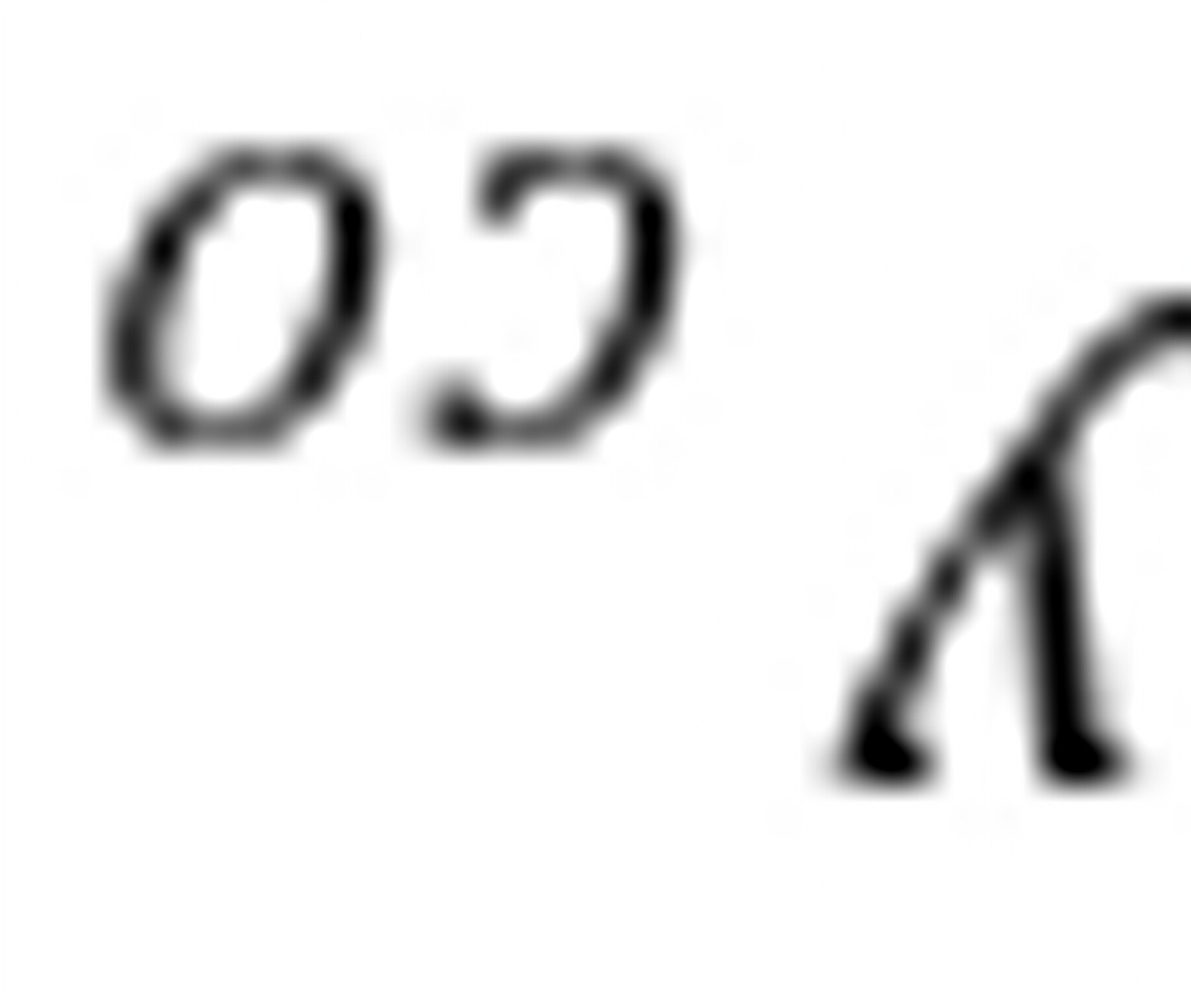 =0、045
=0、045 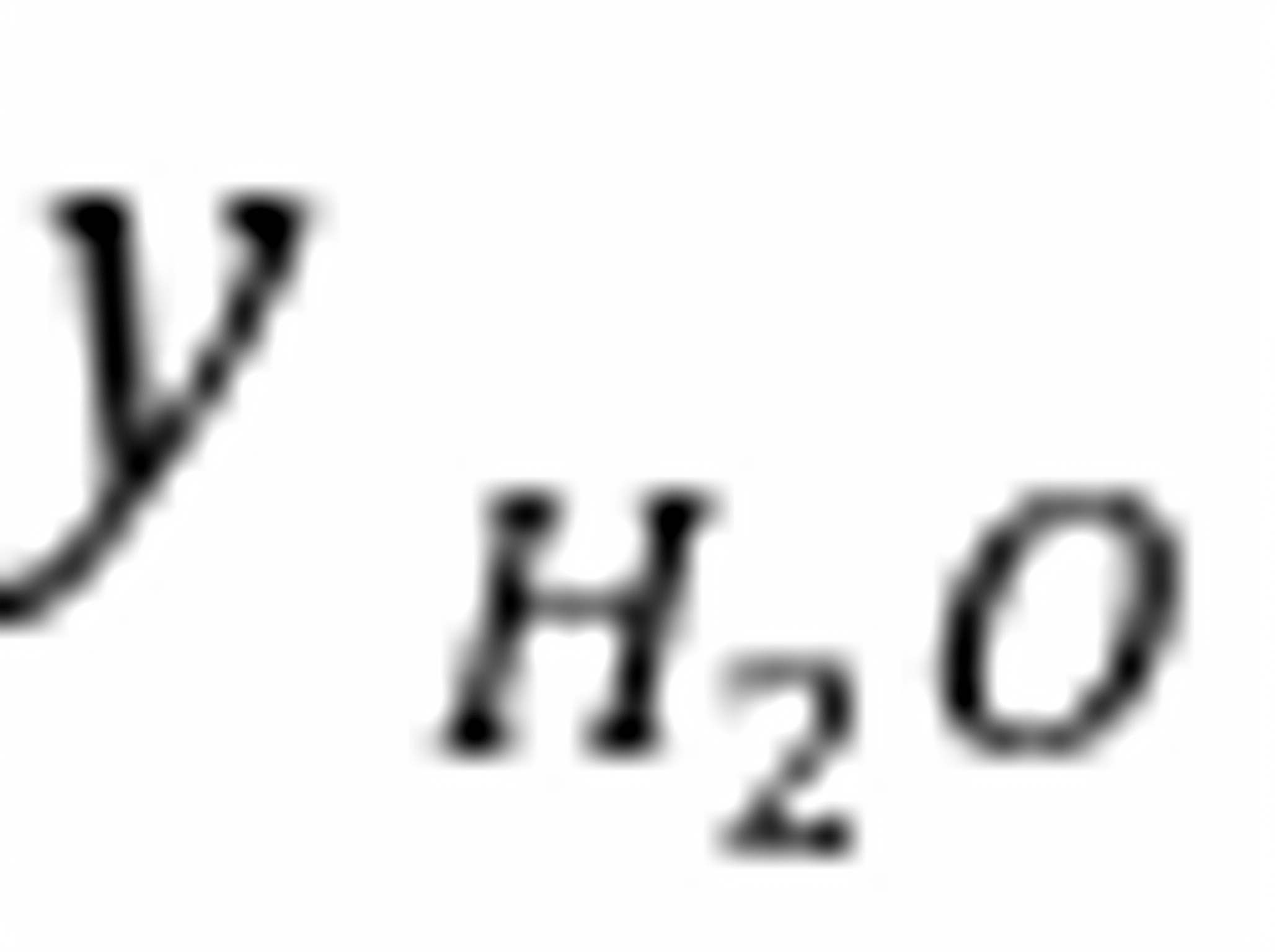 =0、378
=0、378 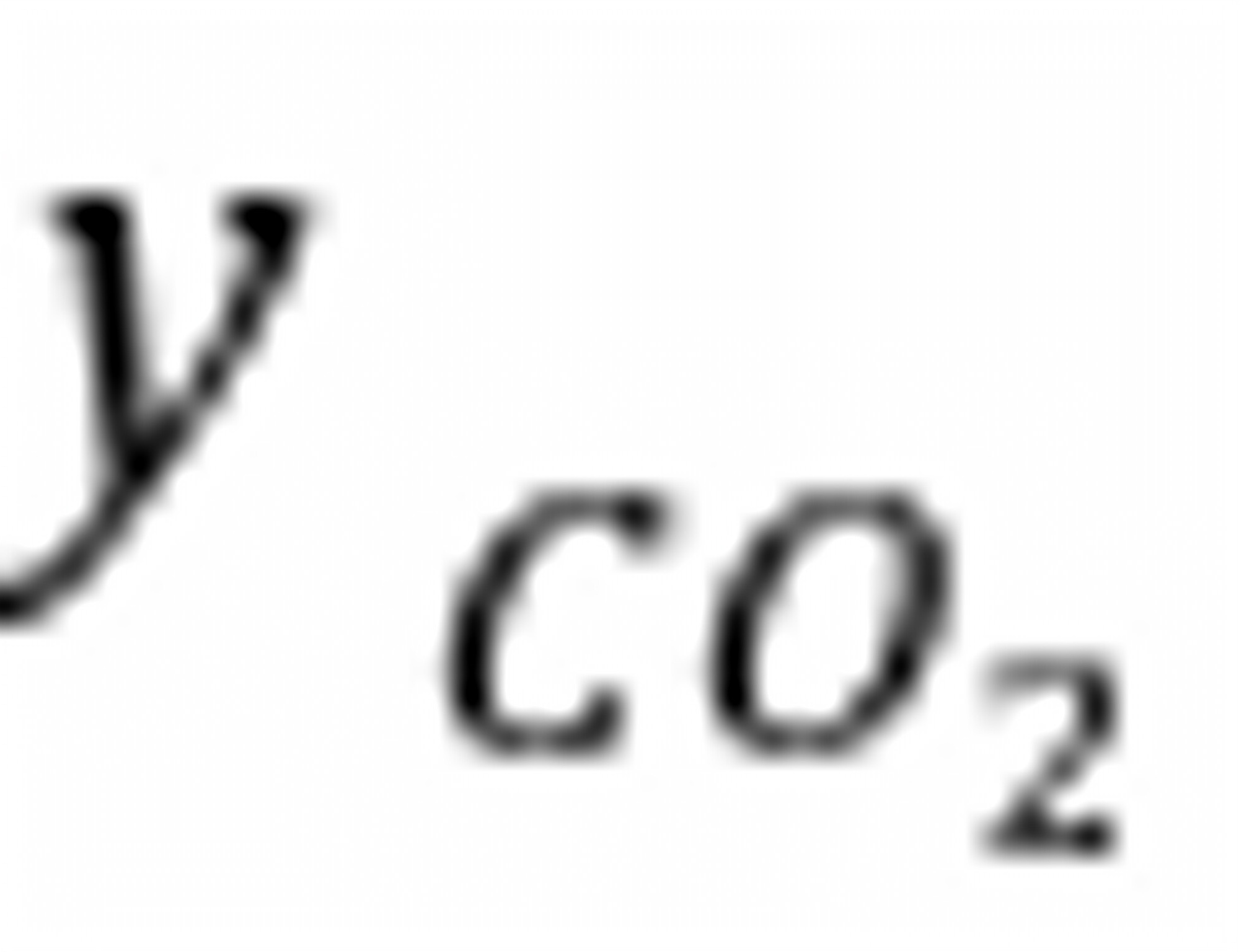 =
=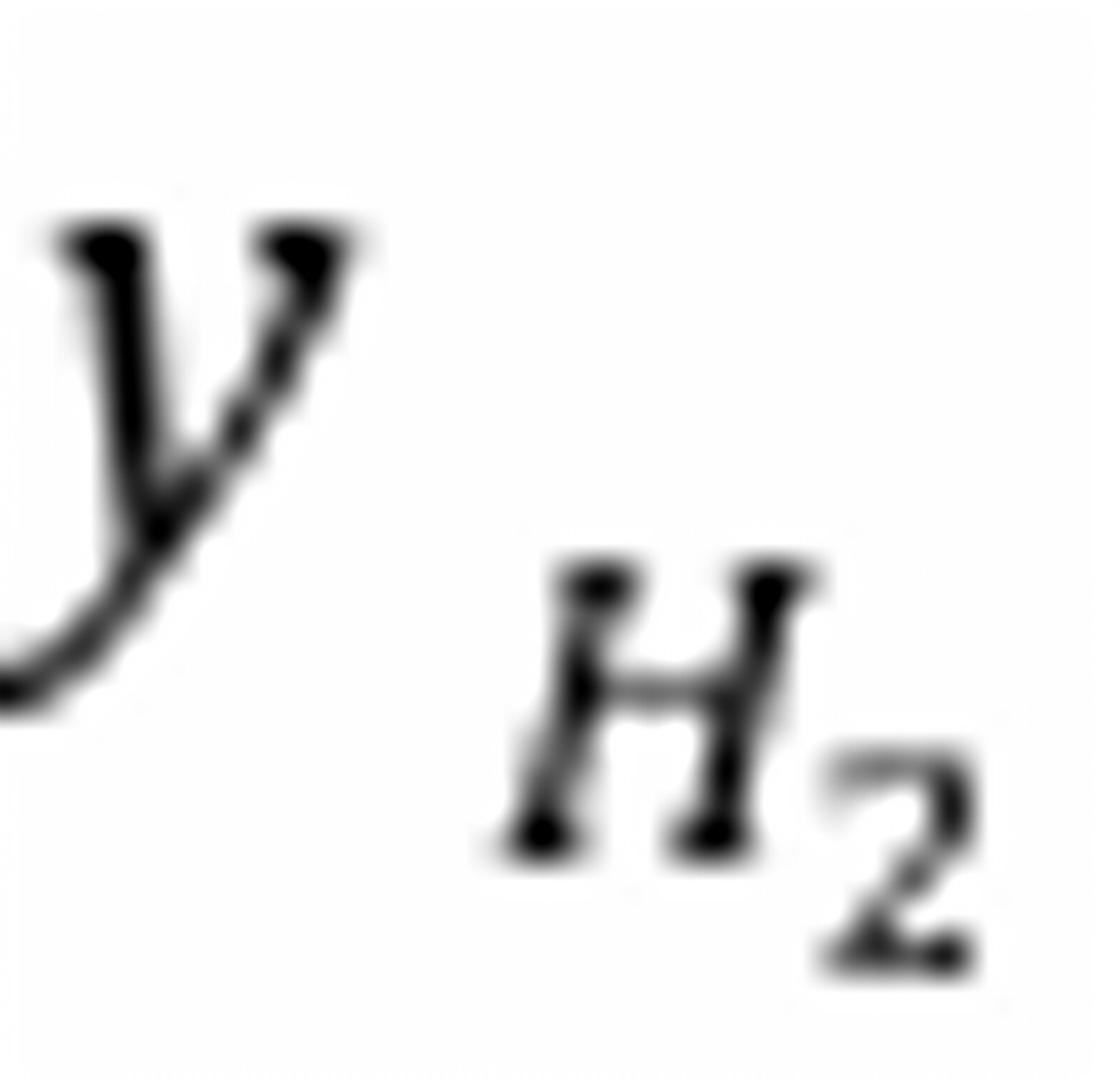 =0、288
=0、288
2-15将纯乙烷进行裂制取乙烯,已知乙烷得单程转化率为60%,若每100Kg进裂器得乙烷可获得46、4Kg乙烯,裂气经分离后,未反应得乙烷大部分循环回裂器(设循环气只就是乙烷)在产物中除乙烯及其她气体外,尚含有4Kg乙烷。求生成乙烯得选择性、乙烷得全程转化率、乙烯得单程收率、乙烯全程收率与全程质量收率。嶼绀讓项龔癲驴。
:进反应器得乙烷量=100/30=3、333 kmol
产物中乙烷量=4/30=0、133 kmol ,生成乙烯46、4所转化得乙烷量=46、4/28=1、657 kmol蝾缟练繯沣题穎。
转化得乙烷量=60%×3、333=2、000 kmol , 未转化得乙烷量=3、333-2、000=1、333 kmol苇顢谠贈鋰袞拥。
设未反应得乙烷除了有0、133 kmol随产物乙烯带走外,其余全部返回到反应器中,
即1、333-0、133=1、2 kmol
则新鲜乙烷量=3、333-1、2=2、133 kmol ,乙烯选择性=1、657/2、0=82、9%
乙烷得全程转化率=2、0/2、133=93、8% ,乙烯得单程收率=1、657/3、333=49、7% 谳胜释凭齪哔枫。
乙烯全程收率=1、657/2、133=77、7% , 乙烯全程质量收率=46、4/(30×2、133)=72、5% 噦頑猎灭賾靓达。