题目
例 2-10 已知下列化合物在298.15K时的标准生成吉布斯能-|||-C6H6(1)-|||-NH3(g)-|||-C6H5NH2(1)-|||-H2O(g)-|||-(Delta )_(1)(G)_(m)/(kJcdot (mol)^-1)-|||-124.14-|||--16.64-|||-153.22-|||--228.60 -394.38-|||-CO2(g)-|||-求下列反应在298.15K时的 Delta (G)_(m)-|||-(1) _(6)(H)_(6)(1)+N(H)_(3)(g)arrow (C)_(6)(H)_(5)N(H)_(2)(1)+(H)_(2)(g)-|||-(2)C(石墨 +2(H)_(2)O(g)arrow C(O)_(2)(g)+2(H)_(2)(g)

题目解答
答案
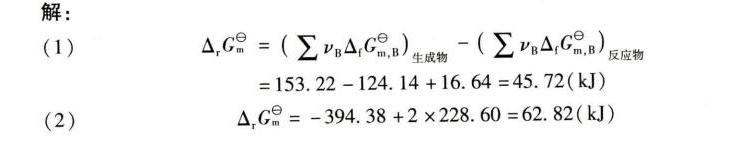
解析
本题考查反应吉布斯能的计算,核心思路是利用标准生成吉布斯能数据,通过公式:
$\Delta G^\theta = \sum \Delta G_{f}^\theta (\text{产物}) - \sum \Delta G_{f}^\theta (\text{反应物})$
计算反应的吉布斯能变化。需注意:
- 元素的稳定态形式(如石墨碳、H₂(g)等)的标准生成吉布斯能为0;
- 化学计量数需与反应式一致。
反应(1):$C_6H_6(l) + NH_3(g) \rightarrow C_6H_5NH_2(l) + H_2(g)$
-
确定各物质的标准生成吉布斯能:
- $C_6H_6(l)$:$124.14 \, \text{kJ/mol}$
- $NH_3(g)$:$-16.64 \, \text{kJ/mol}$
- $C_6H_5NH_2(l)$:$153.22 \, \text{kJ/mol}$
- $H_2(g)$(元素稳定态):$0 \, \text{kJ/mol}$
-
代入公式计算:
$\Delta G^\theta = [153.22 + 0] - [124.14 + (-16.64)] = 153.22 - 107.5 = 45.72 \, \text{kJ}$
反应(2):$C(\text{石墨}) + 2H_2O(g) \rightarrow CO_2(g) + 2H_2(g)$
-
确定各物质的标准生成吉布斯能:
- $C(\text{石墨})$(元素稳定态):$0 \, \text{kJ/mol}$
- $H_2O(g)$:$-228.60 \, \text{kJ/mol}$
- $CO_2(g)$:$-394.38 \, \text{kJ/mol}$
- $H_2(g)$(元素稳定态):$0 \, \text{kJ/mol}$
-
代入公式计算:
$\Delta G^\theta = [-394.38 + 2 \times 0] - [0 + 2 \times (-228.60)] = -394.38 + 457.2 = 62.82 \, \text{kJ}$